Clear Sky Science · fr
L’inflammation neuroauto-immune provoque la mort neuronale via la parthanatose médiée par la nucléase MIF
Pourquoi l’inflammation cérébrale est importante
La sclérose en plaques et les maladies apparentées n’attaquent pas seulement l’isolant qui entoure les fibres nerveuses : elles entraînent aussi, progressivement, la mort des neurones eux‑mêmes. Cette perte discrète de neurones est à l’origine des troubles de la marche, de la vision et des fonctions cognitives qui peuvent persister même lorsque les rechutes sont contrôlées. L’étude résumée ici pose une question fondamentale et cruciale : lors de l’inflammation auto‑immune du cerveau et de la moelle épinière, comment les neurones meurent‑ils précisément, et peut‑on bloquer ce processus sans neutraliser complètement le système immunitaire ?
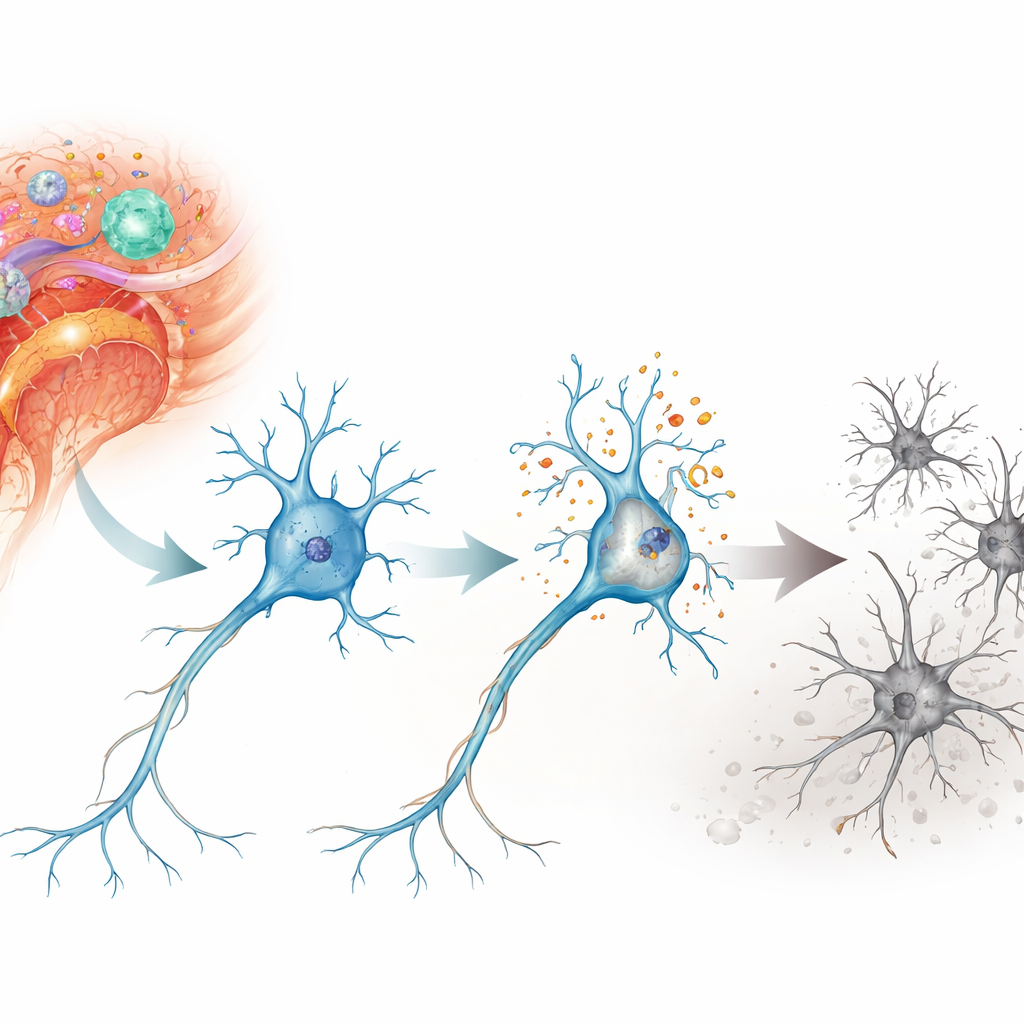
Une réaction en chaîne délétère à l’intérieur des neurones
Les auteurs se sont concentrés sur une forme de mort cellulaire appelée parthanatose, un programme déclenché par des dommages sévères à l’ADN plutôt que par la voie d’autodestruction plus familière qu’est l’apoptose. Dans un modèle murin d’inflammation neuroauto‑immune, l’encéphalomyélite auto‑immune expérimentale, ils ont étudié les neurones de la moelle épinière et de la rétine — des zones atteintes dans la sclérose en plaques. Ils ont observé des signes nets de ruptures d’ADN et de stress oxydatif dans ces neurones, en particulier dans les motoneurones de la moelle épinière et dans les cellules ganglionnaires rétiniennes qui relient l’œil au cerveau. Sur des jours à des semaines, ces cellules ont été progressivement perdues, ce qui correspond à l’aggravation du handicap neurologique chez les animaux.
Suivre le scénario de mort appelé parthanatose
En examinant plus finement, l’équipe a retracé les étapes moléculaires de la parthanatose à l’intérieur des neurones affectés. Lorsqu’ADN était endommagé, une enzyme nucléaire nommée PARP1 devenait hyperactive et produisait de longues chaînes d’une molécule appelée PAR. Ces chaînes débordaient dans le corps cellulaire, où elles contribuaient à déclencher la libération d’une protéine mitochondriale (AIF) qui s’associe à une autre protéine, le facteur inhibiteur de migration des macrophages (MIF). Le complexe AIF–MIF retournait alors vers le noyau. Là, MIF agissait comme une nucléase — une enzyme qui coupe l’ADN — provoquant une fragmentation à grande échelle du génome et scellant le sort du neurone. Les auteurs ont détecté chacun de ces marqueurs, y compris un excès de PAR, la liaison AIF–MIF et l’accumulation de MIF dans les noyaux neuronaux, au pic de la maladie chez la souris et, dans une moindre mesure, dans des tissus cérébraux humains provenant d’une personne atteinte de sclérose en plaques.
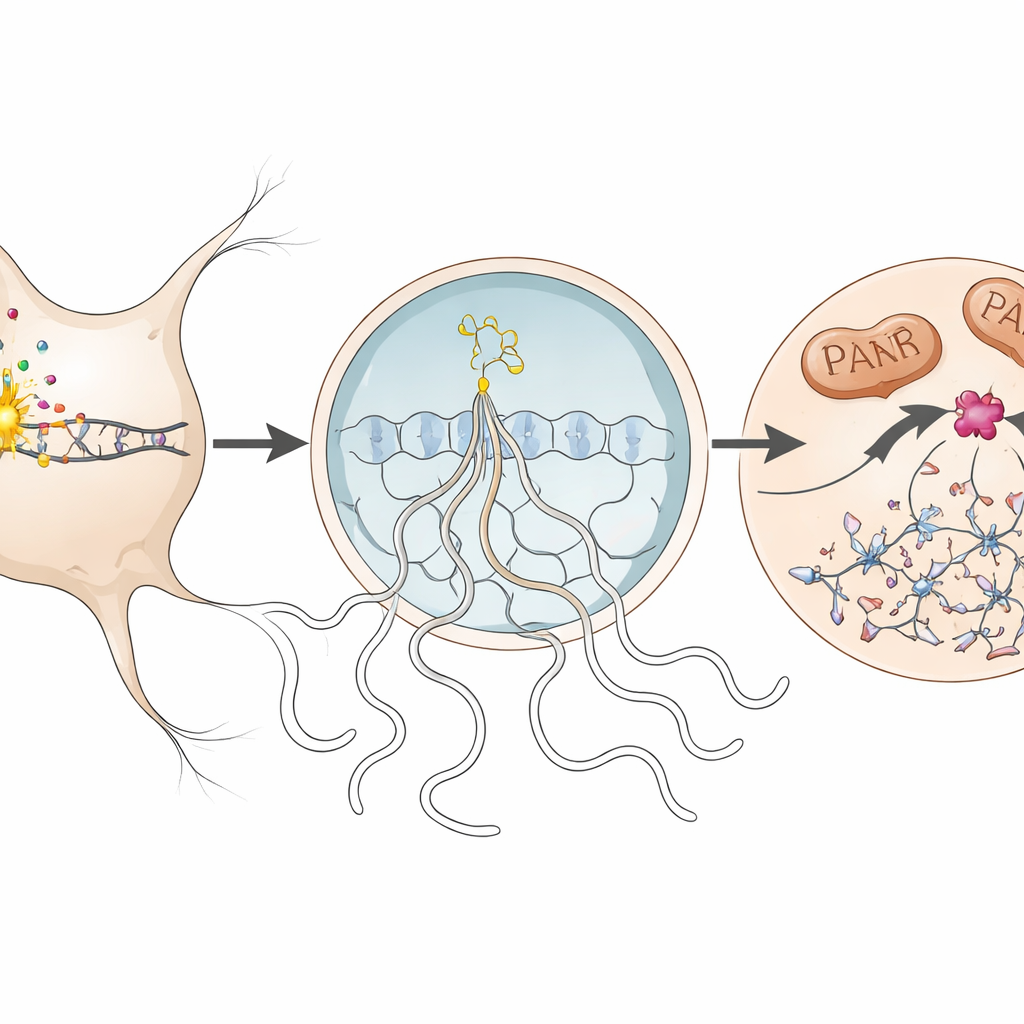
Protéger les neurones en désactivant une seule enzyme
Pour vérifier si cette voie est bien responsable de la perte neuronale, les chercheurs ont neutralisé l’activité nucléasique de MIF de deux manières complémentaires. D’abord, ils ont utilisé une souris knock‑in portant une mutation subtile de MIF (E22Q) qui préserve ses autres fonctions mais l’empêche de couper l’ADN. Chez ces animaux, l’attaque auto‑immune contre la myéline et l’infiltration des cellules immunitaires dans la moelle épinière étaient inchangées, pourtant les neurones de la moelle épinière et de la rétine étaient significativement mieux préservés et les scores de handicap à long terme étaient plus faibles que chez les souris normales. Ensuite, ils ont traité des souris avec PAANIB‑1, une petite molécule qui bloque sélectivement l’activité nucléasique de MIF. Qu’il soit administré de façon préventive ou après l’apparition des symptômes, ce médicament a réduit la perte neuronale dans la phase chronique de la maladie sans modifier l’infiltration des cellules immunitaires, l’activation gliale ou le degré de démyélinisation.
Les neurones réagissent différemment lorsque la parthanatose est bloquée
L’équipe a ensuite demandé en quoi les neurones survivants diffèrent au niveau de l’activité génique. En utilisant le séquençage ARN d’un grand nombre de noyaux isolés de tissu médullaire, ils ont profilé des dizaines de milliers de neurones provenant de souris normales et de souris porteuses de la mutation MIF, avec ou sans maladie. Chez les souris standards atteintes d’inflammation auto‑immune, les neurones ont activé de nombreux gènes liés au système immunitaire, y compris des voies répondant aux signaux d’interféron et participant à la présentation d’antigènes, tout en réduisant l’expression de gènes essentiels à la transmission électrique normale, à la communication par neurotransmetteurs et à la production de facteurs de croissance protecteurs. En revanche, les neurones des souris mutantes pour MIF ont conservé une grande partie de cette expression génique fonctionnelle de base, même si certains programmes inflammatoires étaient parfois encore plus fortement activés. Une réanalyse de données cérébrales humaines de sclérose en plaques a montré une suppression similaire, à long terme, des gènes de fonction neuronale basique, suggérant que les observations chez la souris reflètent des changements chez l’homme.
Ce que cela signifie pour les traitements à venir
Pris ensemble, les résultats désignent la parthanatose — et plus précisément l’étape finale de découpe de l’ADN assurée par MIF — comme une voie clé par laquelle l’inflammation tue les neurones dans les maladies auto‑immunes. Fait notable, bloquer l’activité nucléasique de MIF a épargné les neurones sans atténuer la réponse immunitaire globale ni modifier la perte de myéline, et les neurones protégés présentaient des profils d’expression génique plus sains. En termes simples pour un lecteur non spécialiste, l’étude identifie un « interrupteur » moléculaire concret pour un programme de mort destructeur à l’intérieur des neurones. Des médicaments ciblés visant cet interrupteur pourraient, en principe, apporter une véritable neuroprotection aux côtés des thérapies actuelles centrées sur le système immunitaire pour la sclérose en plaques et d’autres affections inflammatoires du cerveau et de la moelle épinière.
Citation: Mace, J.W., Gadani, S.P., Smith, M.D. et al. Autoimmune neuroinflammation leads to neuronal death via MIF nuclease-mediated parthanatos. Nat Neurosci 29, 796–809 (2026). https://doi.org/10.1038/s41593-026-02201-7
Mots-clés: sclérose en plaques, neuroinflammation, mort des cellules neuronales, parthanatose, nucléase MIF