Clear Sky Science · nl
Auto-immune neuroinflammatie leidt tot neuronale sterfte via MIF-nuclease-gemedieerde parthanatos
Waarom ontsteking in de hersenen ertoe doet
Multiple sclerose en verwante aandoeningen vallen niet alleen de isolatie rond zenuwvezels aan—ze doden ook geleidelijk de zenuwcellen zelf. Dit verborgen verlies van neuronen veroorzaakt problemen met lopen, zicht en denken die kunnen voortduren zelfs wanneer terugvallen onder controle zijn. De samengevatte studie stelt een fundamentele maar cruciale vraag: tijdens auto-immune ontsteking van hersenen en ruggenmerg, op welke manier sterven neuronen precies, en kan dat proces worden geblokkeerd zonder het immuunsysteem volledig uit te schakelen?
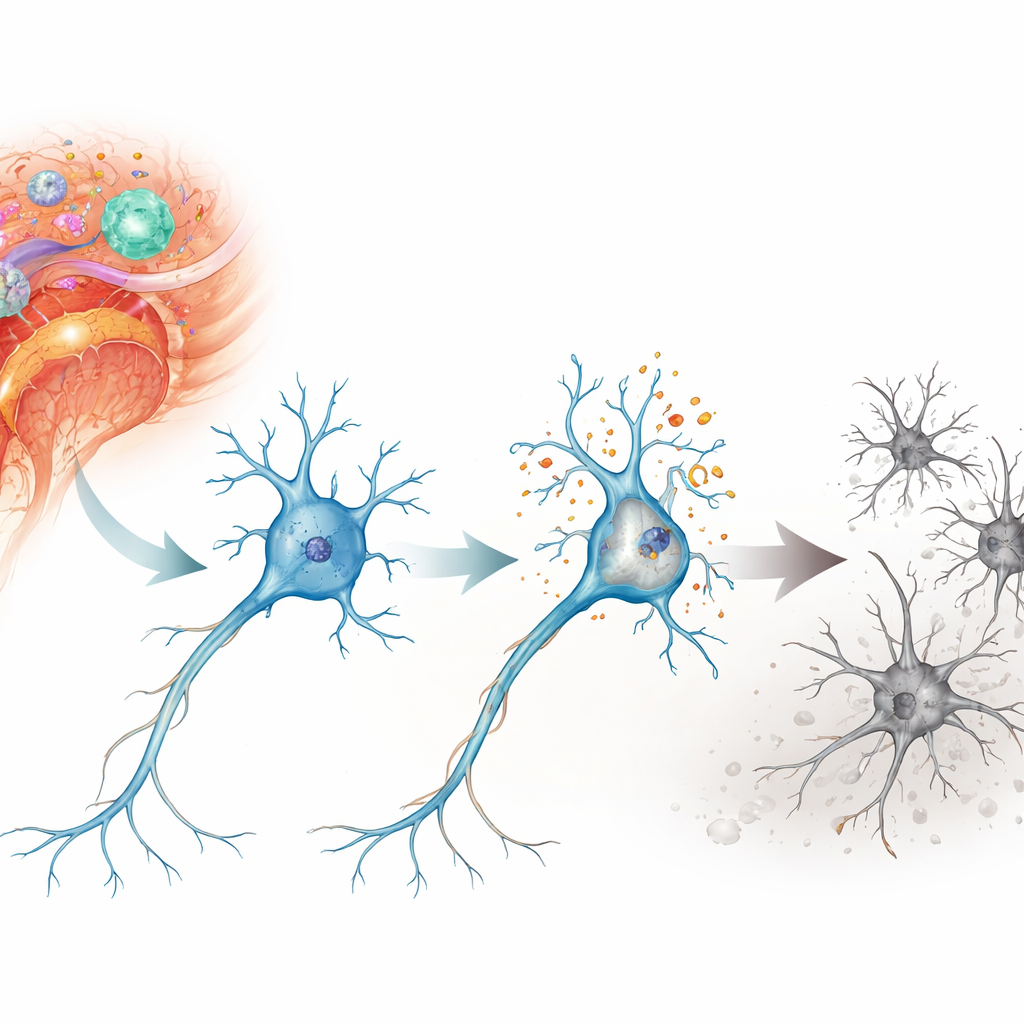
Een schadelijke kettingreactie binnen neuronen
De onderzoekers concentreerden zich op een vorm van celdood die parthanatos wordt genoemd, een programma dat wordt geactiveerd door ernstige DNA-schade in plaats van door het meer bekende zelfmoordpad van apoptose. In een muismodel van auto-immune neuroinflammatie, bekend als experimentele auto-immune encefalomyelitis, onderzochten ze neuronen in het ruggenmerg en netvlies—gebieden die bij multiple sclerose beschadigd raken. Ze vonden sterke aanwijzingen voor DNA-breuken en oxidatieve stress in deze neuronen, vooral in motorneuronen van het ruggenmerg en in retinale ganglioncellen die het oog met de hersenen verbinden. Gedurende dagen tot weken gingen deze cellen geleidelijk verloren, wat overeenkwam met het tijdsverloop van verslechterende neurologische invaliditeit bij de dieren.
Een sterfscript volgen dat parthanatos heet
Nauwkeuriger kijkend traceerde het team de moleculaire stappen van parthanatos binnen de aangetaste neuronen. Wanneer DNA beschadigd raakte, werd een enzym in de kern genaamd PARP1 overactief en produceerde lange ketens van een molecuul genaamd PAR. Deze ketens stroomden naar het cellichaam, waar ze hielpen het vrijkomen van een mitochondriaal eiwit (AIF) te veroorzaken dat samenwerkt met een ander eiwit, macrophage migration inhibitory factor (MIF). Het AIF–MIF-complex keerde vervolgens terug naar de kern. Daar fungeerde MIF als een nuclease—een enzym dat DNA knipt—waardoor grootschalige fragmentatie van het genoom ontstond en het lot van de neuron werd bezegeld. De auteurs detecteerden elk van deze kenmerken, inclusief overtollig PAR, AIF–MIF-binding en accumulatie van MIF in neuronale kernen, tijdens het piekstadium van de ziekte bij de muizen en, in beperktere mate, in menselijke hersenweefsels van een persoon met multiple sclerose.
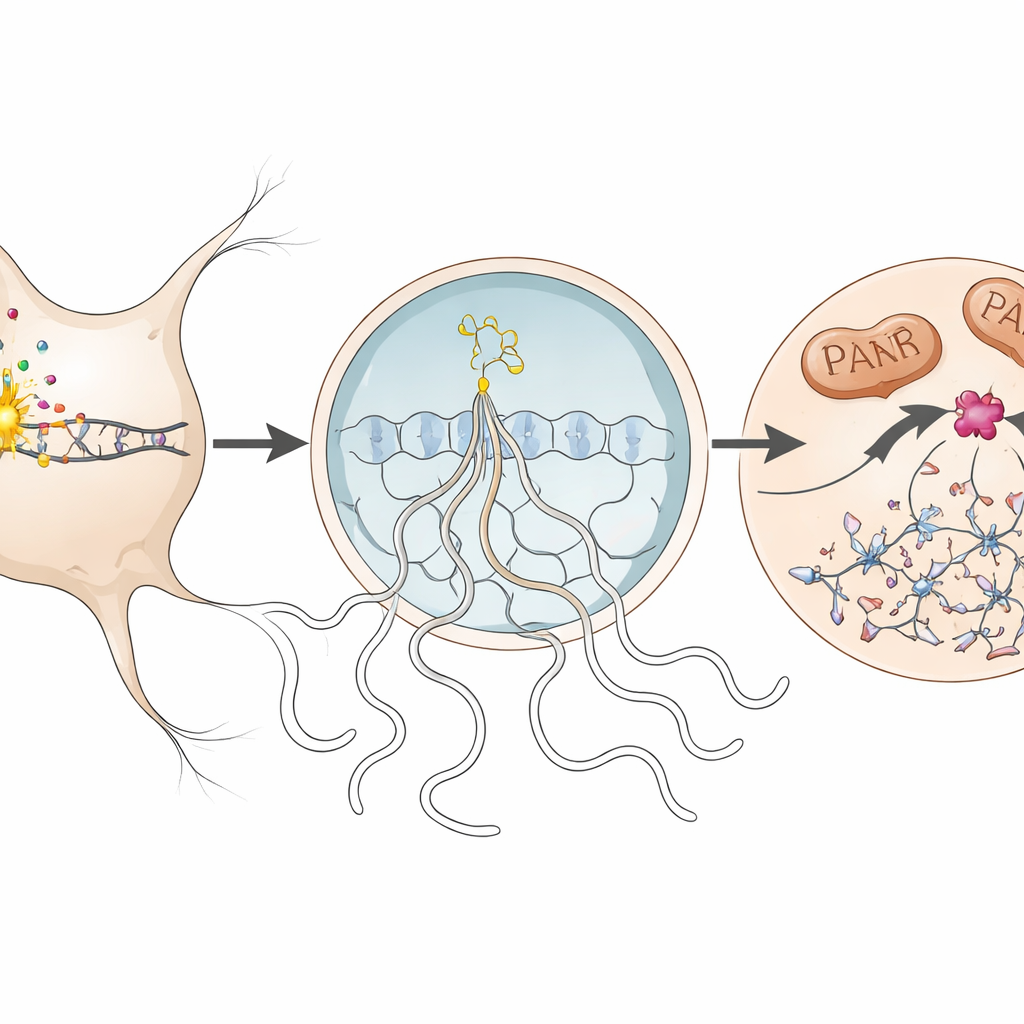
Neuronen beschermen door één enzym uit te schakelen
Om te testen of deze route daadwerkelijk het neuronverlies aandrijft, schakelden de onderzoekers de nuclease-activiteit van MIF op twee complementaire manieren uit. Ten eerste gebruikten ze een knock-in-muis met een subtiele mutatie in MIF (E22Q) die de andere functies behouden laat maar voorkomt dat het DNA knipt. Bij deze dieren waren de auto-immune aanval op myeline en de toestroom van immuuncellen naar het ruggenmerg ongewijzigd, maar neuronen in ruggenmerg en netvlies werden significant beter behouden en de langetermijn-scores voor invaliditeit waren lager dan bij normale muizen. Ten tweede behandelden ze muizen met PAANIB-1, een kleine molecule die selectief de nuclease-activiteit van MIF blokkeert. Of het middel nu preventief werd gegeven of nadat symptomen waren begonnen, het verminderde neuronverlies in de chronische fase van de ziekte zonder de immuuncelinfiltratie, gliale activatie of de mate van demyelinisatie te veranderen.
Neuronen reageren anders wanneer parthanatos wordt geblokkeerd
Het team vroeg zich vervolgens af hoe overgebleven neuronen verschillen op het niveau van genactiviteit. Met single-nucleus RNA-sequencing van ruggenmergweefsel profielen ze tienduizenden neuronen van normale en MIF-mutante muizen met en zonder ziekte. Bij standaardmuizen met auto-immune ontsteking zetten neuronen veel immuungerelateerde genen aan, waaronder paden die reageren op interferonsignalen en helpen antigenen te presenteren, terwijl ze genen voor normale elektrische signalering, neurotransmittercommunicatie en de productie van beschermende groeifactoren omlaag schroefden. Daarentegen behielden neuronen in MIF-mutante muizen veel van deze kernfunctionele genexpressie, ook al werden sommige inflammatoire programma’s zelfs sterker geactiveerd. Een heranalyse van menselijke multiple sclerose-hersendata toonde een vergelijkbare langdurige onderdrukking van basisgenen voor neuronale functies, wat suggereert dat de muisbevindingen veranderingen bij mensen weerspiegelen.
Wat dit betekent voor toekomstige behandelingen
Samengevoegd wijzen de resultaten op parthanatos—en specifiek de laatste DNA-knipstap uitgevoerd door MIF—als een sleutelroute waardoor ontsteking neuronen in auto-immune ziekte doodt. Belangrijk is dat het blokkeren van de nuclease-activiteit van MIF neuronen spaarde zonder de bredere immuunreactie te dempen of myelineverlies te veranderen, en de beschermde neuronen leken gezondere patronen van genactiviteit te behouden. Voor de niet-specialist komt het erop neer dat dit werk een concreet moleculair "uitschakelaar" identificeert voor een destructief sterfprogramma binnen neuronen. Gerichte geneesmiddelen die deze schakel omzetten zouden in principe echte neuroprotectie kunnen toevoegen aan bestaande immuungerichte therapieën voor multiple sclerose en andere inflammatoire aandoeningen van hersenen en ruggenmerg.
Bronvermelding: Mace, J.W., Gadani, S.P., Smith, M.D. et al. Autoimmune neuroinflammation leads to neuronal death via MIF nuclease-mediated parthanatos. Nat Neurosci 29, 796–809 (2026). https://doi.org/10.1038/s41593-026-02201-7
Trefwoorden: multiple sclerose, neuroinflammatie, neuronaal celverlies, parthanatos, MIF-nuclease