Clear Sky Science · de
Autoimmune Neuroinflammation führt mittels MIF-Nuklease-vermitteltem Parthanatos zum neuronalen Tod
Warum Entzündung im Gehirn wichtig ist
Multiple Sklerose und verwandte Erkrankungen greifen nicht nur die Isolierung um Nervenfasern an – sie töten auch nach und nach die Nervenzellen selbst. Dieser verdeckte Verlust von Neuronen treibt Probleme beim Gehen, Sehen und Denken voran, die weiterbestehen können, selbst wenn Schübe unter Kontrolle sind. Die hier zusammengefasste Studie stellt eine grundlegende, aber entscheidende Frage: Wie sterben Neuronen genau während einer autoimmunen Entzündung von Gehirn und Rückenmark, und lässt sich dieser Prozess blockieren, ohne das Immunsystem vollständig lahmzulegen?
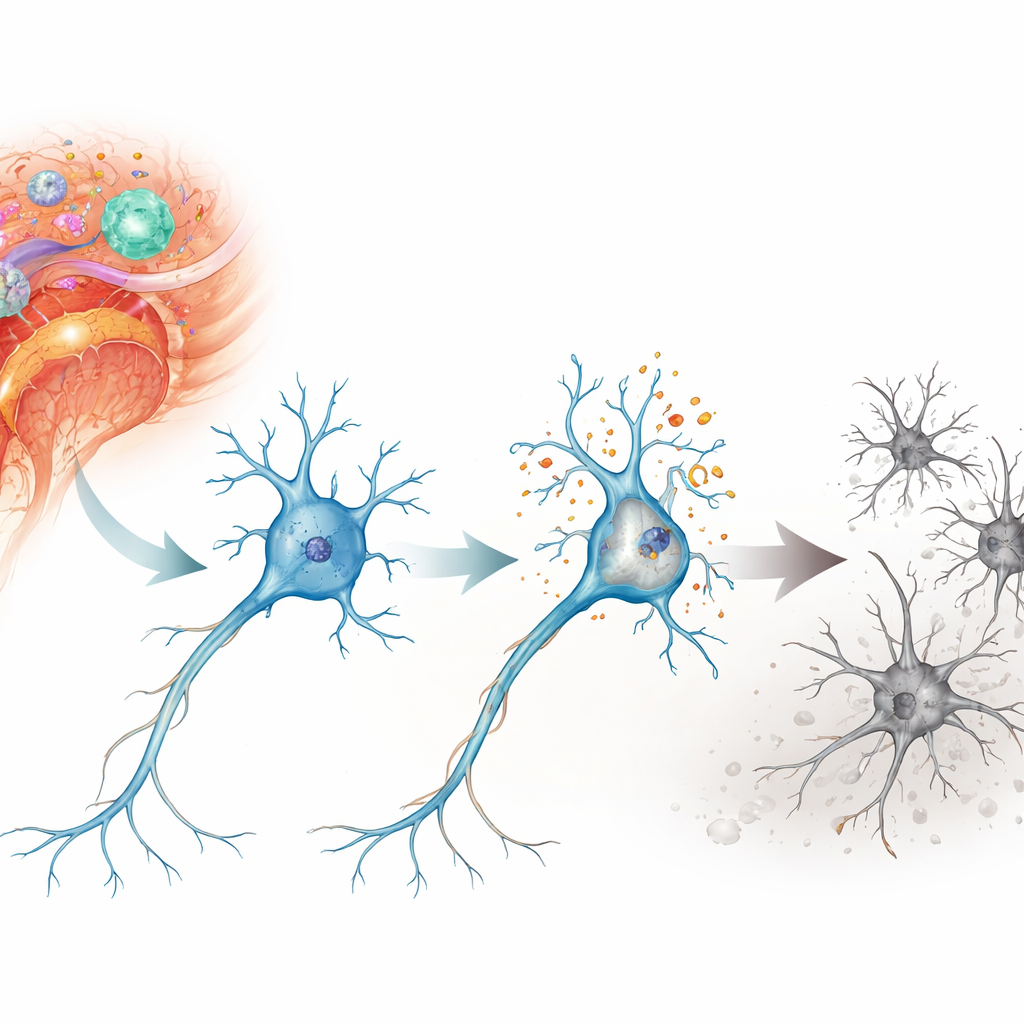
Eine schädliche Kettenreaktion in Neuronen
Die Forschenden konzentrierten sich auf eine Form des Zelltods namens Parthanatos, ein Programm, das durch schwere DNA-Schäden ausgelöst wird und sich von dem bekannteren Selbstmordmechanismus der Apoptose unterscheidet. In einem Mausmodell autoimmuner Neuroinflammation, bekannt als experimentelle autoimmune Enzephalomyelitis, untersuchten sie Neuronen im Rückenmark und in der Netzhaut – Regionen, die bei Multipler Sklerose verletzt werden. Sie fanden ausgeprägte Hinweise auf DNA-Brüche und oxidativen Stress in diesen Neuronen, insbesondere in Motoneuronen des Rückenmarks und in retinalen Ganglienzellen, die das Auge mit dem Gehirn verbinden. Über Tage bis Wochen gingen diese Zellen schrittweise verloren und entsprachen damit dem zeitlichen Verlauf der sich verschlechternden neurologischen Behinderung bei den Tieren.
Dem Todesdrehbuch namens Parthanatos folgen
Bei genauerer Untersuchung verfolgte das Team die molekularen Schritte des Parthanatos in den betroffenen Neuronen. Bei DNA-Schäden wurde ein Enzym im Zellkern namens PARP1 überaktiv und produzierte lange Ketten eines Moleküls namens PAR. Diese Ketten traten in den Zellkörper über, wo sie die Freisetzung eines mitochondrialen Proteins (AIF) förderten, das mit einem weiteren Protein, dem Macrophage Migration Inhibitory Factor (MIF), zusammenwirkt. Der AIF–MIF-Komplex wanderte dann zurück in den Zellkern. Dort fungierte MIF als Nuklease – ein Enzym, das DNA schneidet – und verursachte großflächige Fragmentierung des Genoms und besiegelte das Schicksal des Neurons. Die Autorinnen und Autoren detektierten alle diese Kennzeichen, einschließlich überschüssigem PAR, AIF–MIF-Bindung und Akkumulation von MIF in neuronalen Kernen, während der Höhephase der Erkrankung bei Mäusen und, in abgeschwächter Form, in Hirngewebe eines Menschen mit Multipler Sklerose.
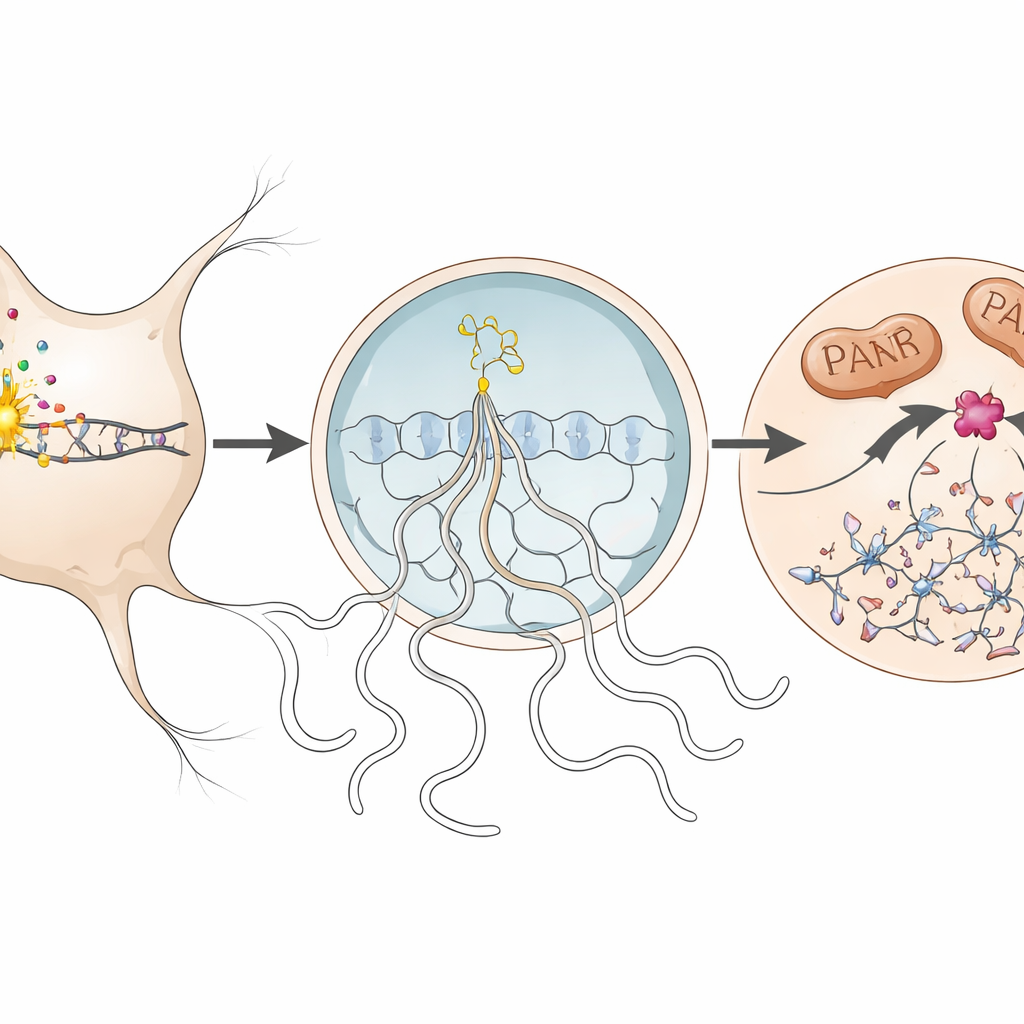
Neuronen schützen durch Entwaffnen eines einzelnen Enzyms
Um zu prüfen, ob dieser Weg tatsächlich den Neuronenverlust antreibt, deaktivierten die Forschenden die Nukleaseaktivität von MIF auf zwei komplementäre Weisen. Zuerst nutzten sie eine Knock-in-Maus, die eine subtile Mutation in MIF (E22Q) trägt, die seine anderen Funktionen intakt lässt, es ihm aber unmöglich macht, DNA zu schneiden. Bei diesen Tieren blieben der autoimmune Angriff auf das Myelin und der Einstrom von Immunzellen ins Rückenmark unverändert, doch die Neuronen im Rückenmark und in der Netzhaut waren deutlich besser erhalten, und die langfristigen Behinderungswerte waren niedriger als bei normalen Mäusen. Zweitens behandelten sie Mäuse mit PAANIB-1, einem kleinen Molekül, das selektiv die Nukleaseaktivität von MIF blockiert. Ob präventiv verabreicht oder nach Beginn der Symptome, dieses Medikament verringerte den Neuronenverlust in der chronischen Krankheitsphase, ohne den Zustrom von Immunzellen, die Aktivierung von Gliazellen oder das Ausmaß der Demyelinisierung zu verändern.
Neuronen reagieren unterschiedlich, wenn Parthanatos blockiert ist
Das Team untersuchte daraufhin, wie überlebende Neuronen auf Ebene der Genaktivität abweichen. Mithilfe von Single-Nucleus-RNA-Sequenzierung von Rückenmarkgewebe profilieren sie Zehntausende Neuronen aus normalen und MIF-mutanten Mäusen mit und ohne Erkrankung. In Standardmäusen mit autoimmuner Entzündung schalteten Neuronen viele immunbezogene Gene an, einschließlich Signalwegen, die auf Interferone reagieren und bei der Antigenpräsentation helfen, während Gene, die für normale elektrische Signalgebung, Neurotransmitter-Kommunikation und die Produktion schützender Wachstumsfaktoren wichtig sind, herunterreguliert wurden. Im Gegensatz dazu bewahrten Neuronen in MIF-mutanten Mäusen einen Großteil dieser zentralen funktionellen Genexpression, obwohl einige entzündliche Programme sogar stärker aktiviert waren. Eine Reanalyse von menschlichen Multipler-Sklerose-Hirndaten zeigte eine ähnliche langfristige Unterdrückung grundlegender neuronaler Funktionsgene, was darauf hindeutet, dass die Mausbefunde Veränderungen beim Menschen widerspiegeln.
Was das für zukünftige Therapien bedeutet
Insgesamt deuten die Ergebnisse darauf hin, dass Parthanatos – speziell der finale DNA-schneidende Schritt, der von MIF ausgeführt wird – ein wichtiger Weg ist, über den Entzündung in autoimmunen Erkrankungen Neuronen tötet. Wichtig ist, dass das Blockieren der Nukleaseaktivität von MIF Neuronen schützte, ohne die breitere Immunantwort zu dämpfen oder den Myelinverlust zu verändern, und die geschützten Neuronen schienen gesündere Muster der Genaktivität beizubehalten. Für eine nichtwissenschaftliche Leserschaft lässt sich das Fazit so zusammenfassen: Diese Arbeit identifiziert einen konkreten molekularen "Ausschalter" für ein zerstörerisches Todesprogramm in Neuronen. Zielgerichtete Medikamente, die diesen Schalter umlegen, könnten prinzipiell neben bestehenden immunfokussierten Therapien für Multiple Sklerose und andere entzündliche Erkrankungen von Gehirn und Rückenmark echte Neuroprotektion bieten.
Zitation: Mace, J.W., Gadani, S.P., Smith, M.D. et al. Autoimmune neuroinflammation leads to neuronal death via MIF nuclease-mediated parthanatos. Nat Neurosci 29, 796–809 (2026). https://doi.org/10.1038/s41593-026-02201-7
Schlüsselwörter: Multiple Sklerose, Neuroinflammation, Neuronaler Zelltod, Parthanatos, MIF-Nuklease