Clear Sky Science · zh
3d-OT:一种面向几何的深度框架,用于空间多组学异构切片的对齐
在三维中观察组织
生物学家现在不仅能测量细胞中哪些分子处于活跃状态,还能确定该细胞在组织中的确切位置。这些新的“空间”图谱有望更清晰地展示大脑的连接方式、肿瘤的扩散路径以及胚胎如何构建器官。然而,大多数实验仍然只采集薄层切片,且每种切片使用不同的测量类型和分辨率。本文提出了3d-OT,一种计算方法,可将这些切片缝合成连贯的三维视图,同时最大化利用每个切片中丰富的分子信息。
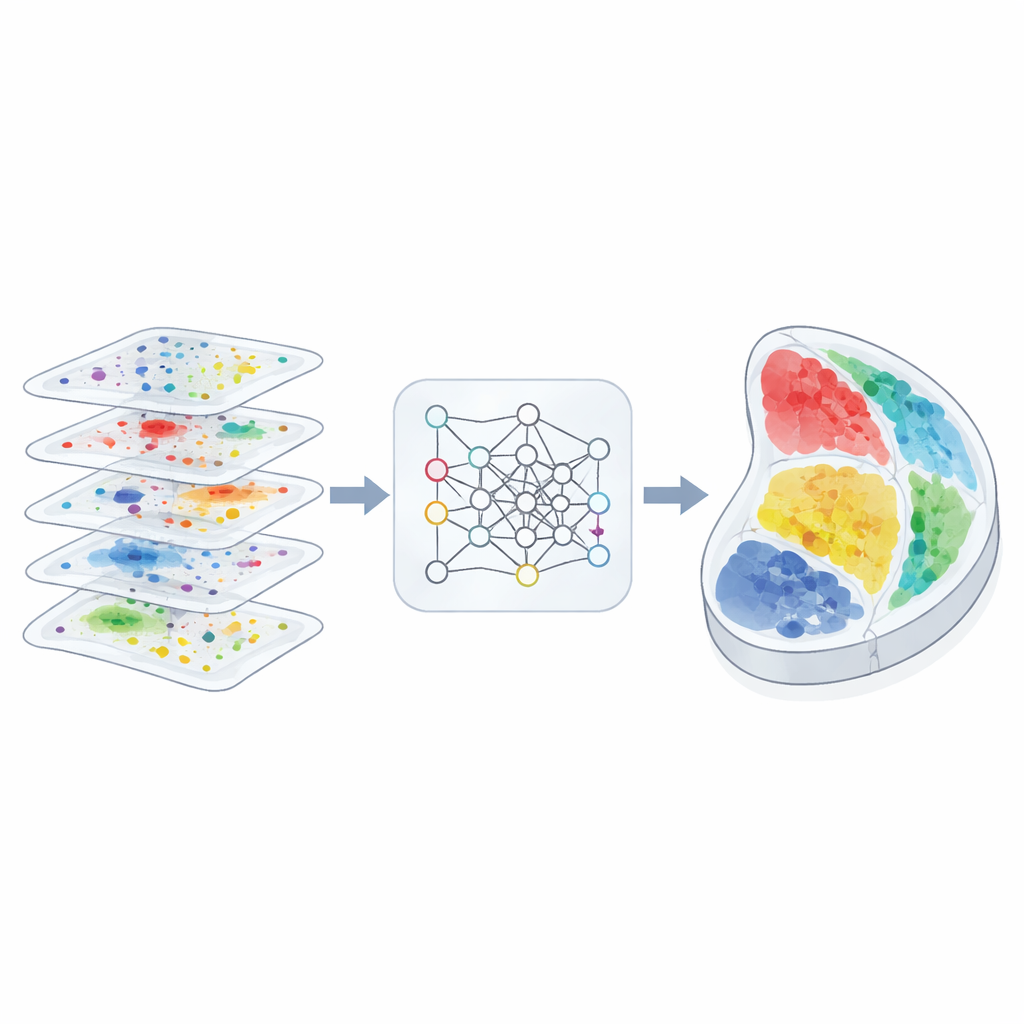
为什么空间映射很重要
传统的遗传学和基因组学告诉我们细胞包含哪些分子,但不知道这些细胞位于何处。空间技术通过记录组织中每个微小位点的分子谱和其物理坐标改变了这一点。不同方法强调不同的分子层:有的描绘RNA,有的测定蛋白质,有的检测DNA上的化学修饰。每一层都揭示了组织结构的不同侧面。挑战在于,研究人员常常得到多个部分重叠、采用不同工具测量的切片。如何在不丢失细致解剖细节的情况下,将这些异构切片一致地对齐到统一的三维空间,一直是一个未解决的主要问题。
一种面向几何的组织视角
作者设计3d-OT时,将每个组织切片视为“点云”,即物理空间中的一簇带有多组学测量的点。3d-OT并不主要依赖网格或图来描述邻域关系,而是采用了一种名为PointNet++的神经网络架构,该架构最初用于三维物体识别。该网络在多次迭代中不仅向每个点输入其分子信号,还输入其精确坐标,使模型能够学习诸如分层的皮层结构或弯曲的器官边界等细微的几何模式。对于同时具有多种分子层的切片,一个融合模块将这些模态混合为共享表示,同时保留每一层的独特贡献。
用软匹配来对齐切片
3d-OT的第二个核心是基于“最优传输”的对齐模块,这是一种在保持整体形状的同时匹配两个分布的数学框架。该方法并不强制在两片切片之间进行刚性的逐点一一配对,而是计算软对应关系:源切片中的每个点可以部分地匹配目标切片中的若干候选点。基于Chamfer距离的重建损失奖励那些使重建位置与真实目标位置高度吻合的对齐。额外的平滑性和“零散度”约束鼓励点在切片之间的流动遵循现实的、连续的组织变形(例如弯曲、拉伸或生长),而不是不合理的跳跃或扭转。
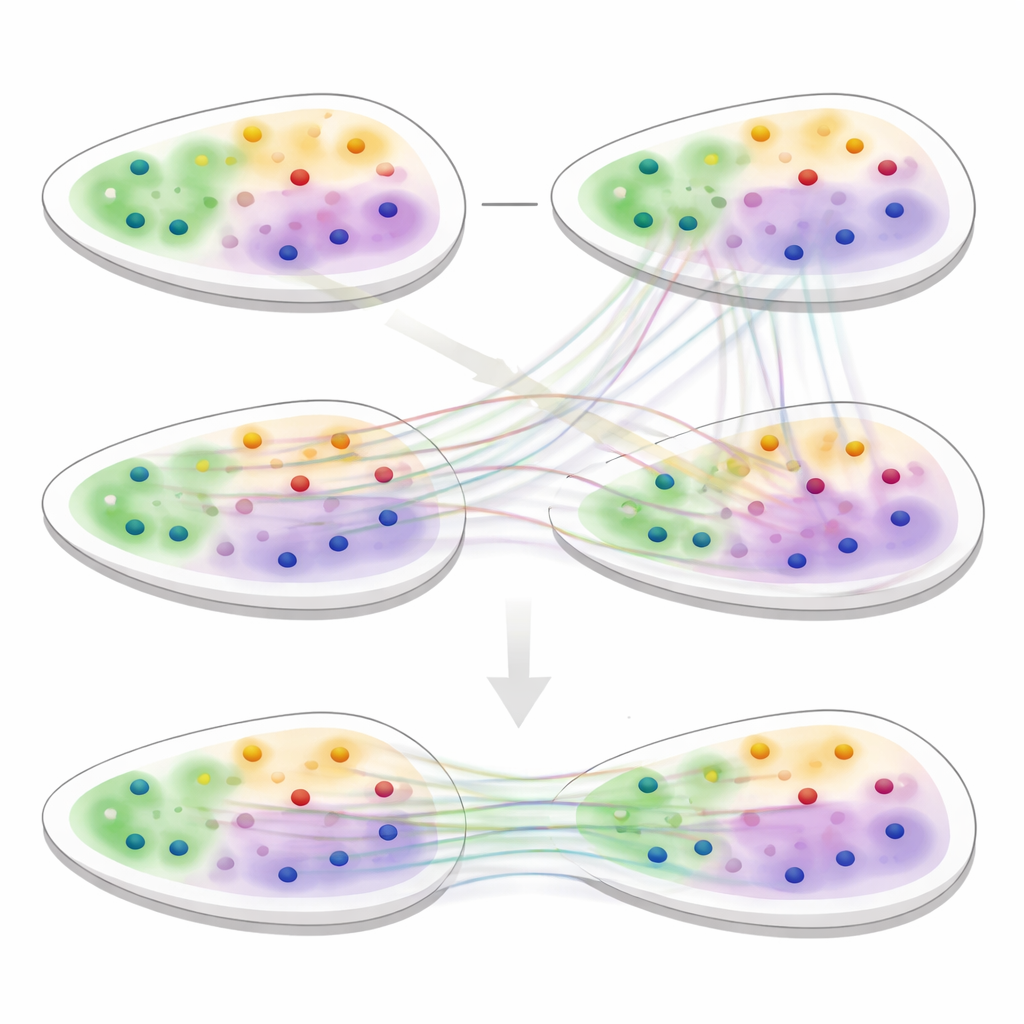
揭示隐藏的组织结构
为了测试3d-OT,团队将其与领先的空间分析工具在多种数据集上进行了比较,包含人脑、乳腺癌、淋巴结和多种小鼠器官。在单切片聚类任务中,3d-OT更准确地恢复了已知的人类和小鼠皮层层次,并且比竞争方法更好地区分了癌症区域。在将RNA与染色质标记结合的多组学小鼠大脑数据中,它将最深皮层内常被视为单一带的两个亚层分离开来,并突出了这些细微区域的标记基因。在多种技术和分辨率下,包括具有挑战性的心脏和神经嵴组织,3d-OT比现有对齐方法提供了更平滑、更符合解剖学的对齐结果。
追踪器官随时间的变化
也许最引人注目的演示来自对小鼠胚胎发育的重建。利用来自多个胚胎发育日的空间数据,3d-OT跨越时间对齐切片,构建了器官生长的三维“电影”。例如,它捕捉到心脏如何从紧凑形态变为环状结构再恢复,以及肝脏如何稳步扩展。该方法还将早期前体区与后期器官连接起来,正确追踪了泌尿生殖脊向肾和卵巢的演变,以及皮肌节向肌肉和结缔组织的分化。这些轨迹与已知的发育生物学相符,同时也提出了用于进一步研究的附加分化路径。
对未来生物学的意义
简而言之,3d-OT将分散的、多层的组织快照转化为一致的、高分辨率的三维地图,既尊重分子身份也尊重物理形状。通过显式编码几何信息并允许切片之间灵活的软匹配,它在识别微小组织区域以及对齐来自不同技术与时间点的数据方面优于早期工具。随着空间多组学数据集的增长,像3d-OT这样的工具将帮助研究人员从平面图像迈向器官在健康、疾病和发育中的动态三维图谱。
引用: Dai, B., Yi, L., Wang, P. et al. 3d-OT: a deep geometry-aware framework for heterogeneous slices alignment of spatial multi-omics. Nat Methods 23, 760–771 (2026). https://doi.org/10.1038/s41592-026-03034-9
关键词: 空间组学, 多组学整合, 组织三维重建, 胚胎发育, 计算生物学