Clear Sky Science · it
3d-OT: un framework profondo sensibile alla geometria per l'allineamento di fette eterogenee della multi-omica spaziale
Vedere i tessuti in tre dimensioni
I biologi sono sempre più in grado di misurare non solo quali molecole sono attive in una cellula, ma anche esattamente dove quella cellula si trova all'interno di un tessuto. Queste nuove mappe “spaziali” promettono visioni più nitide di come sono connessi i cervelli, di come si diffondono i tumori e di come gli embrioni costruiscono gli organi. Tuttavia, la maggior parte degli esperimenti cattura ancora solo sottili sezioni, ognuna con diversi tipi di misura e risoluzioni. Questo articolo presenta 3d-OT, un metodo computazionale che unisce quelle fette in viste 3D coerenti, sfruttando al massimo le ricche informazioni molecolari presenti in ogni sezione.
Perché mappare lo spazio è importante
La genetica e la genomica tradizionali ci dicono quali molecole contengono le cellule, ma non dove queste cellule si trovano. Le tecnologie spaziali cambiano questo registrando sia il profilo molecolare di ogni piccolo punto in un tessuto sia le sue coordinate fisiche. Metodi diversi enfatizzano diversi strati molecolari: alcuni profilano l'RNA, altri le proteine, altri ancora i segni chimici sul DNA. Ogni livello rivela un aspetto differente dell'organizzazione tessutale. La sfida è che i ricercatori spesso si ritrovano con più fette parzialmente sovrapposte del tessuto misurate con strumenti diversi. Allineare queste fette eterogenee in uno spazio 3D coerente, senza perdere dettagli anatomici fini, è stato un problema importante e ancora in gran parte irrisolto.
Una visione dei tessuti consapevole della geometria
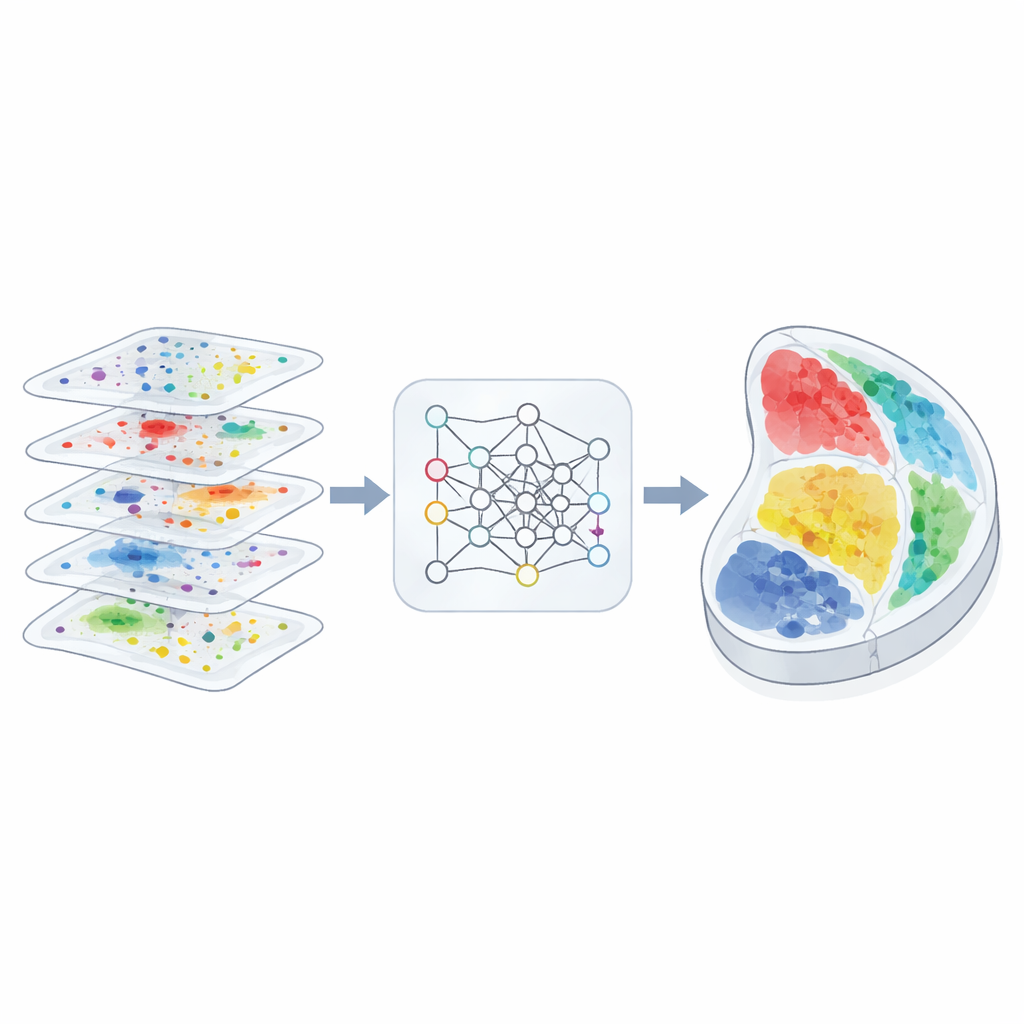
Gli autori hanno progettato 3d-OT per trattare ogni sezione tissutale come una “nuvola di punti”, una nuvola di spot nello spazio fisico, ciascuno con misurazioni multi-omiche. Invece di affidarsi principalmente a una griglia o a un grafo per descrivere le relazioni di vicinato, 3d-OT usa un'architettura di rete neurale chiamata PointNet++ originariamente creata per il riconoscimento di oggetti 3D. Questa rete fornisce ripetutamente a ogni spot non solo i suoi segnali molecolari ma anche le sue coordinate esatte, permettendo al modello di apprendere schemi geometrici sottili come strutture corticali stratificate o confini organici curvi. Per le sezioni con più di uno strato molecolare, un modulo di fusione combina le modalità in una rappresentazione condivisa mantenendo al contempo il contributo distintivo di ciascun livello.
Allineare le fette con corrispondenze morbide
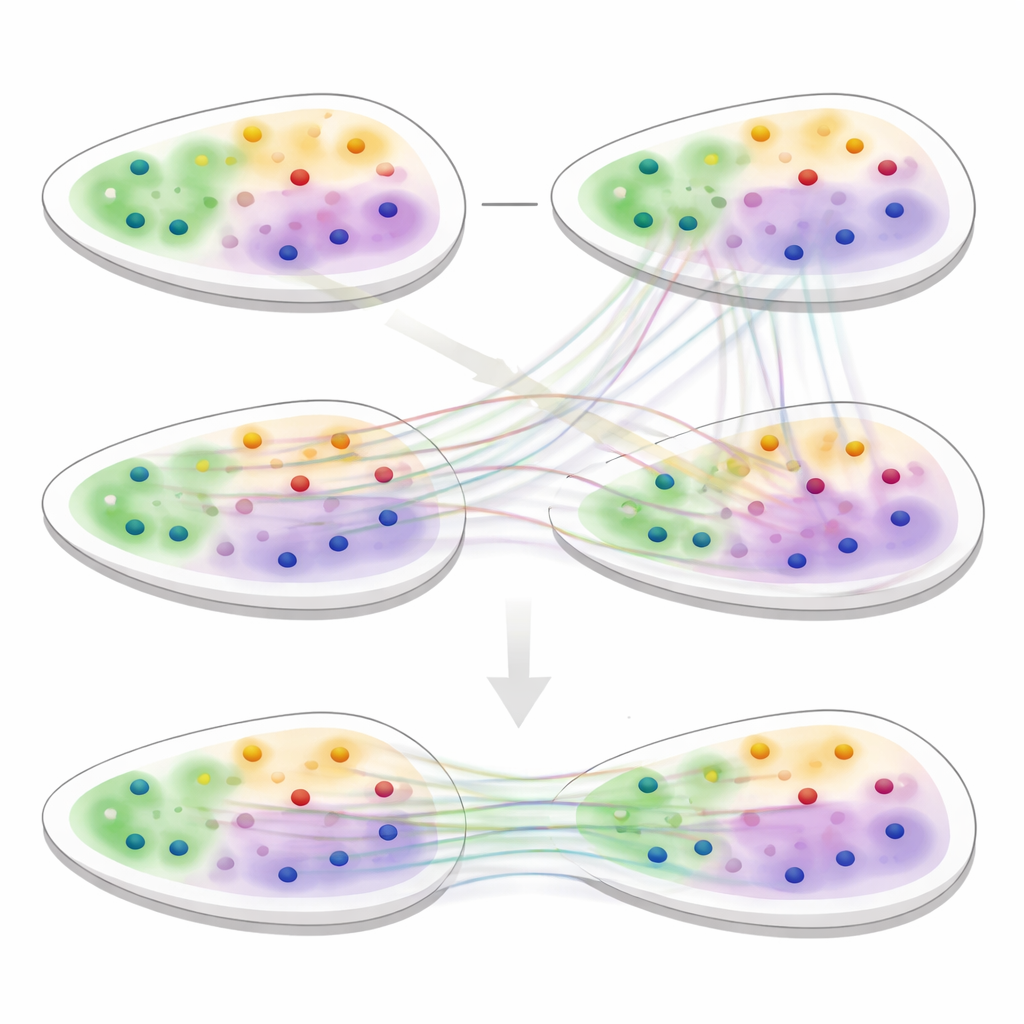
Il secondo nucleo di 3d-OT è un modulo di allineamento basato sul “trasporto ottimo”, un quadro matematico per mettere in corrispondenza due distribuzioni preservandone la forma complessiva. Invece di imporre un accoppiamento rigido uno-a-uno tra gli spot di due sezioni, il metodo calcola corrispondenze morbide: ogni spot in una sezione sorgente può corrispondere parzialmente a diversi candidati in una sezione target. Una perdita di ricostruzione basata sulla distanza di Chamfer premia gli allineamenti che rendono le posizioni ricostruite molto simili alle posizioni reali del target. Vincoli aggiuntivi di liscezza e di “zero divergenza” incoraggiano che il flusso di spot tra le sezioni segua deformazioni tissutali realistiche e continue, come piegature, stiramenti o crescita, invece di salti o torsioni implausibili.
Rivelare strutture tissutali nascoste
Per testare 3d-OT, il gruppo lo ha confrontato con i principali strumenti di analisi spaziale su una varietà di dataset, inclusi cervello umano, tumore al seno, linfonodo e diversi organi di topo. Nei compiti di clustering su singole sezioni, 3d-OT ha recuperato con maggiore accuratezza strati noti della corteccia umana e murina e ha distinto meglio le regioni tumorali rispetto ai metodi concorrenti. Nei dati multi-omici del cervello di topo che combinavano RNA e marcature della cromatina, ha separato due sotto-strati all'interno dello strato corticale più profondo che spesso appaiono come una singola banda, evidenziando geni marker per queste regioni fini. Attraverso molte tecnologie e risoluzioni, inclusi tessuti difficili come cuore e cresta neurale, 3d-OT ha fornito allineamenti più lisci e più fedeli anatomicamente rispetto ai metodi di allineamento esistenti.
Seguire gli organi nel tempo
Forse la dimostrazione più impressionante è venuta dalla ricostruzione dello sviluppo embrionale del topo. Utilizzando dati spaziali di diversi giorni embrionali, 3d-OT ha allineato le fette nel tempo per costruire “filmati” 3D della crescita degli organi. Ha catturato, ad esempio, come il cuore passa da una forma compatta a una struttura ad anello e ritorno, e come il fegato si espande in modo costante. Il metodo ha anche collegato regioni precursori precoci a organi successivi, tracciando correttamente la cresta urogenitale verso rene e ovaio, e il dermomiotomo verso muscolo e tessuto connettivo. Queste traiettorie corrispondevano alla biologia dello sviluppo nota, suggerendo al contempo ulteriori percorsi di differenziamento da studiare.
Cosa significa questo per la biologia futura
In termini semplici, 3d-OT trasforma istantanee sparse e multi-strato dei tessuti in mappe 3D coerenti e ad alta risoluzione che rispettano sia l'identità molecolare sia la forma fisica. Codificando esplicitamente la geometria e consentendo corrispondenze flessibili e morbide tra le sezioni, supera gli strumenti precedenti nell'identificare regioni tissutali fini e nell'allineare dati provenienti da tecnologie e tempi diversi. Con la crescita dei dataset di multi-omics spaziali, metodi come 3d-OT aiuteranno i ricercatori a passare da immagini piatte ad atlanti 3D dinamici di organi in salute, malattia e sviluppo.
Citazione: Dai, B., Yi, L., Wang, P. et al. 3d-OT: a deep geometry-aware framework for heterogeneous slices alignment of spatial multi-omics. Nat Methods 23, 760–771 (2026). https://doi.org/10.1038/s41592-026-03034-9
Parole chiave: omics spaziali, integrazione multi-omica, ricostruzione tissutale 3D, sviluppo embrionale, biologia computazionale