Clear Sky Science · es
3d-OT: un marco profundo consciente de la geometría para la alineación de cortes heterogéneos en multi-ómicas espaciales
Ver los tejidos en tres dimensiones
Los biólogos pueden cada vez más medir no solo qué moléculas están activas en una célula, sino también exactamente dónde se sitúa esa célula dentro de un tejido. Estos nuevos mapas “espaciales” prometen vistas más claras de cómo se conectan los cerebros, cómo se diseminan los tumores y cómo los embriones construyen órganos. Sin embargo, la mayoría de los experimentos aún capturan solo cortes delgados, cada uno usando distintos tipos de medida y resoluciones. Este artículo presenta 3d-OT, un método computacional que cose esos cortes en vistas 3D coherentes, aprovechando al máximo la rica información molecular de cada corte.
Por qué importa cartografiar el espacio
La genética y la genómica tradicionales nos dicen qué moléculas contienen las células, pero no dónde viven esas células. Las tecnologías espaciales cambian eso al registrar tanto el perfil molecular de cada pequeño punto en un tejido como sus coordenadas físicas. Diferentes métodos enfatizan distintas capas moleculares: algunos perfilan ARN, otros proteínas, otros las marcas químicas sobre el ADN. Cada capa revela un aspecto distinto de la organización tisular. El reto es que los investigadores a menudo acaban con múltiples cortes parciales y superpuestos medidos con herramientas diferentes. Alinear esos cortes heterogéneos en un espacio 3D consistente, sin perder el detalle anatómico fino, ha sido un problema difícil de resolver.
Una visión de los tejidos consciente de la geometría
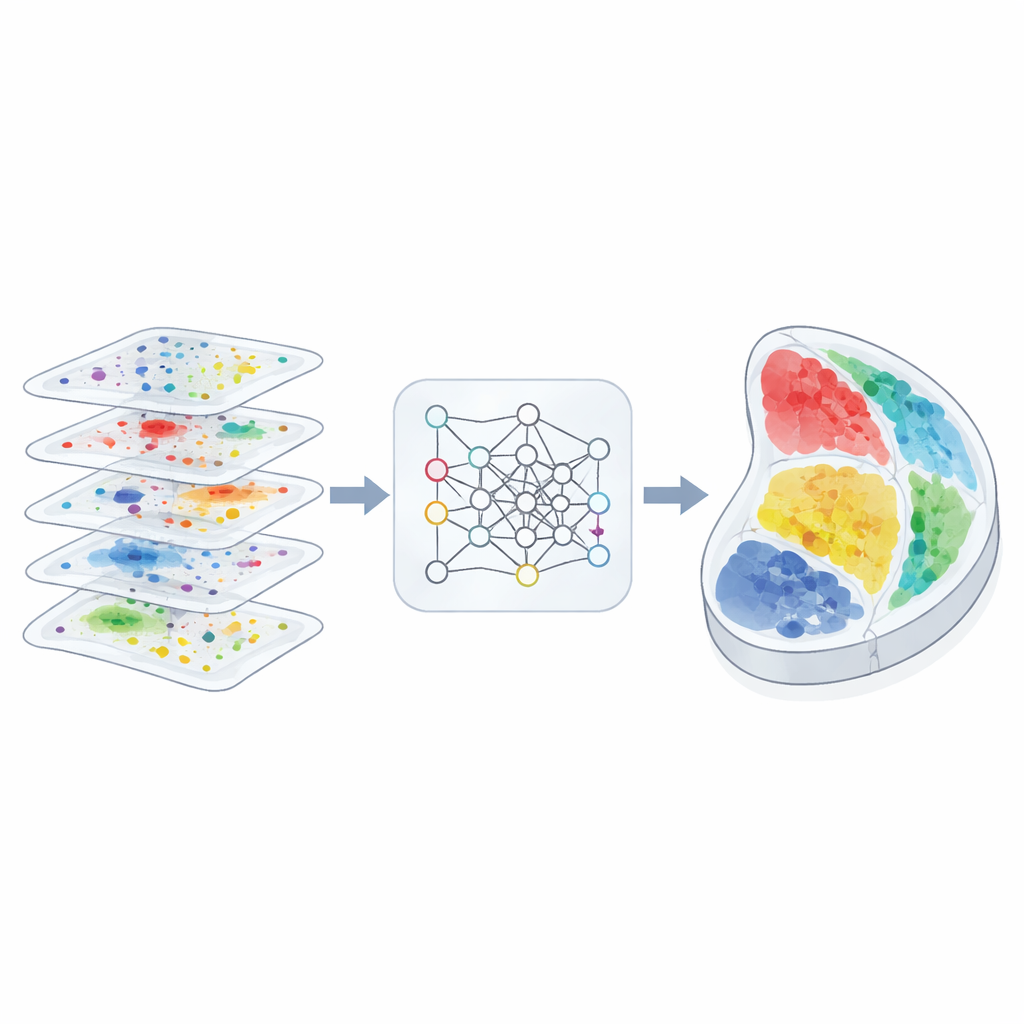
Los autores diseñaron 3d-OT para tratar cada corte de tejido como una “nube de puntos”, una nube de posiciones en el espacio físico, cada una con mediciones multi-ómicas. En lugar de confiar principalmente en una cuadrícula o grafo para describir relaciones de vecindad, 3d-OT usa una arquitectura de red neuronal llamada PointNet++ que se creó originalmente para el reconocimiento de objetos 3D. Esta red alimenta repetidamente a cada punto no solo con sus señales moleculares, sino también con sus coordenadas exactas, permitiendo al modelo aprender patrones geométricos sutiles como estructuras corticales en capas o límites orgánicos curvados. Para cortes con más de una capa molecular, un módulo de fusión combina las modalidades en una representación compartida manteniendo al mismo tiempo la contribución distintiva de cada capa.
Alineando cortes con correspondencias suaves
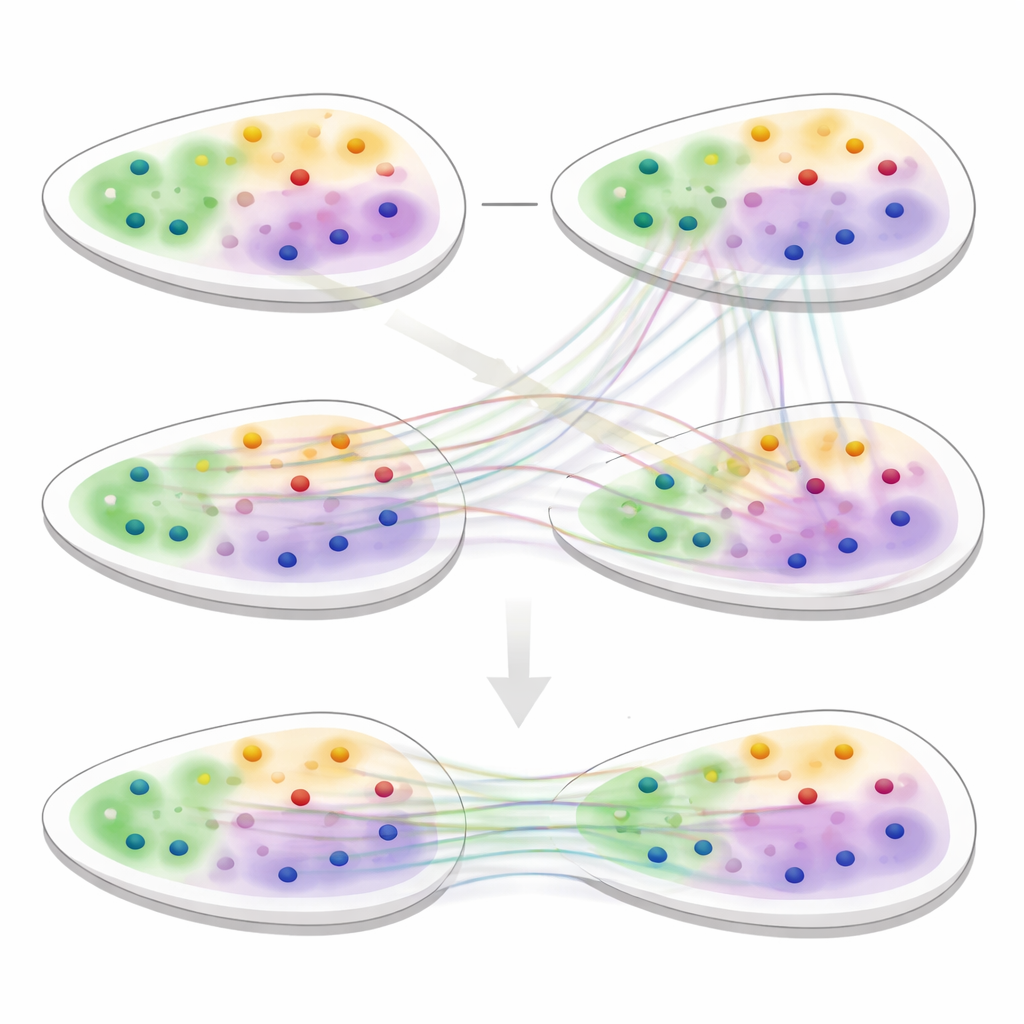
El segundo núcleo de 3d-OT es un módulo de alineación basado en el “transporte óptimo”, un marco matemático para emparejar dos distribuciones preservando su forma global. En lugar de forzar un emparejamiento rígido uno a uno entre puntos de dos cortes, el método calcula correspondencias suaves: cada punto en un corte origen puede corresponder parcialmente a varios candidatos en un corte destino. Una pérdida de reconstrucción basada en la distancia de Chamfer recompensa alineamientos que hacen que las posiciones reconstruidas se parezcan estrechamente a las posiciones reales del destino. Restricciones adicionales de suavidad y de “divergencia cero” fomentan que el flujo de puntos entre cortes siga deformaciones tisulares realistas y continuas, como flexión, estiramiento o crecimiento, en lugar de saltos o giros poco plausibles.
Revelando la estructura tisular oculta
Para evaluar 3d-OT, el equipo lo comparó con las principales herramientas de análisis espacial en una variedad de conjuntos de datos, que incluyeron cerebro humano, cáncer de mama, ganglio linfático y múltiples órganos de ratón. En tareas de agrupamiento de cortes individuales, 3d-OT recuperó con mayor precisión las capas conocidas de la corteza humana y de ratón y distinguió mejor las regiones cancerosas que los métodos competidores. En datos multi-ómicos del cerebro de ratón que combinaban ARN con marcas de cromatina, separó dos subcapas dentro de la capa cortical más profunda que a menudo aparecen como una banda única, y resaltó genes marcador para estas regiones finas. A través de múltiples tecnologías y resoluciones, incluidos tejidos difíciles como el corazón y la cresta neural, 3d-OT proporcionó alineamientos más suaves y anatómicamente fieles que los métodos de alineación existentes.
Siguiendo órganos a través del tiempo
Quizá la demostración más llamativa provino de la reconstrucción del desarrollo embrionario del ratón. Usando datos espaciales de varios días embrionarios, 3d-OT alineó cortes a lo largo del tiempo para construir “películas” 3D del crecimiento de órganos. Capturó, por ejemplo, cómo el corazón cambia de una forma compacta a una estructura en anillo y de nuevo, y cómo el hígado se expande de manera sostenida. El método también vinculó regiones precursoras tempranas con órganos posteriores, trazando correctamente la cresta urogenital hacia riñón y ovario, y el dermomiotomo hacia músculo y tejido conectivo. Estas trayectorias concordaron con la biología del desarrollo conocida, a la vez que sugirieron vías adicionales de diferenciación para estudiar.
Qué significa esto para la biología futura
En términos sencillos, 3d-OT convierte instantáneas dispersas y multilayer de tejidos en mapas 3D consistentes y de alta resolución que respetan tanto la identidad molecular como la forma física. Al codificar explícitamente la geometría y permitir correspondencias flexibles y suaves entre cortes, supera a herramientas anteriores en la identificación de regiones tisulares finas y en la alineación de datos de diferentes tecnologías y puntos temporales. A medida que crezcan los conjuntos de datos de multi-ómicas espaciales, métodos como 3d-OT ayudarán a los investigadores a pasar de imágenes planas a atlas 3D dinámicos de órganos en salud, enfermedad y desarrollo.
Cita: Dai, B., Yi, L., Wang, P. et al. 3d-OT: a deep geometry-aware framework for heterogeneous slices alignment of spatial multi-omics. Nat Methods 23, 760–771 (2026). https://doi.org/10.1038/s41592-026-03034-9
Palabras clave: omics espaciales, integración multi-ómica, reconstrucción 3D de tejidos, desarrollo embrionario, biología computacional