Clear Sky Science · de
3d-OT: ein tiefgehendes, geometrie-bewusstes Framework zur Ausrichtung heterogener Schnitte in räumlicher Multi-Omics
Gewebe in drei Dimensionen sehen
Biologinnen und Biologen können zunehmend nicht nur nachweisen, welche Moleküle in einer Zelle aktiv sind, sondern auch genau bestimmen, wo sich diese Zelle im Gewebe befindet. Diese neuen „räumlichen“ Karten versprechen klarere Einblicke darin, wie Gehirne verdrahtet sind, wie Tumoren sich ausbreiten und wie Embryonen Organe aufbauen. Die meisten Experimente erfassen jedoch noch immer nur dünne Schnitte, wobei jeder Schnitt unterschiedliche Messarten und Auflösungen verwendet. Dieser Artikel stellt 3d-OT vor, eine rechnerische Methode, die diese Schnitte zu kohärenten 3D-Ansichten verknüpft und dabei die reichen molekularen Informationen jedes Schnitts bestmöglich nutzt.
Warum räumliche Karten wichtig sind
Traditionelle Genetik und Genomik sagen uns, welche Moleküle Zellen enthalten, aber nicht, wo diese Zellen lokalisiert sind. Räumliche Technologien ändern das, indem sie sowohl das molekulare Profil jeder winzigen Stelle im Gewebe als auch deren physikalische Koordinaten aufzeichnen. Verschiedene Methoden legen den Fokus auf verschiedene molekulare Schichten: Einige erfassen RNA, andere Proteine, wieder andere die chemischen Markierungen auf der DNA. Jede Schicht offenbart eine andere Facette der Gewebeorganisation. Die Herausforderung besteht darin, dass Forschende häufig mehrere, teilweise überlappende Gewebeschnitte erhalten, die mit unterschiedlichen Werkzeugen gemessen wurden. Diese heterogenen Schnitte konsistent in einem 3D-Raum auszurichten, ohne feine anatomische Details zu verlieren, war lange ein ungelöstes Problem.
Ein geometrie-bewusster Blick auf Gewebe
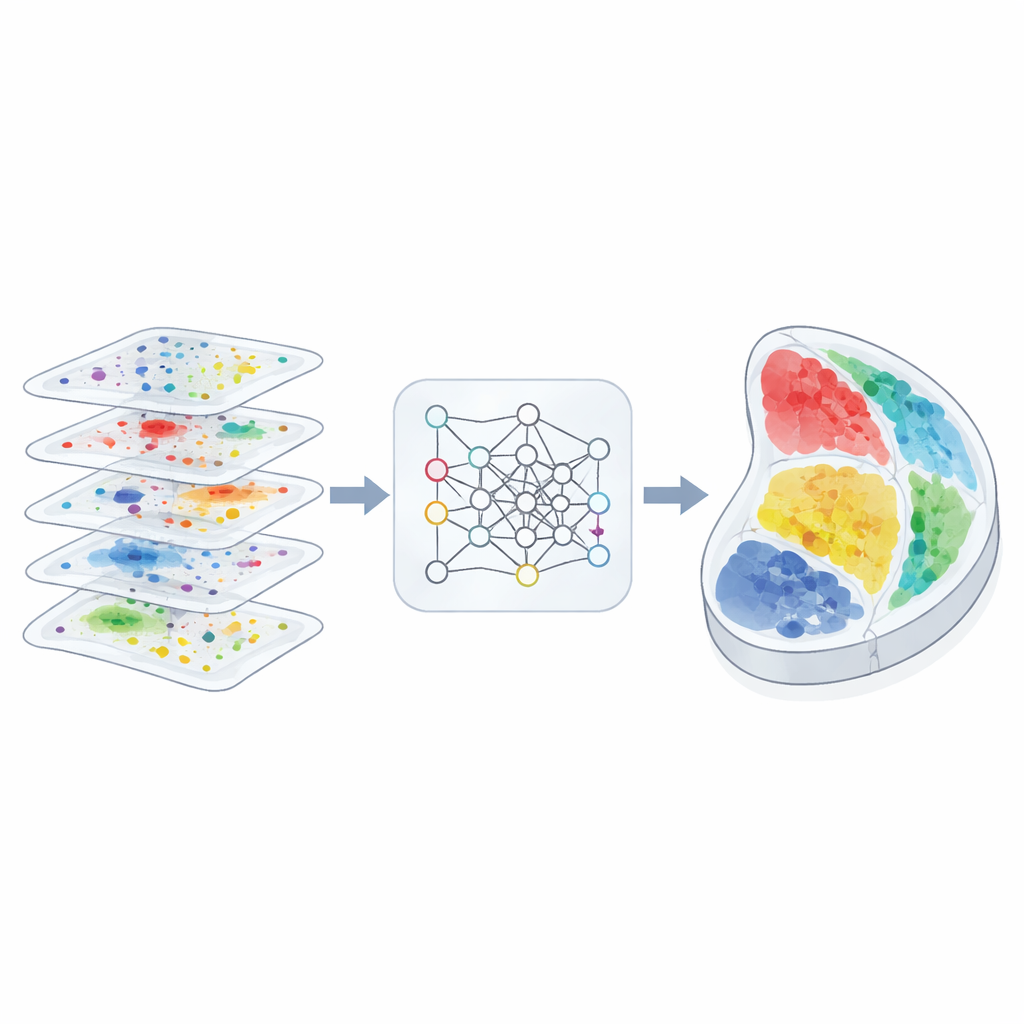
Die Autorinnen und Autoren haben 3d-OT so entworfen, dass jeder Gewebeschnitt als „Punktwolke“ behandelt wird — eine Wolke von Punkten im physischen Raum, von denen jeder Multi-Omics-Messungen trägt. Anstatt sich hauptsächlich auf ein Raster oder einen Graphen zur Beschreibung von Nachbarschaftsbeziehungen zu stützen, verwendet 3d-OT eine neuronale Netzwerkarchitektur namens PointNet++, die ursprünglich für die 3D-Objekterkennung entwickelt wurde. Dieses Netzwerk füttert wiederholt jedem Punkt nicht nur seine molekularen Signale, sondern auch seine exakten Koordinaten, sodass das Modell subtile geometrische Muster wie geschichtete Cortex-Strukturen oder gekrümmte Organränder erlernen kann. Bei Schnitten mit mehr als einer molekularen Schicht verbindet ein Fusionsmodul die Modalitäten zu einer gemeinsamen Repräsentation, während die spezifischen Beiträge jeder Schicht erhalten bleiben.
Schnitte mit weichen Zuordnungen ausrichten
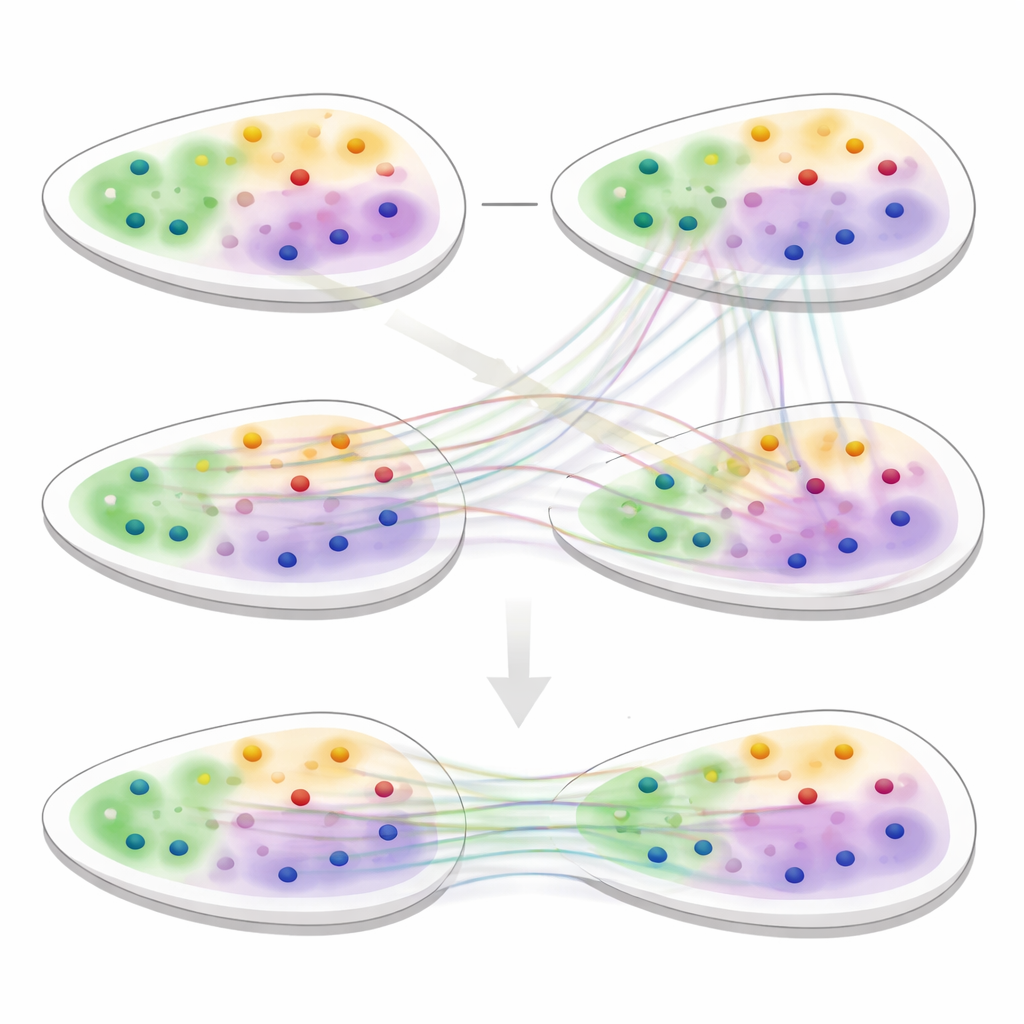
Der zweite Kern von 3d-OT ist ein Ausrichtungsmodul, das auf „optimalem Transport“ basiert — einem mathematischen Rahmen zur Anpassung zweier Verteilungen unter Erhalt ihrer Gesamtstruktur. Anstatt eine starre Eins-zu-eins-Zuordnung zwischen Punkten in zwei Schnitten zu erzwingen, berechnet die Methode weiche Korrespondenzen: Jeder Punkt in einem Quellschnitt kann sich teilweise mehreren Kandidaten in einem Zielschnitt zuordnen. Ein Rekonstruktionsverlust auf Basis der Chamfer-Distanz belohnt Ausrichtungen, die die rekonstruierten Positionen eng an die tatsächlichen Zielpositionen anlehnen. Zusätzliche Glattheits- und „Null-Divergenz“-Beschränkungen fördern, dass der Fluss der Punkte zwischen Schnitten realistische, kontinuierliche Gewebeverformungen wie Biegen, Dehnen oder Wachstum folgt, statt unplausibler Sprünge oder Verdrehungen.
Verborgene Gewebestrukturen offenlegen
Um 3d-OT zu testen, verglich das Team die Methode mit führenden Werkzeugen der räumlichen Analyse an einer Vielzahl von Datensätzen, darunter menschliches Gehirn, Brustkrebs, Lymphknoten und mehrere Mausorgane. Bei Einzelschnitt-Clustering-Aufgaben rekonstruierte 3d-OT bekannte Schichten des menschlichen und Maus-Cortex genauer und unterschied Krebsregionen besser als konkurrierende Methoden. In Multi-Omics-Daten des Mausgehirns, die RNA mit Chromatinmarken kombinierten, trennte es zwei Sublayer innerhalb der tiefsten kortikalen Schicht, die oft als ein einzelner Streifen erscheinen, und hob Marker-Gene für diese feinen Regionen hervor. Über verschiedene Technologien und Auflösungen hinweg, einschließlich herausfordernder Gewebe wie Herz und Neuralleiste, lieferte 3d-OT glattere und anatomisch treuere Ausrichtungen als bestehende Verfahren.
Organe im Laufe der Zeit verfolgen
Die wohl eindrücklichste Demonstration gelang bei der Rekonstruktion der Embryonalentwicklung von Mäusen. Mithilfe räumlicher Daten aus mehreren embryonalen Tagen richtete 3d-OT Schnitte über die Zeit aus, um 3D-„Filme“ des Organwachstums zu erstellen. Es erfasste beispielsweise, wie sich das Herz von einer kompakten Form zu einer ringähnlichen Struktur und wieder zurück verändert, und wie die Leber kontinuierlich expandiert. Die Methode verknüpfte außerdem frühe Vorläuferregionen mit späteren Organen, indem sie korrekt die urogenitale Leiste in Niere und Eierstock und das Dermomyotom in Muskel- und Bindegewebe zurückverfolgte. Diese Entwicklungsverläufe stimmten mit bekannter Entwicklungsbiologie überein und schlugen zugleich zusätzliche Differenzierungswege für weitergehende Untersuchungen vor.
Was das für die zukünftige Biologie bedeutet
Einfach ausgedrückt verwandelt 3d-OT verstreute, mehrschichtige Momentaufnahmen von Geweben in konsistente, hochauflösende 3D-Karten, die sowohl molekulare Identität als auch physische Form respektieren. Durch die explizite Kodierung von Geometrie und die Möglichkeit flexibler, weicher Zuordnungen zwischen Schnitten übertrifft es frühere Werkzeuge bei der Identifikation feiner Geweberegionen und der Ausrichtung von Daten aus verschiedenen Technologien und Zeitpunkten. Mit dem Wachstum räumlicher Multi-Omics-Datensätze werden Methoden wie 3d-OT Forschenden helfen, von flachen Bildern zu dynamischen 3D-Atlanten von Organen in Gesundheit, Krankheit und Entwicklung überzugehen.
Zitation: Dai, B., Yi, L., Wang, P. et al. 3d-OT: a deep geometry-aware framework for heterogeneous slices alignment of spatial multi-omics. Nat Methods 23, 760–771 (2026). https://doi.org/10.1038/s41592-026-03034-9
Schlüsselwörter: spatial omics, multi-omics Integration, Gewebe-3D-Rekonstruktion, Embryonalentwicklung, computational biology