Clear Sky Science · nl
3d-OT: een deep geometry-aware framework voor het uitlijnen van heterogene plakjes bij ruimtelijke multi-omics
Weefsels in drie dimensies zien
Biologen kunnen steeds beter vaststellen niet alleen welke moleculen in een cel actief zijn, maar ook precies waar die cel zich in een weefsel bevindt. Deze nieuwe “ruimtelijke” kaarten beloven helderdere inzichten in hoe hersenen zijn bekabeld, hoe tumoren zich verspreiden en hoe embryo’s organen opbouwen. Toch leggen de meeste experimenten nog steeds alleen dunne plakjes vast, elk met verschillende meettypen en resoluties. Dit artikel introduceert 3d-OT, een computationele methode die die plakjes tot consistente 3D-weergaven naait, terwijl ze optimaal gebruikmaakt van de rijke moleculaire informatie in elk plakje.
Waarom het in kaart brengen van ruimte ertoe doet
Traditionele genetica en genomica vertellen ons welke moleculen cellen bevatten, maar niet waar die cellen zich bevinden. Ruimtelijke technologieën veranderen dat door zowel het moleculaire profiel van elk klein punt in een weefsel als diens fysieke coördinaten vast te leggen. Verschillende methoden leggen de nadruk op verschillende moleculaire lagen: sommige bepalen RNA, andere eiwitten, weer andere chemische markeringen op DNA. Elke laag onthult een andere kant van weefselorganisatie. De uitdaging is dat onderzoekers vaak meerdere, deels overlappende plakjes krijgen die met verschillende instrumenten zijn gemeten. Het uitlijnen van die heterogene plakjes in een consistente 3D-ruimte, zonder fijne anatomische details te verliezen, is een groot onopgelost probleem geweest.
Een geometrie-bewuste kijk op weefsels
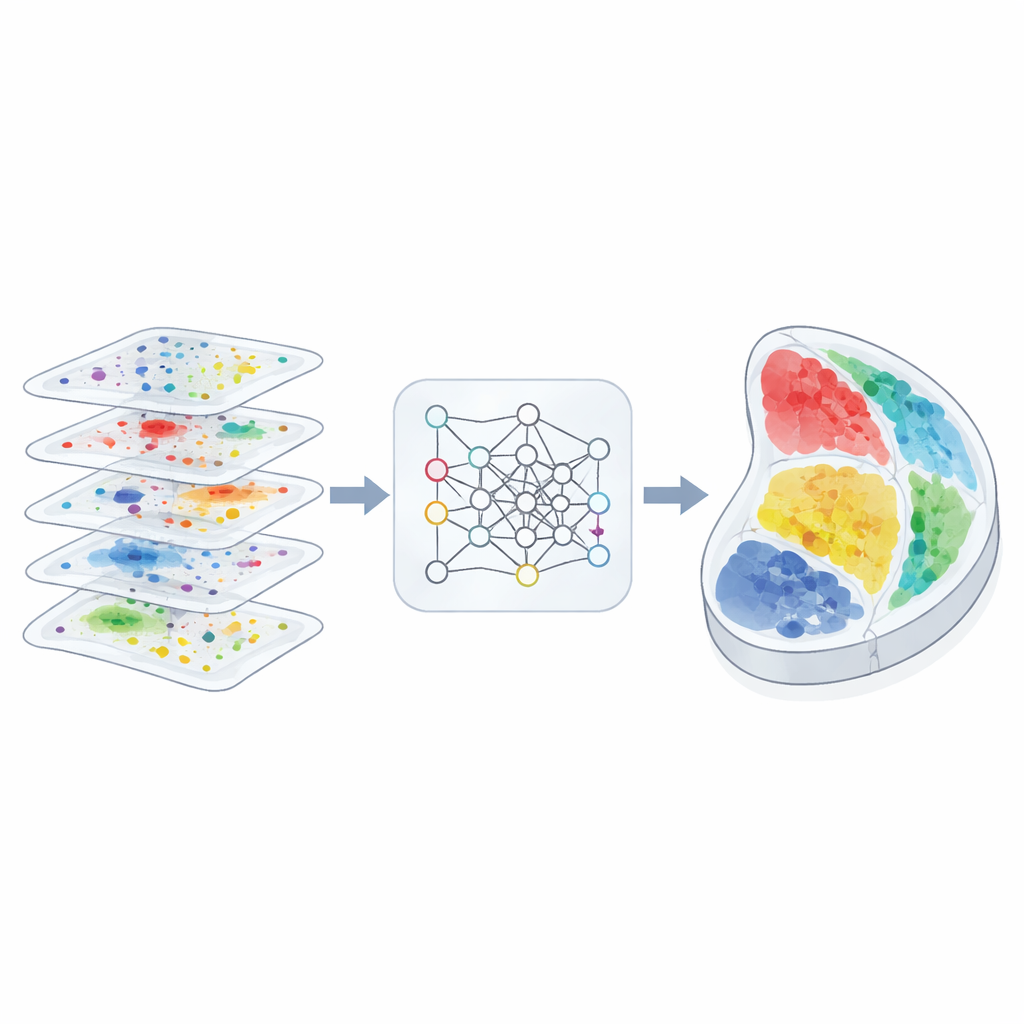
De auteurs ontwierpen 3d-OT om elk weefselplakje te behandelen als een “point cloud”, een wolk van punten in de fysieke ruimte, elk met multi-omicsmetingen. In plaats van zich hoofdzakelijk op een raster of graaf te baseren om buurtrelaties te beschrijven, gebruikt 3d-OT een neurale netwerkarchitectuur genaamd PointNet++ die oorspronkelijk is ontwikkeld voor 3D-voorwerpherkenning. Dit netwerk voedt elk punt herhaaldelijk niet alleen met zijn moleculaire signalen maar ook met zijn exacte coördinaten, waardoor het model subtiele geometrische patronen kan leren, zoals gelaagde cortexstructuren of gebogen orgaangrenzen. Voor plakjes met meer dan één moleculaire laag mengt een fusie-module de modaliteiten tot een gedeelde representatie, terwijl de onderscheidende bijdrage van elke laag behouden blijft.
Plakjes uitlijnen met zachte matches
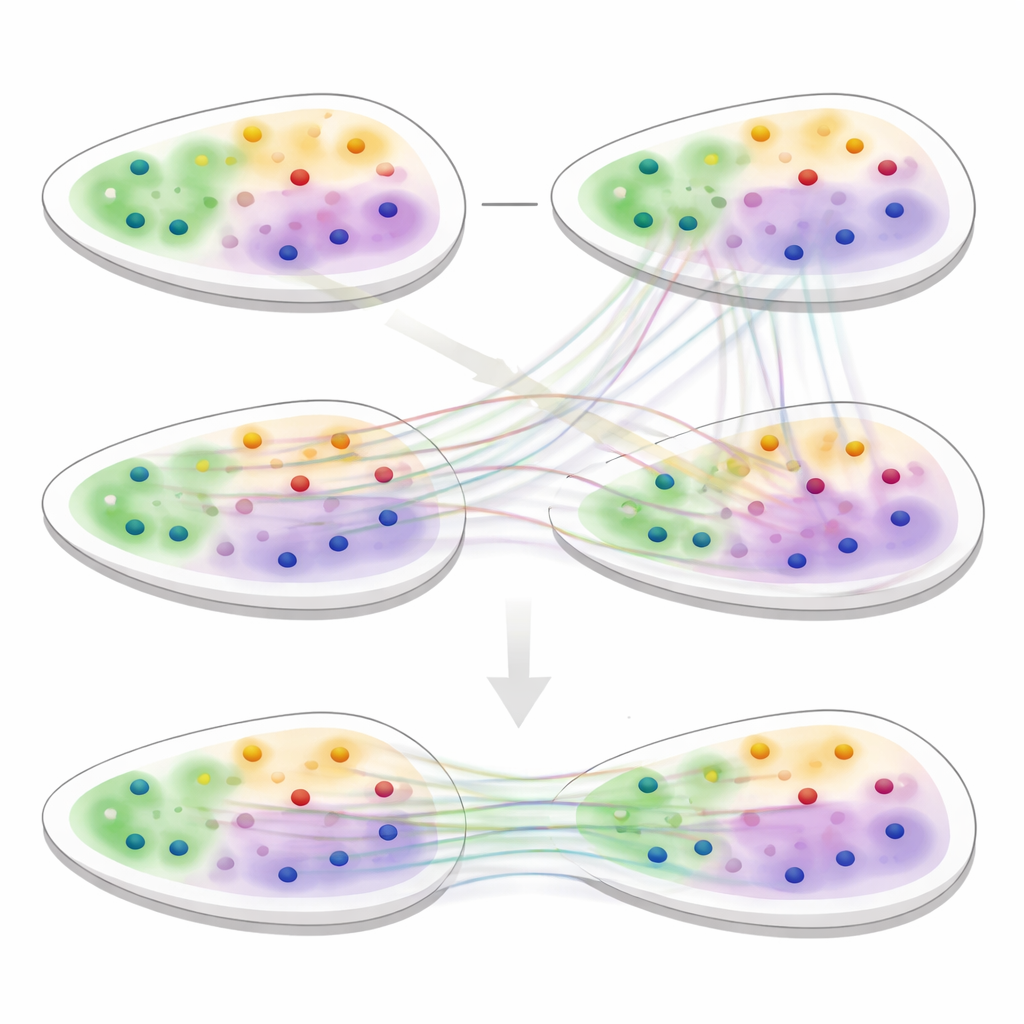
De tweede kern van 3d-OT is een uitlijningsmodule gebaseerd op “optimal transport”, een wiskundig kader om twee distributies op elkaar af te stemmen terwijl hun algemene vorm behouden blijft. In plaats van te dwingen tot een rigide één-op-één koppeling tussen punten in twee plakjes, berekent de methode zachte correspondenties: elk punt in een bronplakje kan gedeeltelijk overeenkomen met meerdere kandidaten in een doelplakje. Een reconstructieverlies gebaseerd op chamfer-afstand beloont uitlijningen die de gereconstrueerde posities dicht bij de werkelijke doelposities laat liggen. Extra soepelheids- en “nul-divergentie”-constraints stimuleren dat de verplaatsing van punten tussen plakjes realistische, continue weefseldeformaties volgt, zoals buigen, uitrekken of groei, in plaats van onwaarschijnlijke sprongen of draaigingen.
Verborgen weefselstructuur onthullen
Om 3d-OT te testen vergeleek het team het met toonaangevende ruimtelijke analysetools op verschillende datasets, inclusief menselijk brein, borstkanker, lymfeknoop en meerdere muisorganen. Bij clustertaken binnen enkele plakjes herstelde 3d-OT bekende lagen van de menselijke en muiscortex nauwkeuriger en onderscheidde het kankergebieden beter dan concurrerende methoden. In multi-omics muizenbreindata die RNA combineerden met chromatinemarkeringen, scheidde het twee sublagen binnen de diepste corticale laag die vaak als één band verschijnen, en benadrukte marker-genen voor deze fijne regio’s. Over meerdere technologieën en resoluties, inclusief uitdagende hart- en neurale-kamweefsels, leverde 3d-OT vloeiendere en anatomisch getrouwere uitlijningen dan bestaande methoden.
Organen volgen door de tijd
Misschien wel de meest opvallende demonstratie kwam uit het reconstrueren van muisembryo-ontwikkeling. Met ruimtelijke data van meerdere embryonale dagen leidde 3d-OT plakjes over de tijd uit om 3D-“films” van orgaangroei te bouwen. Het ving bijvoorbeeld hoe het hart verandert van een compacte vorm naar een ringachtige structuur en weer terug, en hoe de lever gestaag groeit. De methode koppelde ook vroege precursorregio’s aan latere organen, waarbij de urogenitale richel correct werd gevolgd naar nier en eierstok, en de dermomyotoom naar spier en bindweefsel. Deze trajecten kwamen overeen met bekende ontwikkelingsbiologie en suggereerden tegelijk aanvullende differentiatiepaden voor vervolgonderzoek.
Wat dit betekent voor toekomstige biologie
In eenvoudige bewoordingen verandert 3d-OT verspreide, meerlagige momentopnames van weefsels in consistente, hoge-resolutie 3D-kaarten die zowel moleculaire identiteit als fysieke vorm respecteren. Door geometrie expliciet te coderen en flexibele, zachte matches tussen plakjes toe te staan, presteert het beter dan eerdere tools bij het identificeren van fijne weefselregio’s en het uitlijnen van data van verschillende technologieën en tijdstippen. Naarmate ruimtelijke multi-omicsdatasets groeien, zullen methoden zoals 3d-OT onderzoekers helpen te verschuiven van platte beelden naar dynamische 3D-atlassen van organen in gezondheid, ziekte en ontwikkeling.
Bronvermelding: Dai, B., Yi, L., Wang, P. et al. 3d-OT: a deep geometry-aware framework for heterogeneous slices alignment of spatial multi-omics. Nat Methods 23, 760–771 (2026). https://doi.org/10.1038/s41592-026-03034-9
Trefwoorden: spatial omics, multi-omics integratie, 3D-weergave van weefsel, embryonale ontwikkeling, computationele biologie