Clear Sky Science · zh
通过指纹区单键振动模式的超光谱中红外检测区分鞘磷脂和胆固醇
为什么细胞中的脂肪很重要
脂肪,或称脂质,不仅仅是储存的热量。它们构建细胞膜、引导化学信号,并与癌症、心脏病、肥胖和神经系统疾病等状况紧密相关。然而,在活细胞中观察特定类型的脂质一直出乎意料地困难,通常需要使用可能干扰科学家想要观察的过程的荧光染料。本研究提出了一种在不使用任何标记的情况下观察并区分活细胞中关键脂质的方法,打开了一扇实时观察这些分子如何行为的窗口。
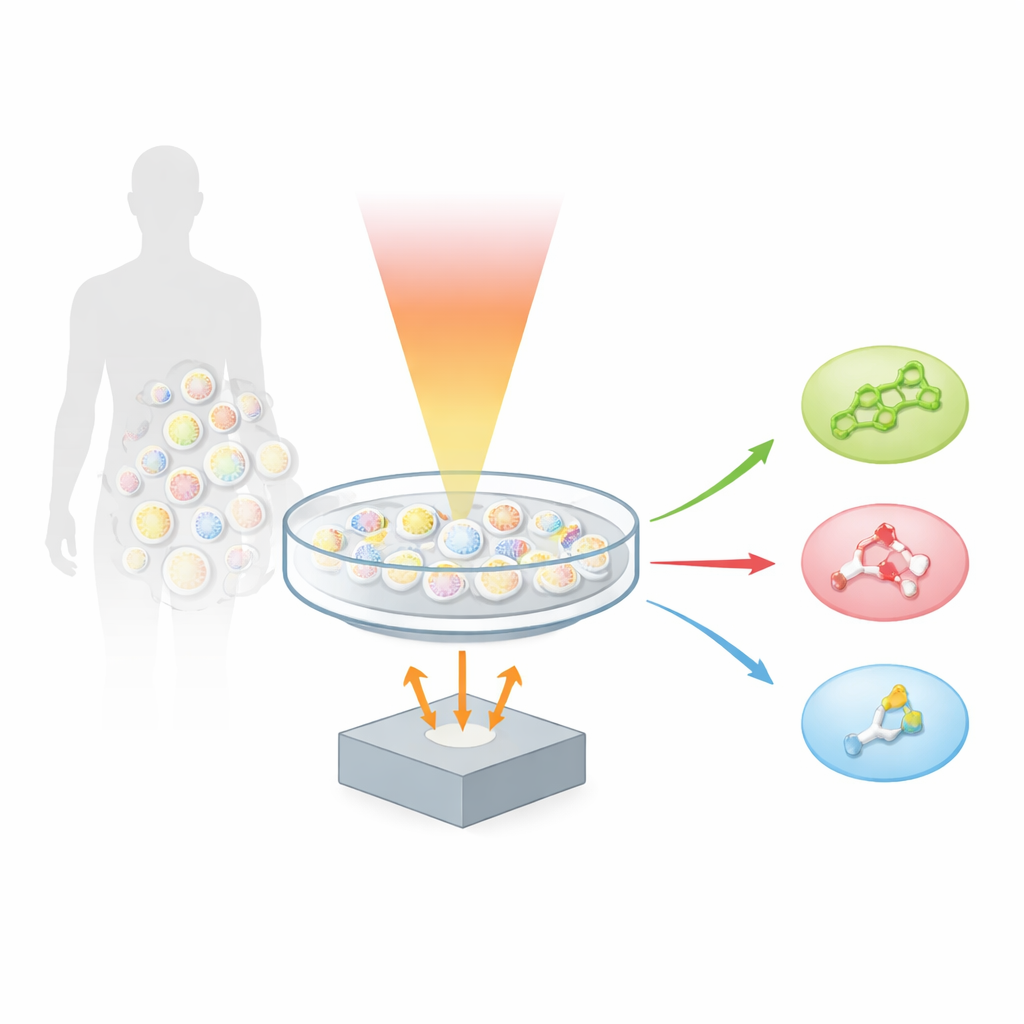
一种聆听分子的全新方式
作者基于一种称为光声学的技术,该技术将光转为声音。当分子吸收一短脉冲的红外光时,会产生微小的加热和热膨胀,进而产生极其微弱的超声波。通过用多种中红外波长扫描样品并记录产生的声波,团队创建了“超光谱指纹光声显微术”(hyperspectral fingerprint optoacoustic microscopy,简称 hyFOPM)。每种脂质在所谓的指纹区(约在1730到900 cm^-1之间)的照明下会以特征性的方式振动,这些振动像条形码一样,使系统能够将胆固醇与鞘磷脂以及一种常见膜脂磷脂酰胆碱区分开来,尽管这些分子共同存在于同一细胞膜中。
在简化样品上测试该方法
为了解 hyFOPM 能多清晰地分辨脂质,研究人员首先在受控样品上进行了测试。他们制备了包含纯胆固醇、鞘磷脂、磷脂酰胆碱和水的小孔,并在宽广的碳—氢伸缩区和更精细的指纹区对其进行扫描。通过对记录到的光谱进行数学解混,研究表明指纹区包含更丰富的信息。在该区域,胆固醇产生与其刚性环结构相关的强信号,而鞘磷脂因其酰胺键显示出独特特征,磷脂酰胆碱则呈现来自其酯基的明显指纹。统计分析证实,这些光谱指纹使三种脂质可以以约96–97%的准确率被分类,且仅指纹区即可提供最干净的分离和最少的物种间串扰。
从模型膜到更真实的细胞表面
真实细胞膜比纯脂质孔要复杂得多,因此团队接着研究了巨型单层囊泡(GUVs)——由选定脂质混合物组成的细胞大小气泡。他们组装了三类 GUV:一种仅由鞘磷脂和胆固醇密集组成;一种模拟典型细胞膜的混合、斑块状特性;以及一种仅由流体磷脂酰胆碱构成。HyFOPM 图像清晰显示了这些囊泡,并表明紧密包装的膜产生比松散膜更强的信号。通过将囊泡的光谱与纯脂质的光谱进行比较并解混贡献,研究人员能够还原每个囊泡的实际脂质组成,甚至检测到高达约40%的批次间差异。这意味着该技术也可作为生物物理学和药物研究中常用膜模型的质量控制工具。
在活细胞内观察与疾病相关脂质的变化
真正的考验是 hyFOPM 是否能在活细胞内追踪特定脂质对处理的反应。在暴露于一种已知会提升鞘磷脂的实验性抗肿瘤化合物的肺癌细胞中,该方法测得与该脂质相关的光谱特征在72小时内上升了超过两倍,而对照细胞仅显示出温和的漂移。在第二项实验中,载体分子输送的胆固醇注入人肾细胞。HyFOPM 检测到与胆固醇相关信号的急剧增加以及鞘磷脂的轻微下降,这与已知该处理对细胞膜的影响一致。关键是,这些测量仅使用了少数精心挑选的红外波段,暗示未来的系统可通过仅采样最具信息量的谱段来实现更快成像。
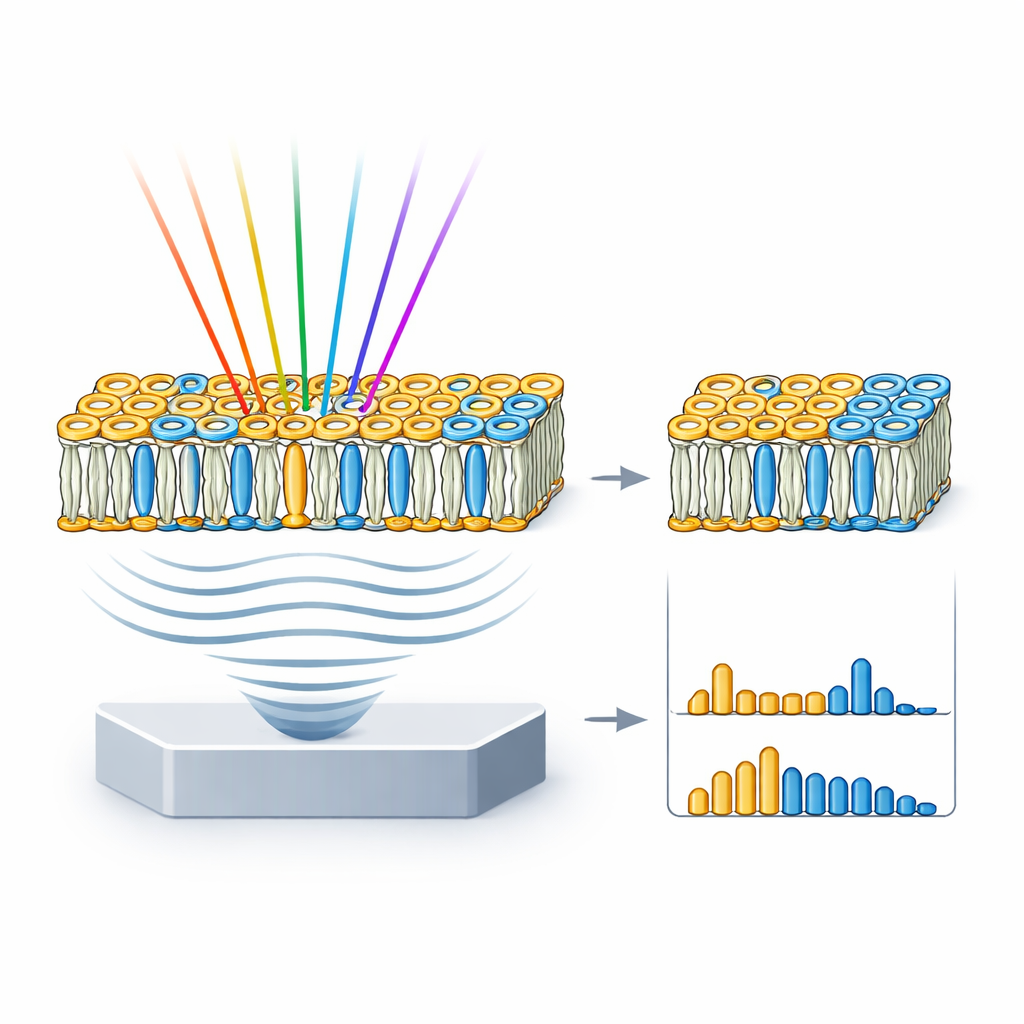
这对健康与疾病意味着什么
通过在活细胞中提供无标记、具有化学特异性的脂质图谱,hyFOPM 避开了荧光染色和基因标签的许多缺点。研究者现在可以直接从振动指纹中区分主要脂类(如胆固醇和鞘磷脂),跟踪它们在药物处理期间如何积累或消失,并评估模型膜的真实组成。由于中红外光声信号可在比传统显微镜更大的深度被检测到,该方法的未来版本可能对组织甚至患者中的脂质失衡进行成像。这最终可能有助于诊断和监测由细胞内脂肪隐秘舞动部分驱动的疾病——从动脉粥样硬化到神经退行性疾病。}
引用: Gasparin, F., Prebeck, A., Soldà, A. et al. Differentiation of sphingomyelin and cholesterol by hyperspectral mid-infrared detection of single-bond vibrational modes in the fingerprint region. Nat Methods 23, 815–822 (2026). https://doi.org/10.1038/s41592-026-03025-w
关键词: 脂质成像, 胆固醇, 鞘磷脂, 光声显微术, 中红外光谱