Clear Sky Science · ar
تمييز السفينغوميلين والكوليسترول عبر كشف تحت أحمر متوسط الطيف فائق الطيف لأوضاع اهتزاز الروابط الأحادية في منطقة البصمة
لماذا تهم الدهون داخل خلايانا
الدهون، أو الليبيدات، ليست مجرد سعرات مخزنة. إنها تساهم في بناء أغشية الخلايا، وتوجه الإشارات الكيميائية وترتبط ارتباطًا وثيقًا بحالات مثل السرطان وأمراض القلب والسمنة والاضطرابات العصبية. ومع ذلك كان من الصعب بشكل مدهش مراقبة أنواع محددة من الليبيدات داخل الخلايا الحية، وغالبًا ما تطلب ذلك صبغات فلورية قد تُعطّل العمليات التي يرغب العلماء في ملاحظتها. تقدم هذه الدراسة طريقة لرؤية وتمييز ليبيدات رئيسية داخل الخلايا الحية بدون أي وسم، ما يفتح نافذة لرصد سلوك هذه الجزيئات في الزمن الحقيقي.
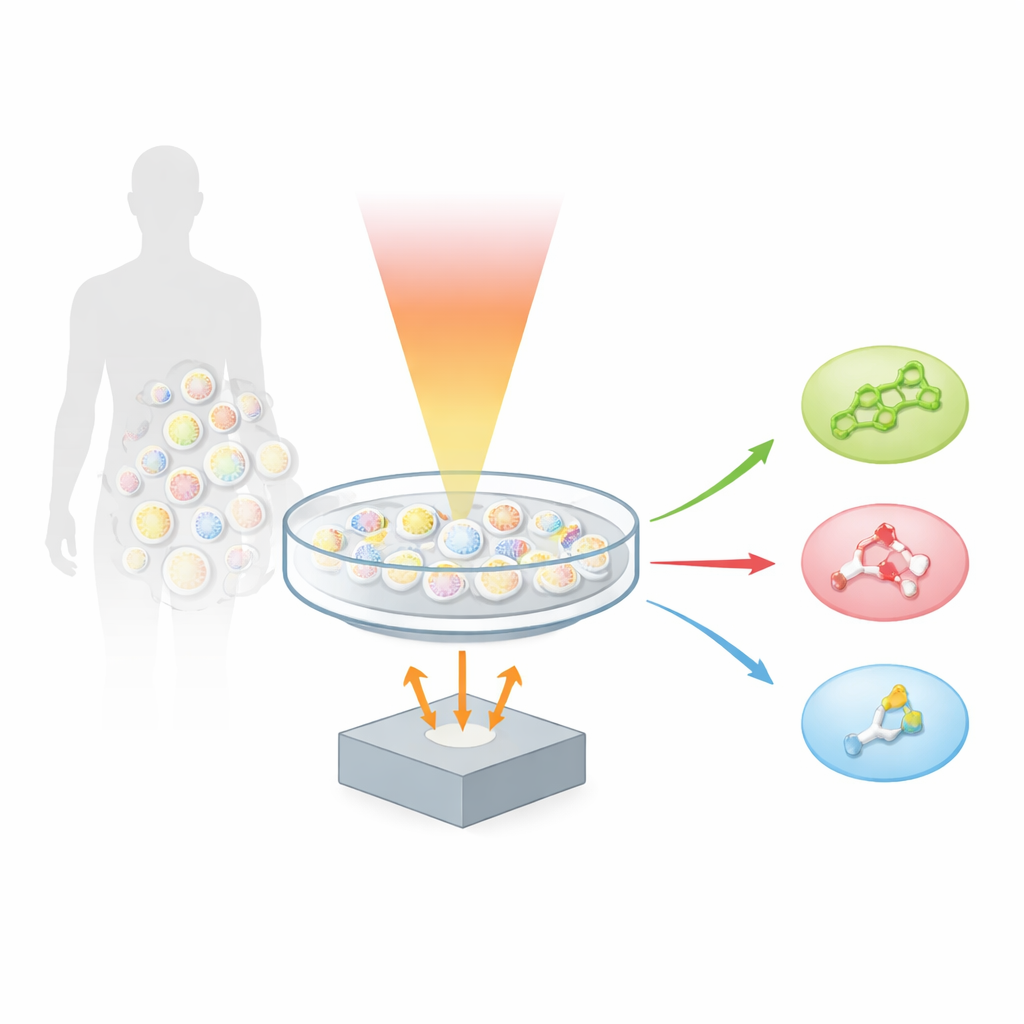
طريقة جديدة «للاستماع» إلى الجزيئات
يعتمد المؤلفون على تقنية تُدعى الضوئي الصوتي (optoacoustics)، التي تحول الضوء إلى صوت. عندما يمتص جزيء نبضة قصيرة من الضوء تحت الأحمر، يسخن ويتمدد قليلًا جدًا، مولّدًا موجة فوق صوتية دقيقة. من خلال مسح العينة بألوان عديدة من الضوء تحت الأحمر المتوسط وتسجيل الصوت الناتج، أنشأ الفريق «المجهر الضوئي الصوتي فائق الطيف لمنطقة البصمة»، أو hyFOPM. كل نوع من الليبيدات يهتز بطريقة مميزة عند تسليطه في ما يُسمى بمنطقة البصمة من طيف الأشعة تحت الحمراء، تقريبًا بين 1730 و900 سنتيمتر عكسي. تعمل هذه الاهتزازات كرموز شريطية تُمكّن النظام من تمييز الكوليسترول عن السفينغوميلين وعن ليبيد غشائي شائع يسمى فوسفاتيديلكولين، رغم تواجد هذه الجزيئات معًا في نفس غشاء الخلية.
اختبار الطريقة على عينات مبسطة
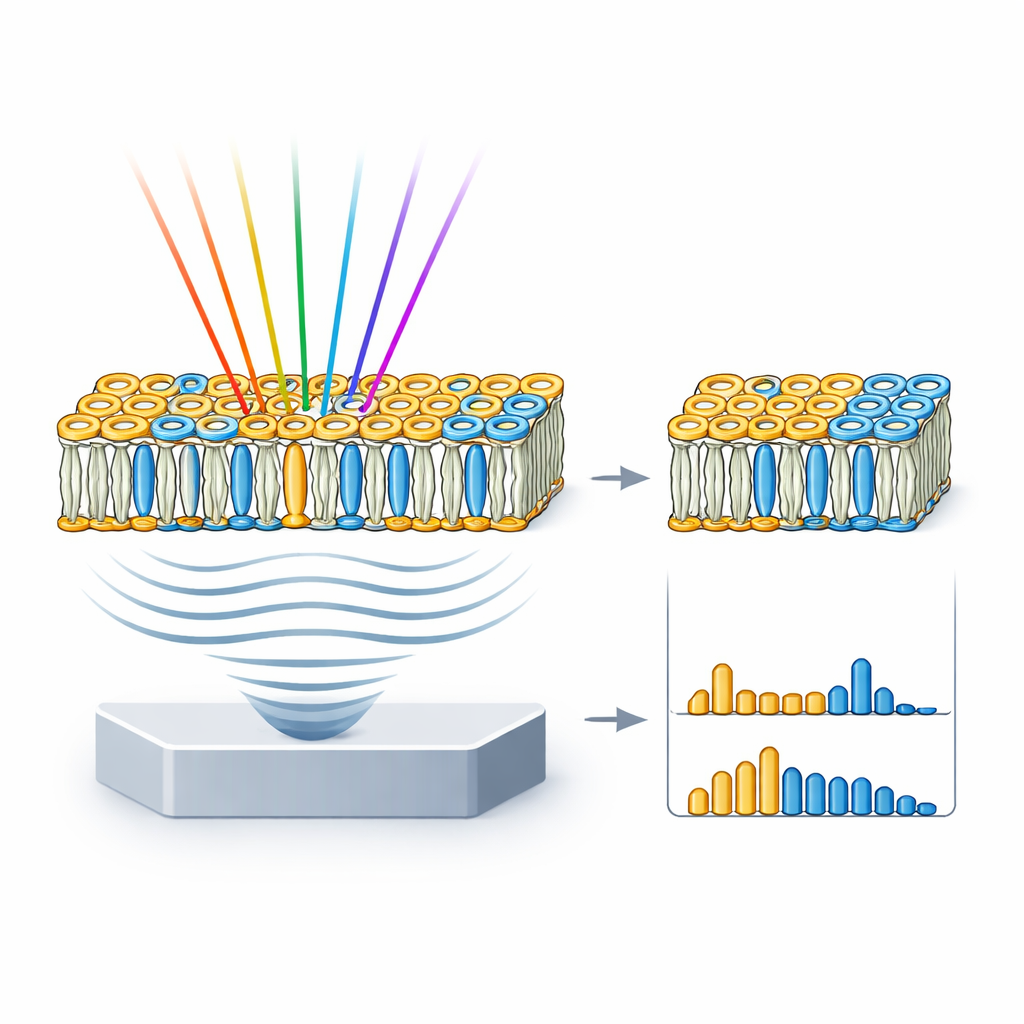
لاستقصاء مدى قدرة hyFOPM على فصل الليبيدات بوضوح، اختبرها الباحثون أولًا على عينات مُتحكم بها. حضّروا آبارًا صغيرة تحتوي على كوليسترول نقي، وسفينغوميلين، وفوسفاتيديلكولين وماء، وُمسحت عبر كل من نطاق استطالة الكربون–الهيدروجين العريض والمنطقة التفصيلية الأخص «منطقة البصمة». عبر فك الخلط الطيفي رياضيًا للطيف المسجّل، أظهروا أن منطقة البصمة تحتوي على معلومات أغنى بكثير. هناك أعطى الكوليسترول إشارات قوية مرتبطة ببنيته الحلقية الصلبة، في حين عرض السفينغوميلين ميزات مميزة من روابط الأميد، وكشف الفوسفاتيديلكولين توقيعًا واضحًا من مجموعات الإستر. أكدت التحليلات الإحصائية أن هذه بصمات طيفية تسمح بتصنيف الليبيدات الثلاثة بدقة تقارب 96–97%، مع أن منطقة البصمة وحدها قدمت الفصل الأنظف وأدنى تداخل بين الأنواع.
من أغشية نموذجية إلى أسطح خلوية واقعية
أغشية الخلايا الحقيقية أعقد من آبار الليبيدات النقية، لذا اتجه الفريق بعد ذلك إلى الحويصلات أحادية الطبقة كبيرة الحجم (GUVs) — فقاعات بحجم الخلايا مصنوعة من خلائط ليبيدية مختارة. جمعوا ثلاثة أنواع من GUVs: نوع مكتظ بالسفينغوميلين والكوليسترول فقط؛ ونوع يحاكي الطبيعة المختلطة والمرقطة لغشاء خلية نموذجي؛ ونوع مصنوع فقط من فوسفاتيديلكولين سائل. كشفت صور hyFOPM هذه الحويصلات بوضوح وأظهرت أن الأغشية المكتظة أنتجت إشارات أقوى من الأغشية الأقل إحكامًا. بمقارنة طيف الحويصلات مع طيف الليبيدات النقية وفك خلط المساهمات، استطاع الباحثون استعادة التركيب الليبيدي الفعلي لكل حويصلة وحتى كشف تباين بين الدفعات يصل إلى حوالي 40%. وهذا يعني أن التقنية يمكن أن تعمل أيضًا كأداة مراقبة جودة لنماذج الأغشية المستخدمة كثيرًا في الفيزياء الحيوية وبحوث الأدوية.
مراقبة تغيّر الليبيدات المرتبطة بالأمراض داخل الخلايا الحية
الاختبار الحقيقي كان ما إذا كان بإمكان hyFOPM تتبع ليبيدات محددة داخل خلايا حية أثناء استجابتها للعلاجات. في خلايا سرطان الرئة المعرضة لمركب تجريبي مضاد للأورام معروف بزيادة السفينغوميلين، قاست الطريقة زيادة أكثر من ضعفين في الميزة الطيفية المرتبطة بذلك الليبيد على مدى 72 ساعة، بينما أظهرت الخلايا الضابطة انحرافًا طفيفًا فقط. في تجربة ثانية، غمرت خلايا كلوية بشرية بالكوليسترول الموصل بواسطة جزيئات حاملة. اكتشف hyFOPM زيادة حادة في الإشارات المرتبطة بالكوليسترول وانخفاضًا طفيفًا في السفينغوميلين، متوافقًا مع التأثيرات المعروفة لهذه المعالجة على أغشية الخلايا. والأهم من ذلك أن هذه القياسات تحققت باستخدام مجرد مجموعة مختارة بعناية من ألوان تحت الحمراء، مما يشير إلى أن الأنظمة المستقبلية يمكن أن تُسارع عبر أخذ عينات فقط من النطاقات الطيفية الأكثر إفادة.
ما يعنيه هذا للصحة والمرض
من خلال توفير خرائط كيميائية محددة للليبيدات في الخلايا الحية بدون وسم، يتجاوز hyFOPM العديد من عيوب الصبغات الفلورية والوسوم الجينية. يمكن للباحثين الآن تمييز فئات ليبيدية رئيسية مثل الكوليسترول والسفينغوميلين مباشرة من بصماتها الاهتزازية، ومتابعة كيفية تراكمها أو اختفائها أثناء العلاجات الدوائية، وتقييم التركيب الحقيقي لأغشية النماذج. وبما أن الإشارات الضوئية الصوتية في نطاق تحت الأحمر المتوسط يمكن اكتشافها على أعماق أكبر مما تسمح به المجاهر التقليدية، فقد تُصوّر الإصدارات المستقبلية اختلالات الليبيدات في الأنسجة وحتى في المرضى. وقد يساعد ذلك في نهاية المطاف على تشخيص ومراقبة أمراض — من تصلب الشرايين إلى التنكس العصبي — التي تقودها جزئيًا الرقصة الخفية للدهون داخل خلايانا.
الاستشهاد: Gasparin, F., Prebeck, A., Soldà, A. et al. Differentiation of sphingomyelin and cholesterol by hyperspectral mid-infrared detection of single-bond vibrational modes in the fingerprint region. Nat Methods 23, 815–822 (2026). https://doi.org/10.1038/s41592-026-03025-w
الكلمات المفتاحية: تصوير الدهون, الكوليسترول, السفينغوميلين, المجهر الضوئي الصوتي, مطيافية تحت الحمراء المتوسطة