Clear Sky Science · de
Differenzierung von Sphingomyelin und Cholesterin durch hyperspektrale mittel‑infrarote Detektion von Einfachbindungs‑Schwingungsmoden im Fingerprint‑Bereich
Warum die Fette in unseren Zellen wichtig sind
Fette, oder Lipide, sind mehr als bloß gespeicherte Kalorien. Sie bauen Zellmembranen mit auf, steuern chemische Signale und stehen in engem Zusammenhang mit Erkrankungen wie Krebs, Herzkrankheiten, Adipositas und neurologischen Störungen. Dennoch war es überraschend schwierig, bestimmte Lipidarten in lebenden Zellen zu beobachten – das erforderte oft fluoreszierende Farbstoffe, die genau die Prozesse stören können, die Forschende untersuchen wollen. Diese Studie stellt eine Methode vor, wichtige Lipide in lebenden Zellen ohne jegliche Markierung zu sehen und zu unterscheiden und öffnet damit ein Fenster dafür, wie sich diese Moleküle in Echtzeit verhalten.
Eine neue Art, Moleküle "hören"
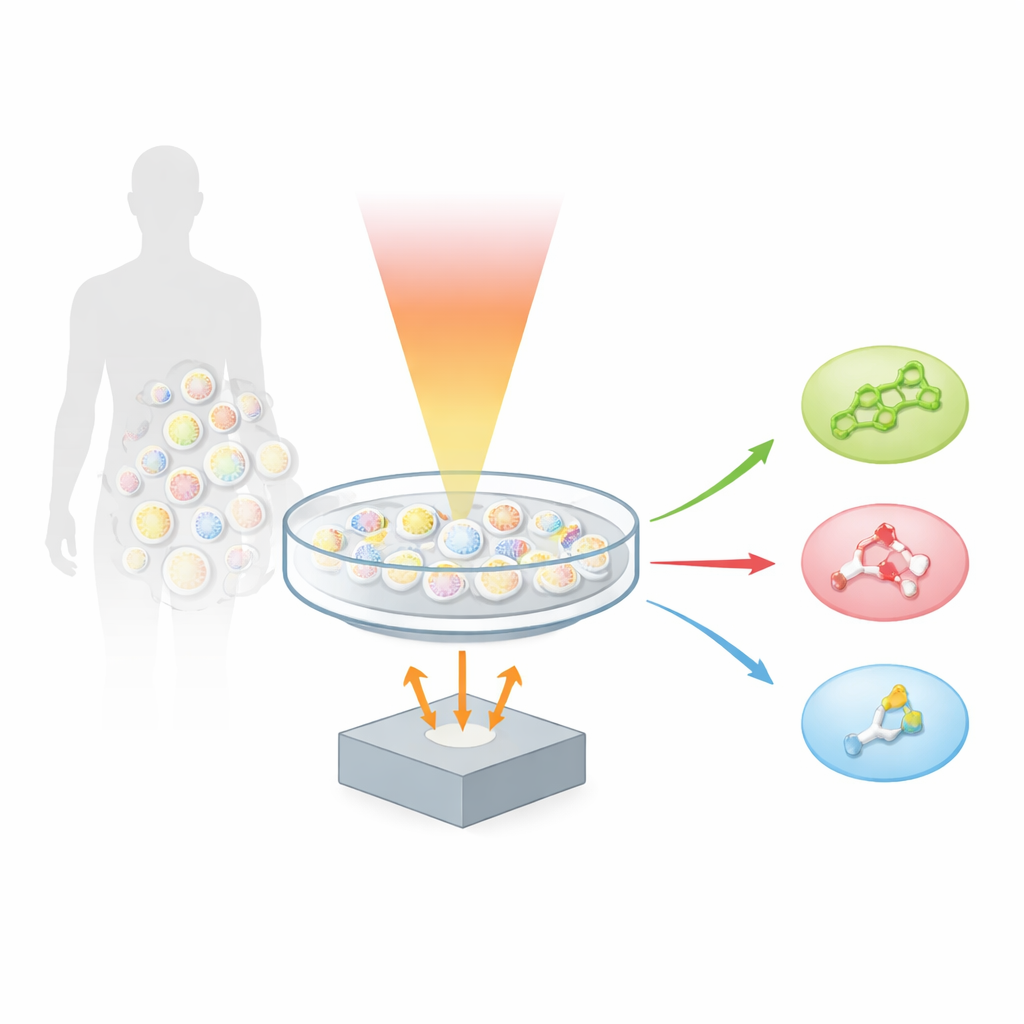
Die Autorinnen und Autoren bauen auf einer Technik auf, die Optoakustik genannt wird und Licht in Schall umwandelt. Wenn ein Molekül einen kurzen Puls infraroten Lichts absorbiert, erwärmt es sich und dehnt sich minimal aus, wodurch eine winzige Ultraschallwelle entsteht. Durch das Abtasten einer Probe mit vielen Farben des Mittel‑Infrarotlichts und das Aufzeichnen des entstehenden Schalls entwickelte das Team die „hyperspektrale Fingerprint‑optoakustische Mikroskopie“, kurz hyFOPM. Jeder Lipidtyp schwingt bei Beleuchtung im sogenannten Fingerprint‑Bereich des Infrarotspektrums, etwa zwischen 1.730 und 900 Wellenzahlen, charakteristisch. Diese Schwingungen wirken wie Barcodes und erlauben es dem System, Cholesterin von Sphingomyelin und dem häufigen Membranlipid Phosphatidylcholin zu unterscheiden, obwohl diese Moleküle gemeinsam in derselben Zellmembran vorkommen.
Methodentest an vereinfachten Proben
Um herauszufinden, wie gut hyFOPM Lipide trennen kann, testeten die Forschenden die Methode zunächst an kontrollierten Proben. Sie bereiteten kleine Vertiefungen mit reinem Cholesterin, Sphingomyelin, Phosphatidylcholin und Wasser vor und tasteten sowohl den breiten C–H‑Streckbereich als auch den detailreicheren Fingerprint‑Bereich ab. Durch mathematisches Entmischen der aufgezeichneten Spektren zeigten sie, dass der Fingerprint‑Bereich weitaus reichhaltigere Informationen liefert. Dort erzeugte Cholesterin starke Signale, die mit seiner starren Ringsystemstruktur verknüpft sind, während Sphingomyelin deutliche Merkmale seiner Amidbindungen zeigte und Phosphatidylcholin ein klares Signal von seinen Estergruppen enthielt. Statistische Analysen bestätigten, dass sich diese Spektralfingerprints mit etwa 96–97 % Genauigkeit klassifizieren ließen, wobei der Fingerprint‑Bereich allein die sauberste Trennung und die geringste Übersprechung zwischen den Spezies lieferte.
Von Modellmembranen zu realistischen Zelloberflächen
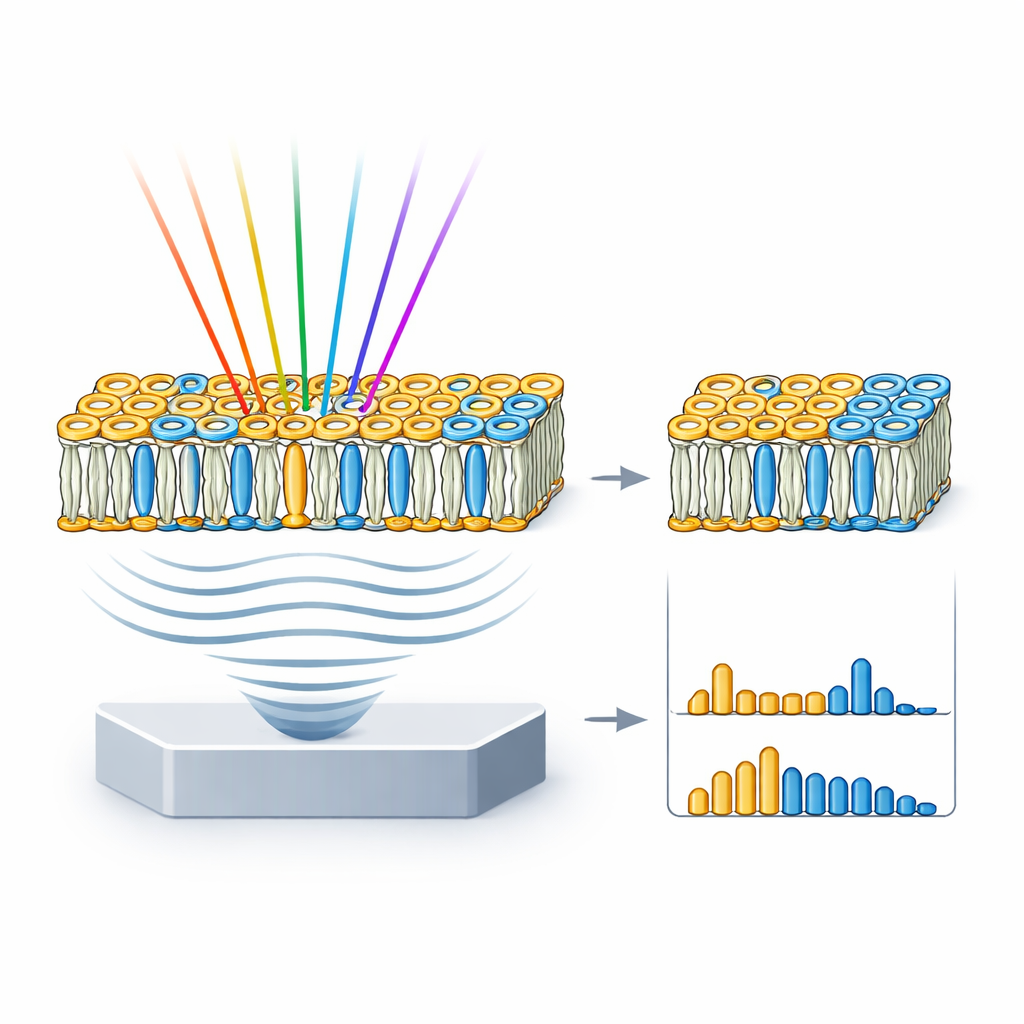
Echte Zellmembranen sind komplexer als reine Lipidvertiefungen, daher wandte sich das Team als Nächstes riesigen unilamellaren Vesikeln (GUVs) zu – zellgroßen Bläschen aus ausgewählten Lipidmischungen. Sie stellten drei Typen von GUVs her: eines dicht gepackt nur aus Sphingomyelin und Cholesterin; eines, das die gemischte, fleckige Natur einer typischen Zellmembran nachahmt; und eines, das nur aus fluidem Phosphatidylcholin besteht. HyFOPM‑Bilder zeigten diese Vesikel klar und zeigten, dass dicht gepackte Membranen stärkere Signale erzeugen als lockerere. Durch den Vergleich der Vesikelspektren mit denen der reinen Lipide und das Entmischen der Beiträge konnten die Forschenden die tatsächliche Lipidzusammensetzung jedes Vesikels rekonstruieren und sogar Chargen‑zu‑Chargen‑Schwankungen von bis zu etwa 40 % nachweisen. Das bedeutet, die Technik kann auch als Qualitätskontrollwerkzeug für Membranmodelle dienen, die häufig in Biophysik und Arzneimittelforschung verwendet werden.
Beobachtung krankheitsassoziierter Lipide in lebenden Zellen
Die eigentliche Bewährungsprobe war, ob hyFOPM spezifische Lipide in lebenden Zellen verfolgen kann, während diese auf Behandlungen reagieren. In Lungenkrebszellen, die einem experimentellen Anti‑Tumor‑Stoff ausgesetzt wurden, der bekanntermaßen Sphingomyelin erhöht, maß die Methode über 72 Stunden einen mehr als zweifachen Anstieg des spektralen Merkmals, das mit diesem Lipid verknüpft ist, während Kontrollzellen nur eine geringe Veränderung zeigten. In einem zweiten Experiment wurden menschliche Nierenzellen mit Cholesterin über Transportmoleküle überflutet. HyFOPM detektierte einen deutlichen Anstieg cholesterinbezogener Signale und einen leichten Rückgang von Sphingomyelin, was mit den bekannten Effekten dieser Behandlung auf Zellmembranen übereinstimmt. Entscheidend ist, dass diese Messungen mit nur einer Handvoll sorgfältig ausgewählter Infrarotfarben erzielt wurden, was darauf hindeutet, dass künftige Systeme durch Abtastung nur der informativsten Spektralbänder schneller gestaltet werden könnten.
Was das für Gesundheit und Krankheit bedeutet
Indem hyFOPM labelfreie, chemisch spezifische Karten von Lipiden in lebenden Zellen liefert, umgeht die Methode viele Nachteile fluoreszierender Färbungen und genetischer Marker. Forschende können nun wichtige Lipidklassen wie Cholesterin und Sphingomyelin direkt aus ihren Schwingungs‑Fingerprints unterscheiden, verfolgen, wie sie sich während Arzneimittelbehandlungen anhäufen oder verschwinden, und die echte Zusammensetzung von Modellmembranen bewerten. Da mittel‑infrarote optoakustische Signale in größeren Tiefen detektiert werden können als bei konventioneller Mikroskopie, könnten zukünftige Ausführungen dieses Ansatzes Lipidungleichgewichte in Geweben und sogar bei Patientinnen und Patienten abbilden. Das könnte schließlich helfen, Krankheiten – von Atherosklerose bis Neurodegeneration – zu diagnostizieren und zu überwachen, die zum Teil durch die verborgene Choreografie der Fette in unseren Zellen angetrieben werden.
Zitation: Gasparin, F., Prebeck, A., Soldà, A. et al. Differentiation of sphingomyelin and cholesterol by hyperspectral mid-infrared detection of single-bond vibrational modes in the fingerprint region. Nat Methods 23, 815–822 (2026). https://doi.org/10.1038/s41592-026-03025-w
Schlüsselwörter: Lipidbildgebung, Cholesterin, Sphingomyelin, optoakustische Mikroskopie, Mittel‑Infrarot‑Spektroskopie