Clear Sky Science · it
Differenziazione tra sfingomielina e colesterolo mediante rilevazione iperspettrale a medio infrarosso delle modalità vibratorie dei legami singoli nella regione fingerprint
Perché i grassi nelle nostre cellule sono importanti
I grassi, o lipidi, sono più che semplici calorie immagazzinate. Contribuiscono alla costruzione delle membrane cellulari, guidano segnali chimici e sono strettamente legati a condizioni come cancro, malattie cardiache, obesità e disturbi neurologici. Tuttavia osservare tipi specifici di lipidi all’interno di cellule vive è stato sorprendentemente difficile, spesso richiedendo coloranti fluorescenti che possono alterare i processi che i ricercatori vogliono studiare. Questo studio introduce un modo per vedere e distinguere lipidi chiave nelle cellule vive senza etichette, aprendo una finestra su come queste molecole si comportano in tempo reale.
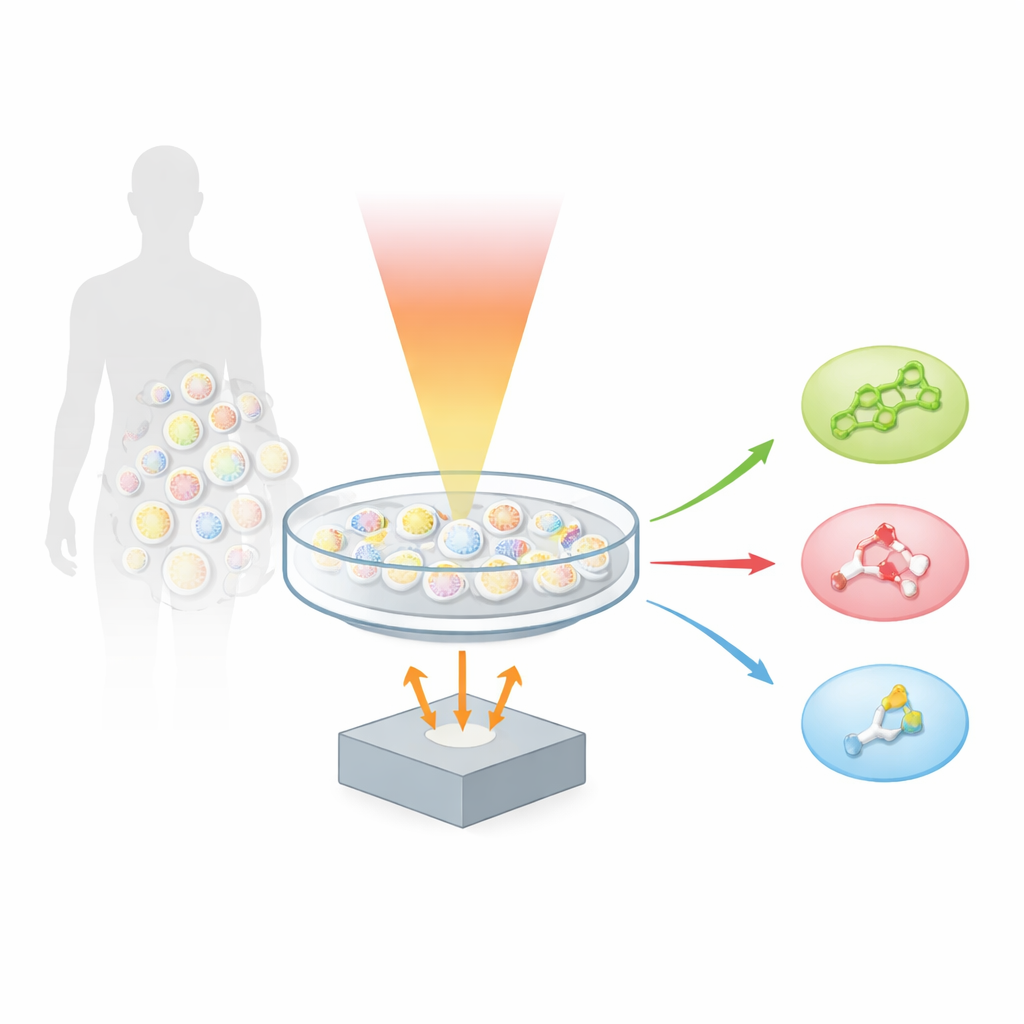
Un nuovo modo per «ascoltare» le molecole
Gli autori si basano su una tecnica chiamata optoacustica, che trasforma la luce in suono. Quando una molecola assorbe un breve impulso di luce infrarossa si riscalda e si espande impercettibilmente, generando una piccola onda ultrasonica. Scansionando un campione con molti colori di luce medio‑infrarossa e registrando il suono risultante, il team ha creato la “microscopia optoacustica iperspettrale fingerprint”, o hyFOPM. Ogni tipo di lipide vibra in modo caratteristico quando illuminato nella cosiddetta regione fingerprint dello spettro infrarosso, approssimativamente tra 1.730 e 900 centimetri inversi. Queste vibrazioni funzionano come codici a barre, permettendo al sistema di distinguere il colesterolo dalla sfingomielina e da un comune lipide di membrana chiamato fosfatidilcolina, nonostante queste molecole coesistano nella stessa membrana cellulare.
Testare il metodo su campioni semplificati
Per verificare quanto nitidamente hyFOPM potesse separare i lipidi, i ricercatori lo hanno prima testato su campioni controllati. Hanno preparato pozzetti minuscoli contenenti colesterolo puro, sfingomielina, fosfatidilcolina e acqua, e li hanno scansionati sia nella larga regione di allungamento carbonio‑idrogeno sia nella più dettagliata regione fingerprint. Separando matematicamente gli spettri registrati, hanno mostrato che la regione fingerprint contiene informazioni molto più ricche. Lì, il colesterolo ha prodotto segnali forti legati alla sua struttura ad anelli rigida, mentre la sfingomielina ha mostrato caratteristiche distintive dovute ai legami ammidici, e la fosfatidilcolina ha rivelato una firma chiara dai suoi gruppi estere. L’analisi statistica ha confermato che queste impronte spettrali permettono di classificare i tre lipidi con un’accuratezza di circa 96–97%, con la sola regione fingerprint che offriva la separazione più netta e il minore incrocio tra specie.
Da membrane modello a superfici cellulari realistiche
Le membrane cellulari reali sono più complesse dei pozzetti di lipidi puri, quindi il team ha poi esaminato vescicole giganti unilamellari, o GUV—bolle delle dimensioni di una cellula fatte con miscele scelte di lipidi. Hanno assemblato tre tipi di GUV: una densamente popolata solo da sfingomielina e colesterolo; una che imita la natura mista e a macchie di una membrana cellulare tipica; e una composta solamente da una fosfatidilcolina fluida. Le immagini hyFOPM hanno rivelato chiaramente queste vescicole e hanno mostrato che le membrane strettamente impaccate producevano segnali più forti rispetto a quelle più sciolte. Confrontando gli spettri delle vescicole con quelli dei lipidi puri e separando i contributi, i ricercatori sono riusciti a recuperare la composizione lipidica reale di ciascuna vescicola e persino a rilevare variazioni lotto dopo lotto fino a circa il 40%. Ciò significa che la tecnica può fungere anche da strumento di controllo qualità per i modelli di membrana spesso usati in biofisica e ricerca farmacologica.
Osservare i lipidi associati alle malattie all’interno di cellule vive
La vera prova era se hyFOPM potesse tracciare lipidi specifici all’interno di cellule vive mentre rispondevano a trattamenti. In cellule di cancro polmonare esposte a un composto antitumorale sperimentale noto per aumentare la sfingomielina, il metodo ha misurato un incremento superiore a due volte della caratteristica spettrale associata a quel lipide in 72 ore, mentre le cellule di controllo mostravano solo una modesta variazione. In un secondo esperimento, cellule renali umane sono state sovraccaricate di colesterolo veicolato da trasportatori. HyFOPM ha rilevato un netto aumento dei segnali legati al colesterolo e una piccola diminuzione della sfingomielina, coerente con gli effetti noti di questo trattamento sulle membrane cellulari. Crucialmente, queste misurazioni sono state ottenute utilizzando solo una manciata di colori infrarossi scelti con cura, suggerendo che i sistemi futuri potrebbero essere resi più veloci campionando soltanto le bande spettrali più informative.
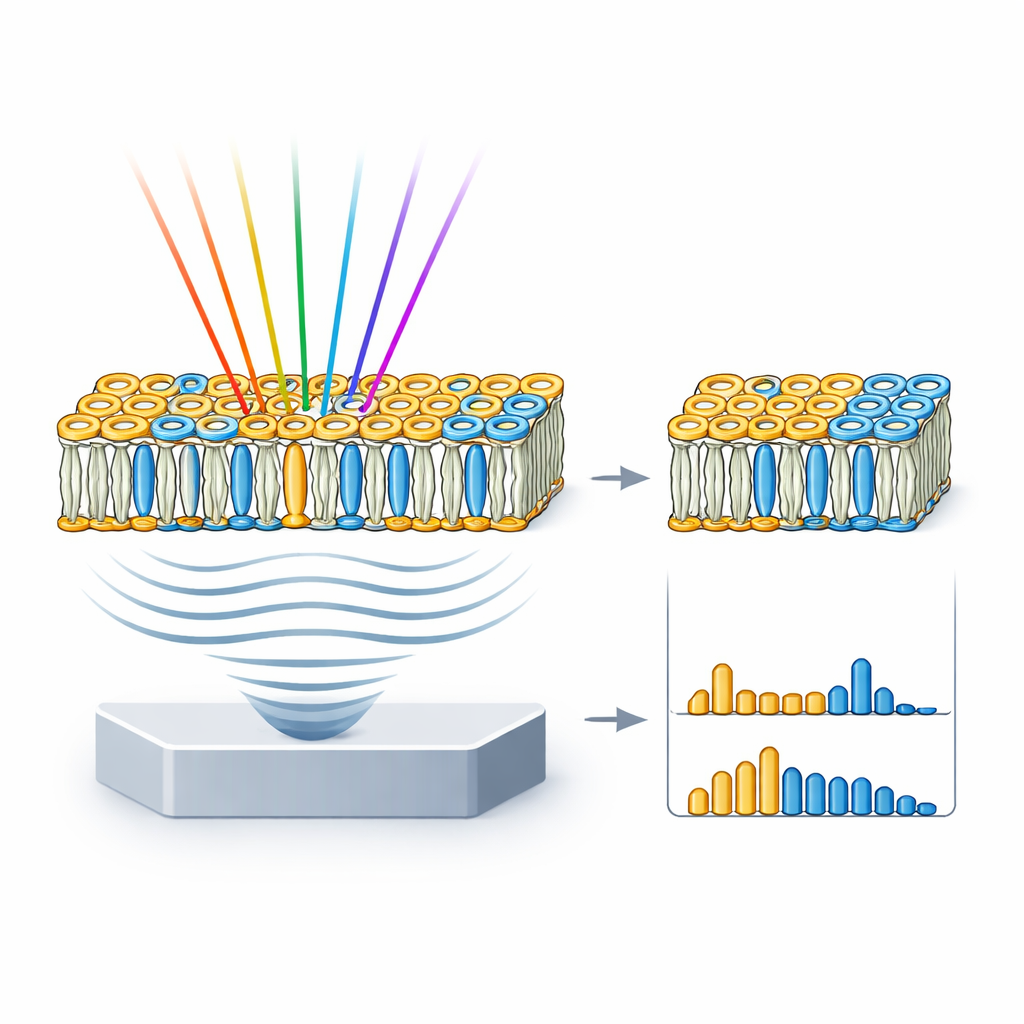
Cosa significa per la salute e le malattie
Fornendo mappe chimicamente specifiche e senza etichette dei lipidi nelle cellule vive, hyFOPM evita molti svantaggi delle colorazioni fluorescenti e dei marcatori genetici. I ricercatori possono ora differenziare classi lipidiche principali come colesterolo e sfingomielina direttamente dalle loro impronte vibratorie, seguire come si accumulano o scompaiono durante i trattamenti farmacologici e valutare la composizione reale delle membrane modello. Poiché i segnali optoacustici nel medio infrarosso possono essere rilevati a profondità maggiori rispetto a quanto consente la microscopia convenzionale, le versioni future di questo approccio potrebbero immaginare squilibri lipidici nei tessuti e persino nei pazienti. Ciò potrebbe infine aiutare a diagnosticare e monitorare malattie—dall’aterosclerosi alla neurodegenerazione—that sono in parte guidate dalla coreografia nascosta dei grassi all’interno delle nostre cellule.
Citazione: Gasparin, F., Prebeck, A., Soldà, A. et al. Differentiation of sphingomyelin and cholesterol by hyperspectral mid-infrared detection of single-bond vibrational modes in the fingerprint region. Nat Methods 23, 815–822 (2026). https://doi.org/10.1038/s41592-026-03025-w
Parole chiave: imaging dei lipidi, colesterolo, sfingomielina, microscopia optoacustica, spettroscopia mid-infrared