Clear Sky Science · sv
Differentiering av sphingomyelin och kolesterol genom hyperspektral mid‑infraröd detektion av enkelbindningsvibrationslägen i fingeravtrycksregionen
Varför fetterna i våra celler spelar roll
Fetter, eller lipider, är mer än lagrade kalorier. De bygger upp cellmembran, styr kemiska signaler och är tätt kopplade till tillstånd som cancer, hjärtsjukdom, fetma och neurologiska sjukdomar. Att iaktta specifika lipider i levande celler har dock varit överraskande svårt och har ofta krävt fluorescerande färgämnen som kan störa de processer forskarna vill studera. Denna studie presenterar ett sätt att se och särskilja viktiga lipider i levande celler utan märkning, vilket öppnar ett fönster mot hur dessa molekyler beter sig i realtid.
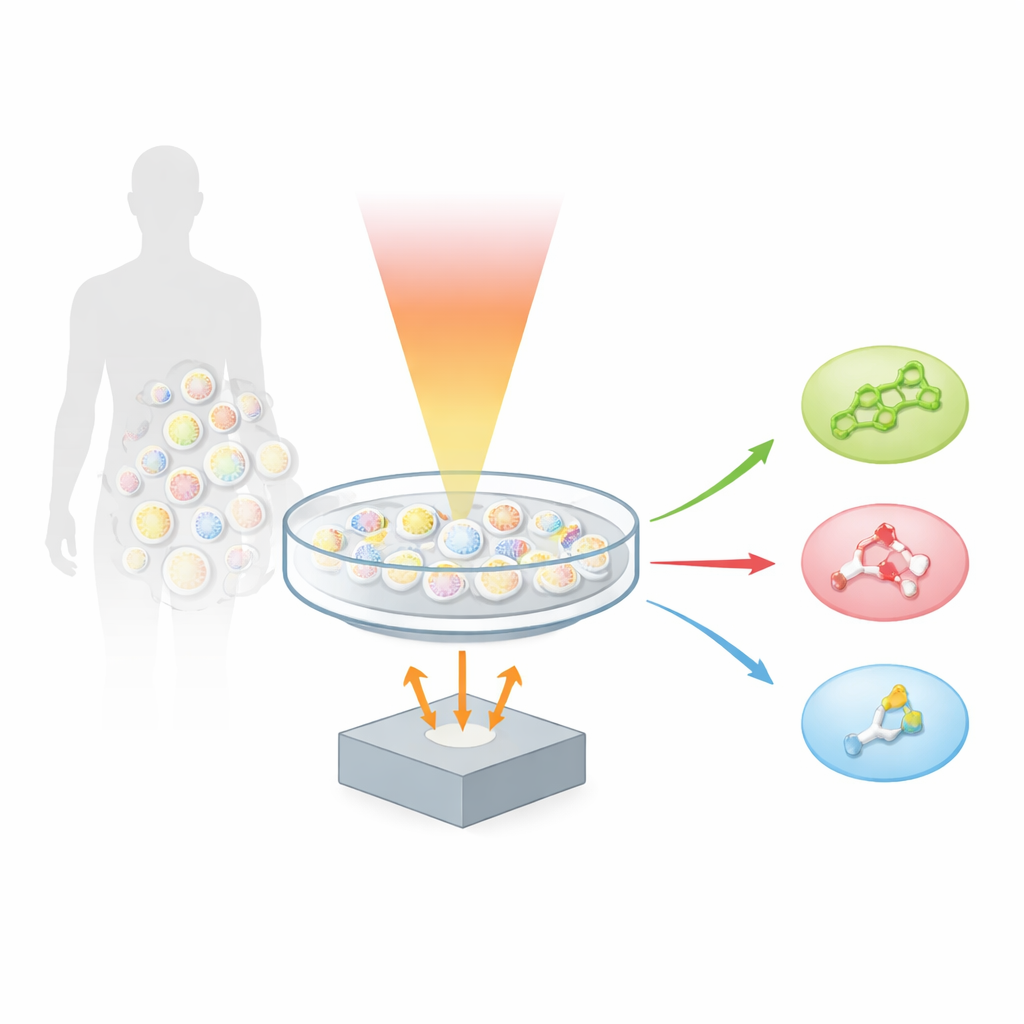
Ett nytt sätt att lyssna på molekyler
Författarna bygger vidare på en teknik kallad optoakustik, som omvandlar ljus till ljud. När en molekyl absorberar en kort puls av infrarött ljus värms den upp och expanderar en aning, vilket skapar en liten ultraljudsvåg. Genom att skanna ett prov med många färger av mid‑infrarött ljus och spela in det resulterande ljudet skapade teamet ”hyperspektral fingerprint optoacoustic microscopy”, eller hyFOPM. Varje lipidtyp vibrerar på ett karakteristiskt sätt när den belyses i den så kallade fingeravtrycksregionen av infrarött spektrum, ungefär mellan 1 730 och 900 inverse centimeter. Dessa vibrationer fungerar som streckkoder och gör att systemet kan skilja kolesterol från sphingomyelin och från en vanlig membranlipid kallad fosfatidylkolin, trots att dessa molekyler samexisterar i samma cellmembran.
Test av metoden på förenklade prover
För att ta reda på hur väl hyFOPM kunde särskilja lipider testade forskarna det först på kontrollerade prover. De förberedde små brunnar innehållande ren kolesterol, sphingomyelin, fosfatidylkolin och vatten, och skannade dem både över den breda kol‑väte‑sträckningsregionen och den mer detaljerade fingeravtrycksregionen. Genom att matematiskt avblanda de inspelade spektren visade de att fingeravtrycksregionen rymmer mycket rikare information. Där gav kolesterol starka signaler kopplade till dess styva ringstruktur, medan sphingomyelin visade distinkta drag från sina amidbindningar och fosfatidylkolin uppvisade en tydlig signatur från sina estergrupper. Statistisk analys bekräftade att dessa spektrala fingeravtryck gjorde det möjligt att klassificera de tre lipiderna med cirka 96–97% noggrannhet, där enbart fingeravtrycksregionen gav den renaste separationen och minst överhörning mellan arter.
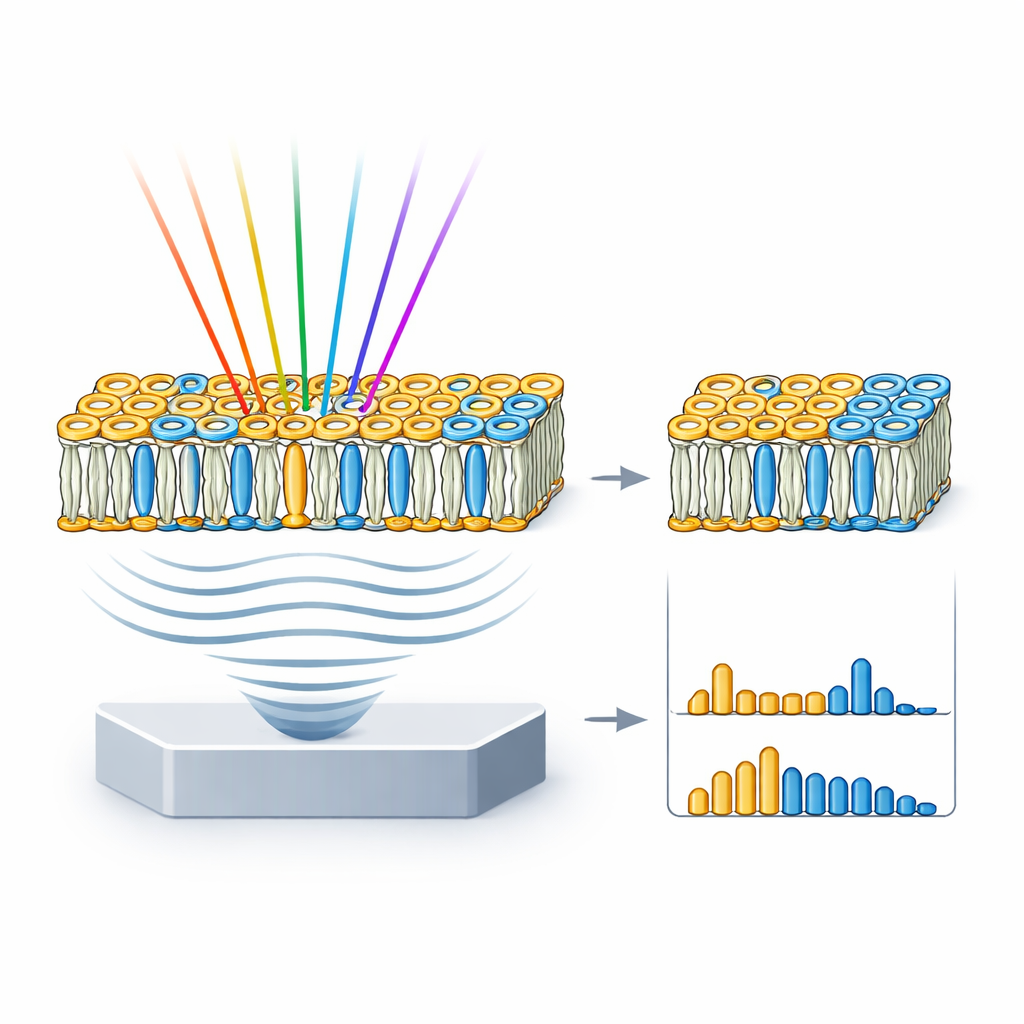
Från modellmembran till realistiska cellytor
Riktiga cellmembran är mer komplexa än rena lipidbrunnar, så teamet gick vidare till gigantiska unilamellära vesiklar, eller GUVs — cellstora bubblor gjorda av valda blandningar av lipider. De byggde tre typer av GUVs: en tätt packad med enbart sphingomyelin och kolesterol; en som efterliknar den blandade, fläckiga naturen hos ett typiskt cellmembran; och en som bara bestod av ett flytande fosfatidylkolin. HyFOPM‑bilder visade dessa vesiklar tydligt och visade att tätt packade membran gav starkare signaler än lösare. Genom att jämföra vesikelns spektra med de rena lipidernas och avblanda bidragen kunde forskarna återfå den faktiska lipidkompositionen i varje vesikel och till och med upptäcka sats‑till‑sats‑variationer på upp till cirka 40%. Det innebär att tekniken också kan fungera som ett kvalitetskontrollverktyg för membranmodeller som ofta används i biofysik- och läkemedelsforskning.
Att följa sjukdomsrelaterade lipidförändringar i levande celler
Det verkliga testet var om hyFOPM kunde spåra specifika lipider i levande celler när de svarade på behandlingar. I lungcancerceller exponerade för en experimentell anti‑tumörförening som är känd för att öka sphingomyelin mätte metoden mer än en tvåfaldig ökning av den spektrala egenskapen kopplad till den lipiden över 72 timmar, medan kontrollceller bara visade en måttlig förändring. I ett andra experiment översköljdes humana njurceller med kolesterol levererat av bärare. HyFOPM upptäckte en skarp ökning i kolesterolrelaterade signaler och en liten minskning i sphingomyelin, i linje med kända effekter av denna behandling på cellmembran. Viktigt är att dessa mätningar uppnåddes med bara ett fåtal noga utvalda infraröda färger, vilket tyder på att framtida system kan göras snabbare genom att bara sampla de mest informativa spektrala banden.
Vad detta betyder för hälsa och sjukdom
Genom att erbjuda märkfria, kemiskt specifika kartor över lipider i levande celler undviker hyFOPM många nackdelar med fluorescerande färgningar och genetiska taggar. Forskare kan nu särskilja större lipidklasser som kolesterol och sphingomyelin direkt från deras vibrationala fingeravtryck, följa hur de ackumuleras eller försvinner under läkemedelsbehandlingar och bedöma den verkliga sammansättningen av modellmembran. Eftersom mid‑infraröda optoakustiska signaler kan detekteras på djup som överstiger vad konventionell mikroskopi tillåter, kan framtida versioner av denna metod avbilda lipidobalanser i vävnader och till och med hos patienter. Det kan i förlängningen hjälpa till att diagnostisera och övervaka sjukdomar — från ateroskleros till neurodegeneration — som delvis drivs av det dolda samspelet mellan fetter i våra celler.
Citering: Gasparin, F., Prebeck, A., Soldà, A. et al. Differentiation of sphingomyelin and cholesterol by hyperspectral mid-infrared detection of single-bond vibrational modes in the fingerprint region. Nat Methods 23, 815–822 (2026). https://doi.org/10.1038/s41592-026-03025-w
Nyckelord: lipidavbildning, kolesterol, sphingomyelin, optoakustisk mikroskopi, mellaninfraröd spektroskopi