Clear Sky Science · pl
Rozróżnianie sfingomieliny i cholesterolu przez hiperspektralną detekcję w podczerwieni środkowej pojedynczych trybów drgań wiązań pojedynczych w regionie odcisków palców
Dlaczego tłuszcze w naszych komórkach mają znaczenie
Tłuszcze, czyli lipidy, to coś więcej niż zapasowe kalorie. Budują błony komórkowe, kierują sygnałami chemicznymi i są ściśle powiązane ze schorzeniami takimi jak nowotwory, choroby serca, otyłość oraz zaburzenia neurologiczne. Mimo to śledzenie konkretnych rodzajów lipidów w żywych komórkach jest zaskakująco trudne i często wymaga barwników fluorescencyjnych, które mogą zaburzać obserwowane procesy. W badaniu przedstawiono metodę pozwalającą oglądać i rozróżniać kluczowe lipidy w żywych komórkach bez znakowania, otwierając okno na zachowanie tych cząsteczek w czasie rzeczywistym.
Nowy sposób „słyszenia” cząsteczek
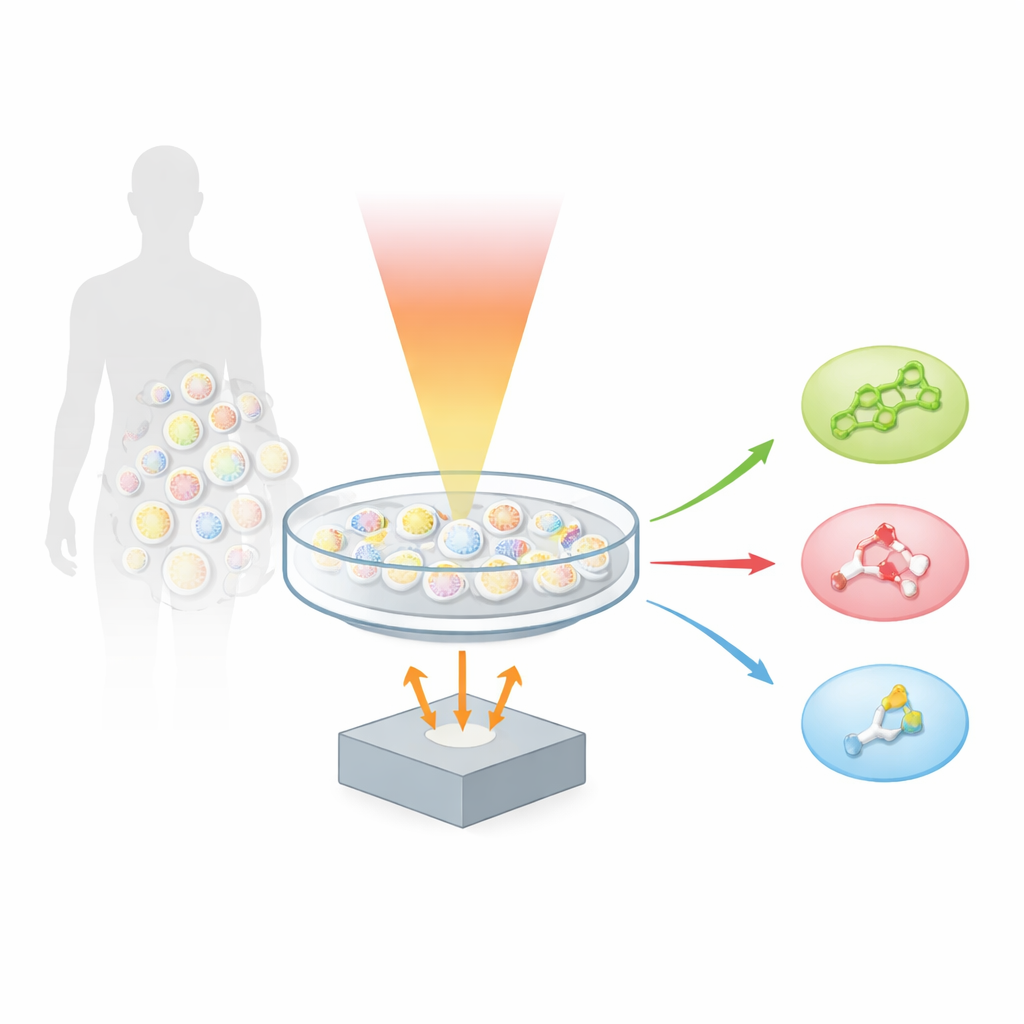
Autorzy rozwijają technikę nazwaną optoakustyką, która zamienia światło w dźwięk. Gdy cząsteczka absorbuje krótki impuls światła podczerwonego, nieco się nagrzewa i rozszerza, generując maleńką falę ultradźwiękową. Przeskanowawszy próbkę wieloma kolorami światła w paśmie podczerwieni środkowej i rejestrując powstały dźwięk, zespół stworzył „hiperspektralną optoakustyczną mikroskopię odcisków palców”, czyli hyFOPM. Każdy rodzaj lipidu drga w charakterystyczny sposób, gdy oświetli się go w tzw. regionie odcisków palców spektrum podczerwieni, mniej więcej między 1730 a 900 centymetrami odwrotnymi. Te drgania działają jak kody kreskowe, pozwalając systemowi odróżnić cholesterol od sfingomieliny i od powszechnego lipidowego składnika błon, fosfatydylocholiny, mimo że wszystkie te cząsteczki współistnieją w tej samej błonie komórkowej.
Testowanie metody na uproszczonych próbkach
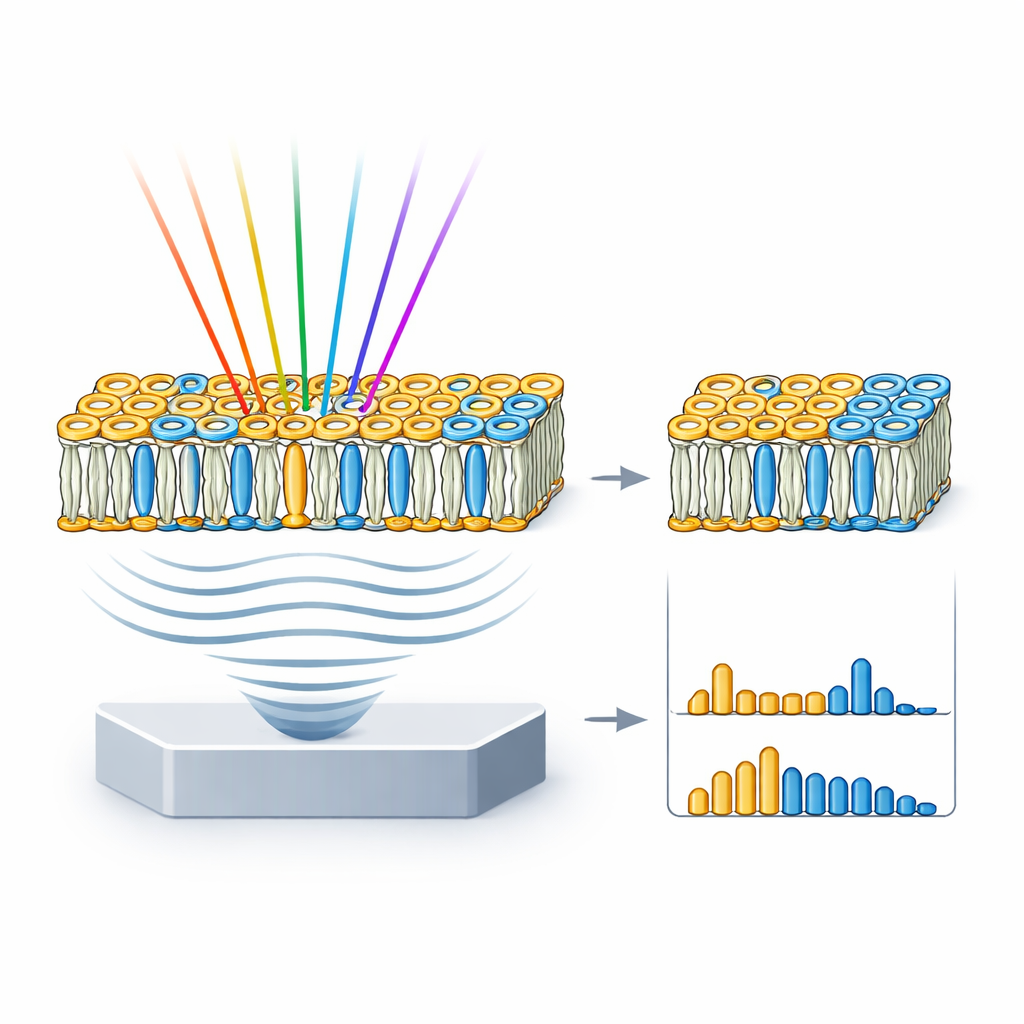
Aby ocenić, jak dokładnie hyFOPM rozdziela lipidy, badacze najpierw przetestowali ją na kontrolowanych próbkach. Przygotowali drobne studzienki zawierające czysty cholesterol, sfingomielinę, fosfatydylocholinę i wodę, i zeskanowali je zarówno w szerokim regionie rozciągania wiązań C–H, jak i w bardziej szczegółowym regionie odcisków palców. Poprzez matematyczne rozdzielenie zarejestrowanych widm pokazali, że region odcisków palców zawiera znacznie bogatsze informacje. Tam cholesterol dawał silne sygnały powiązane z jego sztywną strukturą pierścieniową, sfingomielina ujawniała odrębne cechy związane z wiązaniami amidowymi, a fosfatydylocholina wykazywała wyraźny sygnaturę z grup estrowych. Analiza statystyczna potwierdziła, że te spektroskopowe odciski palców pozwalają sklasyfikować trzy lipidy z około 96–97% dokładnością, przy czym sam region odcisków palców dawał najczystsze rozdzielenie i najmniej nakładania sygnałów między gatunkami.
Od modelowych błon do realistycznych powierzchni komórkowych
Prawdziwe błony komórkowe są bardziej złożone niż czyste studzienki z lipidami, więc zespół sięgnął po olbrzymie unilamelarne pecherzyki (GUV) — bąble o rozmiarach komórkowych złożone z wybranych mieszanek lipidów. Zmontowali trzy typy GUV: jeden gęsto upakowany wyłącznie sfingomieliną i cholesterolem; drugi naśladujący mieszany, łatwo tworzący skórki charakter typowej błony komórkowej; oraz trzeci złożony wyłącznie z płynnej fosfatydylocholiny. Obrazy hyFOPM ukazały te pecherzyki wyraźnie i pokazały, że ściśle upakowane błony generowały silniejsze sygnały niż bardziej luźne. Porównując widma pęcherzyków z widmami czystych lipidów i rozdzielając ich wkład, badacze mogli odtworzyć rzeczywiste składniki lipidowe każdego pęcherzyka, a nawet wykryć różnice między partiami sięgające około 40%. Oznacza to, że technika może równocześnie służyć jako narzędzie kontroli jakości modeli błon często stosowanych w biofizyce i badaniach nad lekami.
Obserwowanie zmian lipidów powiązanych z chorobami w żywych komórkach
Prawdziwym sprawdzianem było, czy hyFOPM potrafi śledzić konkretne lipidy w żywych komórkach w odpowiedzi na leczenie. W komórkach raka płuca wystawionych na eksperymentalny związek przeciwnowotworowy, o którym wiadomo, że zwiększa poziom sfingomieliny, metoda zmierzyła ponad dwukrotny wzrost cechy spektralnej powiązanej z tym lipidem w ciągu 72 godzin, podczas gdy komórki kontrolne wykazały jedynie umiarkowany dryf. W drugim eksperymencie komórki nerkowe człowieka zostały nasycone cholesterolem dostarczonym przez nośniki. HyFOPM wykrył gwałtowny wzrost sygnałów związanych z cholesterolem i niewielki spadek sfingomieliny, zgodny z znanym efektem tego zabiegu na błony komórkowe. Co istotne, pomiary te osiągnięto przy użyciu zaledwie kilku starannie wybranych kolorów podczerwieni, co sugeruje, że przyszłe systemy można przyspieszyć, próbkując jedynie najbardziej informatywne pasma spektralne.
Co to oznacza dla zdrowia i chorób
Dostarczając bezznakowych, chemicznie specyficznych map lipidów w żywych komórkach, hyFOPM omija wiele wad barwień fluorescencyjnych i znaczników genetycznych. Naukowcy mogą teraz bezpośrednio różnicować główne klasy lipidów, takie jak cholesterol i sfingomielina, na podstawie ich drgańowych odcisków palców, śledzić, jak się gromadzą lub zanikają podczas terapii, oraz oceniać rzeczywisty skład modelowych błon. Ponieważ sygnały optoakustyczne w podczerwieni środkowej można wykrywać na głębokościach większych niż w przypadku konwencjonalnej mikroskopii, przyszłe wersje tej metody mogą obrazować zaburzenia lipidowe w tkankach, a nawet u pacjentów. To w przyszłości mogłoby pomóc w diagnozowaniu i monitorowaniu chorób — od miażdżycy po neurodegenerację — które częściowo wynikają z ukrytej choreografii tłuszczów wewnątrz naszych komórek.
Cytowanie: Gasparin, F., Prebeck, A., Soldà, A. et al. Differentiation of sphingomyelin and cholesterol by hyperspectral mid-infrared detection of single-bond vibrational modes in the fingerprint region. Nat Methods 23, 815–822 (2026). https://doi.org/10.1038/s41592-026-03025-w
Słowa kluczowe: obrazowanie lipidów, cholesterol, sfingomielina, mikroskopia optoakustyczna, spektroskopia w podczerwieni środkowej