Clear Sky Science · fr
Différenciation de la sphingomyéline et du cholestérol par détection hyperspectrale dans l’infrarouge moyen des modes de vibration des liaisons simples dans la région «empreinte digitale»
Pourquoi les graisses de nos cellules comptent
Les graisses, ou lipides, ne sont pas de simples réserves caloriques. Elles contribuent à la construction des membranes cellulaires, orientent les signaux chimiques et sont étroitement liées à des affections comme le cancer, les maladies cardiaques, l’obésité et les troubles neurologiques. Pourtant, observer des types spécifiques de lipides à l’intérieur de cellules vivantes a été étonnamment difficile, nécessitant souvent des sondes fluorescentes qui peuvent perturber les processus mêmes que les chercheurs veulent étudier. Cette étude présente une méthode pour voir et distinguer des lipides clés dans des cellules vivantes sans aucun marquage, ouvrant une fenêtre sur le comportement de ces molécules en temps réel.
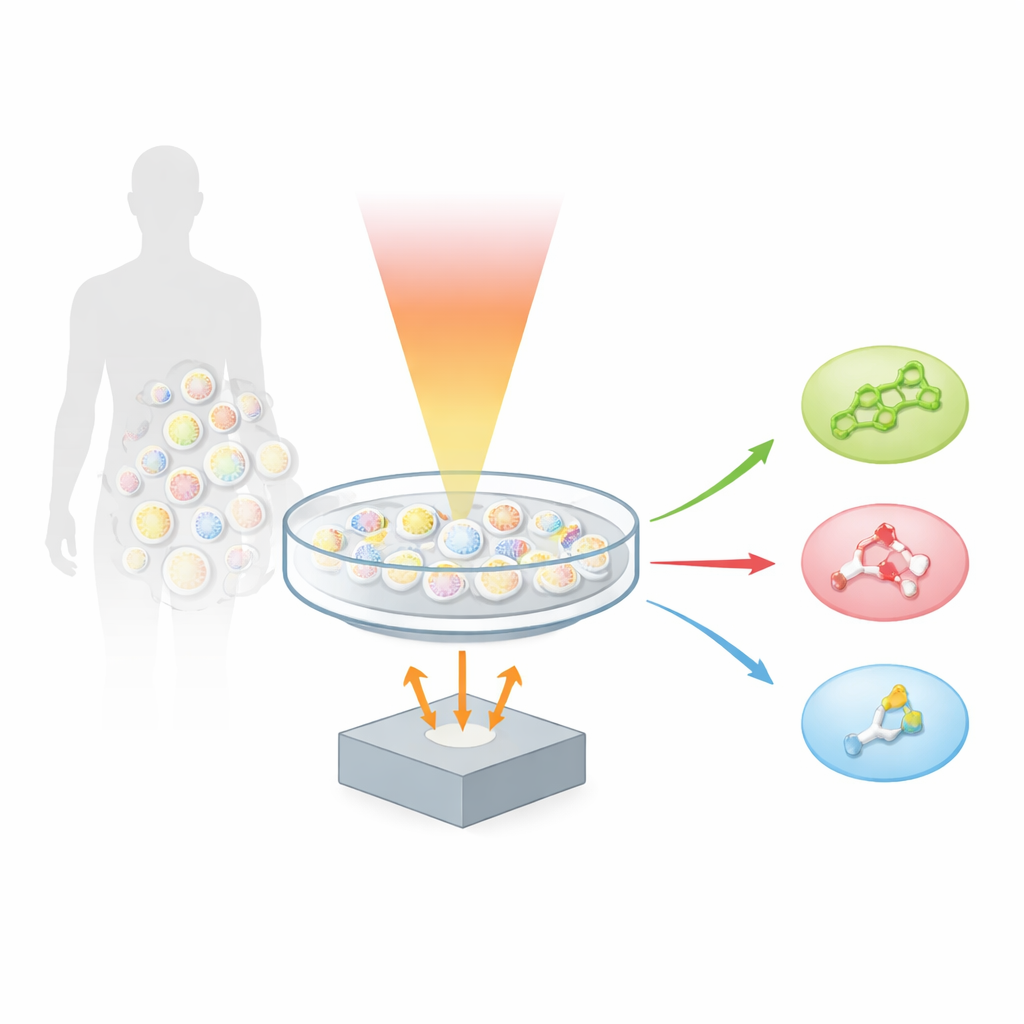
Une nouvelle façon d’écouter les molécules
Les auteurs s’appuient sur une technique appelée optoacoustique, qui convertit la lumière en son. Lorsqu’une molécule absorbe une brève impulsion de lumière infrarouge, elle se réchauffe et se dilate très légèrement, générant une petite onde ultrasonore. En balayant un échantillon avec de nombreuses longueurs d’onde dans l’infrarouge moyen et en enregistrant le son produit, l’équipe a créé la «microscopie optoacoustique hyperspectrale des empreintes», ou hyFOPM. Chaque type de lipide vibre d’une manière caractéristique lorsqu’il est éclairé dans la région dite de l’empreinte digitale du spectre infrarouge, approximativement entre 1 730 et 900 centimètres inverse. Ces vibrations jouent le rôle de codes-barres, permettant au système de distinguer le cholestérol de la sphingomyéline et d’un lipide membranaire courant appelé phosphatidylcholine, même si ces molécules cohabitent dans la même membrane cellulaire.
Tester la méthode sur des échantillons simplifiés
Pour déterminer à quel point hyFOPM pouvait séparer les lipides, les chercheurs l’ont d’abord testé sur des échantillons contrôlés. Ils ont préparé de minuscules puits contenant du cholestérol pur, de la sphingomyéline, de la phosphatidylcholine et de l’eau, et les ont balayés à la fois dans la large région d’étirement carbone–hydrogène et dans la région d’empreinte plus détaillée. En déconvoluant mathématiquement les spectres enregistrés, ils ont montré que la région d’empreinte contient des informations beaucoup plus riches. Là, le cholestérol produisait des signaux forts liés à sa structure rigide en anneaux, tandis que la sphingomyéline présentait des caractéristiques distinctes liées à ses liaisons amide, et la phosphatidylcholine révélait une signature claire de ses groupes ester. L’analyse statistique a confirmé que ces empreintes spectrales permettaient de classifier les trois lipides avec une précision d’environ 96–97 %, la région d’empreinte offrant la séparation la plus nette et le moins de recoupement entre les espèces.
Des membranes modèles aux surfaces cellulaires réalistes
Les membranes cellulaires réelles sont plus complexes que des puits de lipides purs, l’équipe s’est donc tournée vers des vésicules unilamellaires géantes (GUV) — des bulles de taille cellulaire fabriquées à partir de mélanges de lipides choisis. Ils ont assemblé trois types de GUV : l’une dense composée uniquement de sphingomyéline et de cholestérol ; une qui reproduit la nature mixte et patchée d’une membrane cellulaire typique ; et une faite uniquement de phosphatidylcholine fluide. Les images hyFOPM ont révélé ces vésicules de manière claire et montré que les membranes très compactes produisaient des signaux plus forts que les membranes plus lâches. En comparant les spectres des vésicules avec ceux des lipides purs et en séparant les contributions, les chercheurs ont pu reconstituer la composition lipidique réelle de chaque vésicule et même détecter des variations entre lots atteignant environ 40 %. Cela signifie que la technique peut aussi servir d’outil de contrôle qualité pour les modèles membranaires couramment utilisés en biophysique et en recherche pharmaceutique.
Surveiller l’évolution des lipides liés à la maladie dans des cellules vivantes
Le véritable test était de savoir si hyFOPM pouvait suivre des lipides spécifiques à l’intérieur de cellules vivantes en réponse à des traitements. Dans des cellules de cancer du poumon exposées à un composé expérimental anti‑tumoral connu pour augmenter la sphingomyéline, la méthode a mesuré une augmentation de plus de deux fois de la caractéristique spectrale liée à ce lipide sur 72 heures, tandis que les cellules témoins n’affichaient qu’une légère dérive. Dans une deuxième expérience, des cellules rénales humaines ont été surchargées de cholestérol délivré par des transporteurs. HyFOPM a détecté une augmentation nette des signaux associés au cholestérol et une petite diminution de la sphingomyéline, cohérente avec les effets connus de ce traitement sur les membranes cellulaires. Fait crucial, ces mesures ont été obtenues en n’utilisant qu’une poignée de longueurs d’onde infrarouges soigneusement choisies, ce qui suggère que des systèmes futurs pourraient être accélérés en échantillonnant uniquement les bandes spectrales les plus informatives.
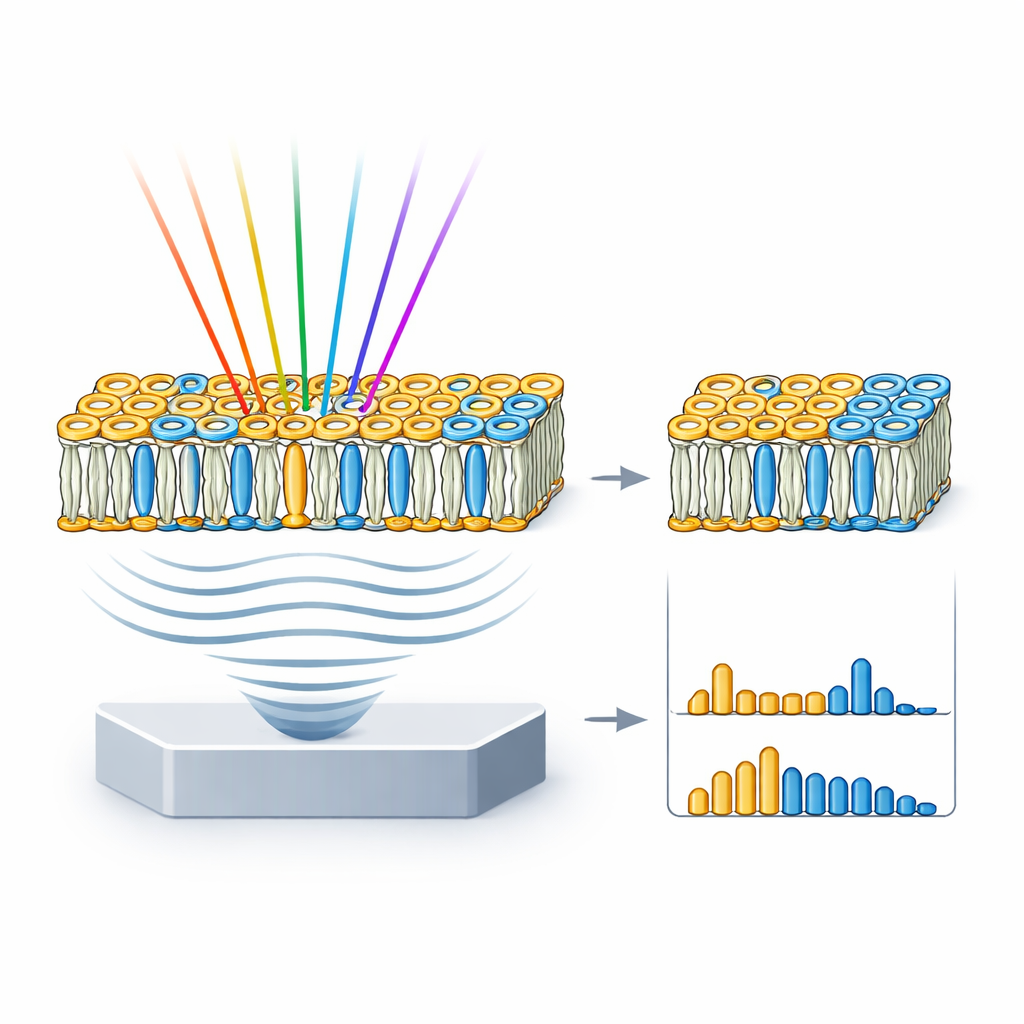
Ce que cela signifie pour la santé et la maladie
En fournissant des cartes chimiques spécifiques et sans marquage des lipides dans des cellules vivantes, hyFOPM évite de nombreux inconvénients des colorants fluorescents et des étiquettes génétiques. Les chercheurs peuvent désormais différencier directement des classes lipidiques majeures comme le cholestérol et la sphingomyéline à partir de leurs empreintes vibrationnelles, suivre leur accumulation ou leur disparition pendant des traitements médicamenteux, et évaluer la composition réelle des membranes modèles. Parce que les signaux optoacoustiques dans l’infrarouge moyen peuvent être détectés à des profondeurs supérieures à celles permises par la microscopie conventionnelle, les versions futures de cette approche pourraient imager les déséquilibres lipidiques dans les tissus et même chez les patients. Cela pourrait éventuellement aider au diagnostic et au suivi de maladies — de l’athérosclérose à la neurodégénérescence — qui sont en partie provoquées par la chorégraphie cachée des graisses à l’intérieur de nos cellules.
Citation: Gasparin, F., Prebeck, A., Soldà, A. et al. Differentiation of sphingomyelin and cholesterol by hyperspectral mid-infrared detection of single-bond vibrational modes in the fingerprint region. Nat Methods 23, 815–822 (2026). https://doi.org/10.1038/s41592-026-03025-w
Mots-clés: imagerie des lipides, cholestérol, sphingomyéline, microscopie optoacoustique, spectroscopie infrarouge moyenne