Clear Sky Science · es
Diferenciación de esfingomielina y colesterol mediante detección hiperespectral en el infrarrojo medio de modos vibracionales de enlaces simples en la región de huella
Por qué importan las grasas en nuestras células
Las grasas, o lípidos, son más que calorías almacenadas. Contribuyen a construir las membranas celulares, dirigen señales químicas y están estrechamente vinculadas a enfermedades como el cáncer, las cardiopatías, la obesidad y trastornos neurológicos. Sin embargo, observar tipos específicos de lípidos dentro de células vivas ha resultado sorprendentemente difícil, requiriendo a menudo tintes fluorescentes que pueden alterar los procesos que los científicos desean estudiar. Este estudio presenta una forma de ver y distinguir lípidos clave en células vivas sin etiquetas, abriendo una ventana a cómo se comportan estas moléculas en tiempo real.
Una nueva forma de escuchar a las moléculas
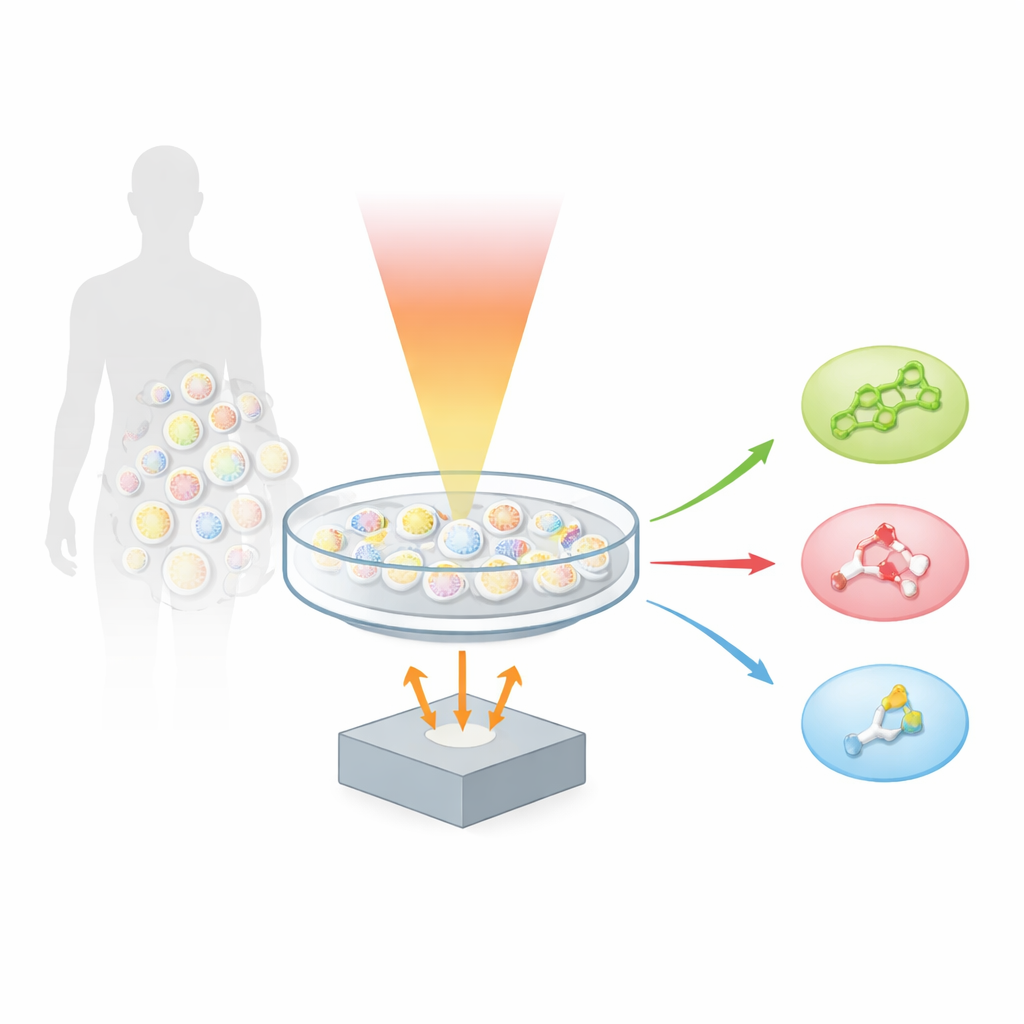
Los autores se basan en una técnica llamada optoacústica, que convierte luz en sonido. Cuando una molécula absorbe un breve pulso de luz infrarroja, se calienta y se expande mínimamente, generando una pequeña onda ultrasónica. Al escanear una muestra con muchos colores de luz del infrarrojo medio y registrar el sonido resultante, el equipo creó la “microscopía optoacústica de huella hiperespectral”, o hyFOPM. Cada tipo de lípido vibra de una manera característica cuando se ilumina en la llamada región de huella del espectro infrarrojo, aproximadamente entre 1.730 y 900 centímetros inversos. Estas vibraciones actúan como códigos de barras, permitiendo al sistema distinguir el colesterol de la esfingomielina y de un lípido de membrana común llamado fosfatidilcolina, aunque estas moléculas coexistan en la misma membrana celular.
Probando el método en muestras simplificadas
Para determinar con qué nitidez hyFOPM podía separar lípidos, los investigadores lo probaron primero en muestras controladas. Prepararon pocillos diminutos que contenían colesterol puro, esfingomielina, fosfatidilcolina y agua, y los escanearon tanto en la amplia región de estiramiento carbono–hidrógeno como en la región de huella más detallada. Mediante la desmezcla matemática de los espectros registrados, demostraron que la región de huella contiene información mucho más rica. Allí, el colesterol produjo señales fuertes vinculadas a su estructura anillada rígida, mientras que la esfingomielina mostró rasgos distintivos por sus enlaces amida, y la fosfatidilcolina reveló una firma clara por sus grupos éster. El análisis estadístico confirmó que estas huellas espectrales permitían clasificar los tres lípidos con aproximadamente un 96–97 % de precisión, siendo la región de huella la que ofrecía la separación más limpia y el menor solapamiento entre especies.
De membranas modelo a superficies celulares realistas
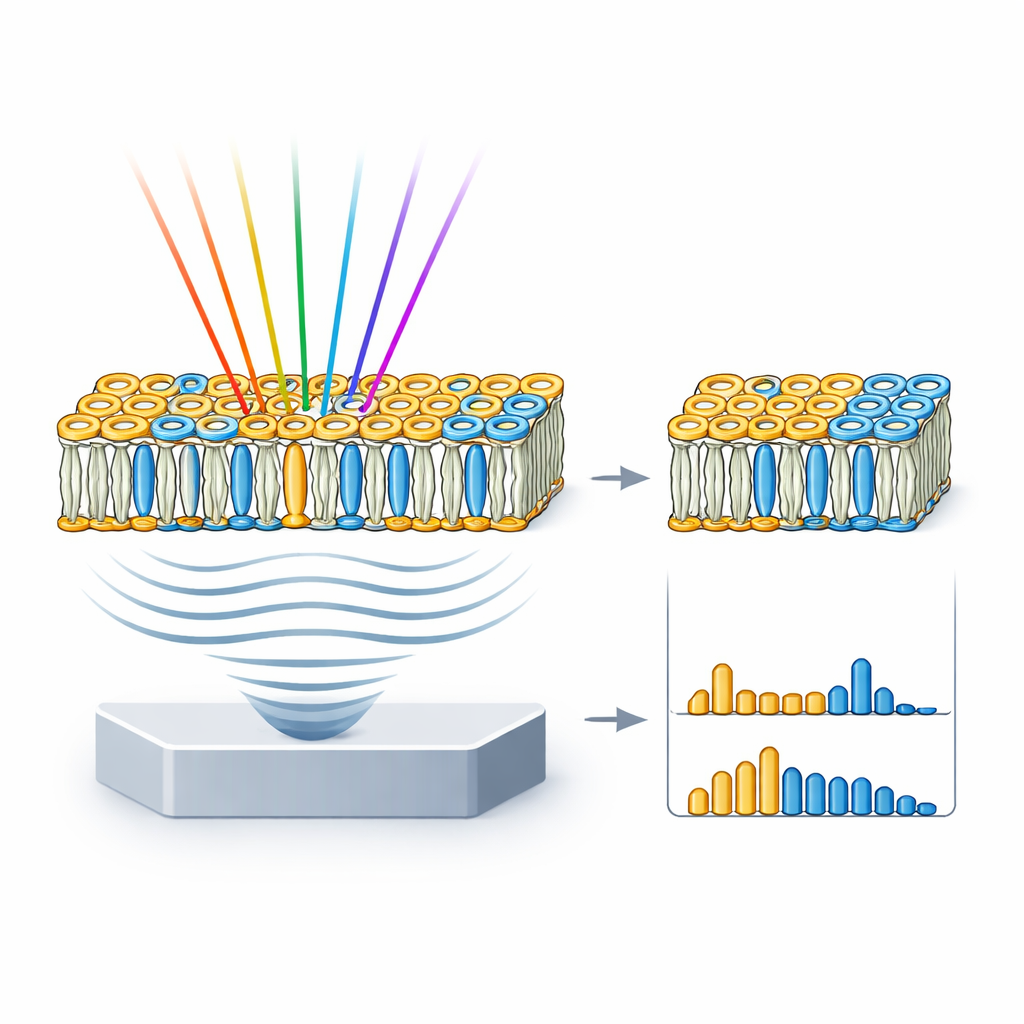
Las membranas celulares reales son más complejas que los pocillos de lípidos puros, por lo que el equipo pasó a vesículas unilamelares gigantes, o GUVs—burbujas del tamaño celular hechas con mezclas de lípidos seleccionadas. Montaron tres tipos de GUVs: una densamente empaquetada con solo esfingomielina y colesterol; otra que imita la naturaleza mixta y parcheada de una membrana celular típica; y una compuesta únicamente por una fosfatidilcolina fluida. Las imágenes hyFOPM revelaron estas vesículas con claridad y mostraron que las membranas estrechamente empaquetadas producían señales más fuertes que las más sueltas. Al comparar los espectros de las vesículas con los de los lípidos puros y desmezclar las contribuciones, los investigadores pudieron recuperar la composición lipídica real de cada vesícula e incluso detectar variaciones entre lotes de hasta alrededor del 40 %. Esto significa que la técnica puede servir también como herramienta de control de calidad para los modelos de membrana utilizados con frecuencia en biofísica e investigación farmacéutica.
Observando cambios en lípidos relacionados con enfermedades dentro de células vivas
La prueba decisiva fue si hyFOPM podría seguir lípidos específicos dentro de células vivas mientras respondían a tratamientos. En células de cáncer de pulmón expuestas a un compuesto anti-tumoral experimental conocido por aumentar la esfingomielina, el método midió un aumento de más de dos veces en la característica espectral vinculada a ese lípido durante 72 horas, mientras que las células control mostraron solo una deriva modesta. En un segundo experimento, células humanas de riñón fueron saturadas con colesterol entregado por moléculas transportadoras. HyFOPM detectó un aumento pronunciado en las señales relacionadas con el colesterol y una pequeña disminución de la esfingomielina, coherente con los efectos conocidos de este tratamiento sobre las membranas celulares. Crucialmente, estas mediciones se lograron usando solo un puñado de colores infrarrojos escogidos cuidadosamente, lo que sugiere que sistemas futuros podrían hacerse más rápidos muestreando únicamente las bandas espectrales más informativas.
Qué significa esto para la salud y la enfermedad
Al proporcionar mapas sin etiquetas y químicamente específicos de lípidos en células vivas, hyFOPM evita muchas de las limitaciones de las tinciones fluorescentes y las etiquetas genéticas. Los investigadores pueden ahora diferenciar clases lipídicas principales, como el colesterol y la esfingomielina, directamente a partir de sus huellas vibracionales, seguir cómo se acumulan o desaparecen durante tratamientos farmacológicos y evaluar la composición real de membranas modelo. Dado que las señales optoacústicas en el infrarrojo medio pueden detectarse a profundidades mayores que las permitidas por la microscopía convencional, versiones futuras de este enfoque podrían visualizar desequilibrios lipídicos en tejidos e incluso en pacientes. Eso podría, eventualmente, ayudar a diagnosticar y monitorizar enfermedades—desde la aterosclerosis hasta la neurodegeneración—que están impulsadas en parte por la coreografía oculta de las grasas dentro de nuestras células.
Cita: Gasparin, F., Prebeck, A., Soldà, A. et al. Differentiation of sphingomyelin and cholesterol by hyperspectral mid-infrared detection of single-bond vibrational modes in the fingerprint region. Nat Methods 23, 815–822 (2026). https://doi.org/10.1038/s41592-026-03025-w
Palabras clave: imágenes de lípidos, colesterol, esfingomielina, microscopía optoacústica, espectroscopía en el infrarrojo medio