Clear Sky Science · nl
Differentiatie van sphingomyeline en cholesterol door hyperspectrale midden‑infrarooddetectie van enkelbindingsvibratiemodi in het vingerafdrukgebied
Waarom de vetten in onze cellen ertoe doen
Vetten, of lipiden, zijn meer dan opgeslagen calorieën. Ze helpen bij de opbouw van celmembranen, sturen chemische signalen en hangen nauw samen met aandoeningen zoals kanker, hartziekten, obesitas en neurologische stoornissen. Toch is het opmerkelijk moeilijk geweest om specifieke soorten lipiden in levende cellen te volgen; vaak zijn fluorescente kleurstoffen nodig die de processen die onderzoekers juist willen bestuderen, kunnen verstoren. Deze studie introduceert een manier om belangrijke lipiden in levende cellen labelvrij waar te nemen en van elkaar te onderscheiden, waardoor men in realtime kan zien hoe deze moleculen zich gedragen.
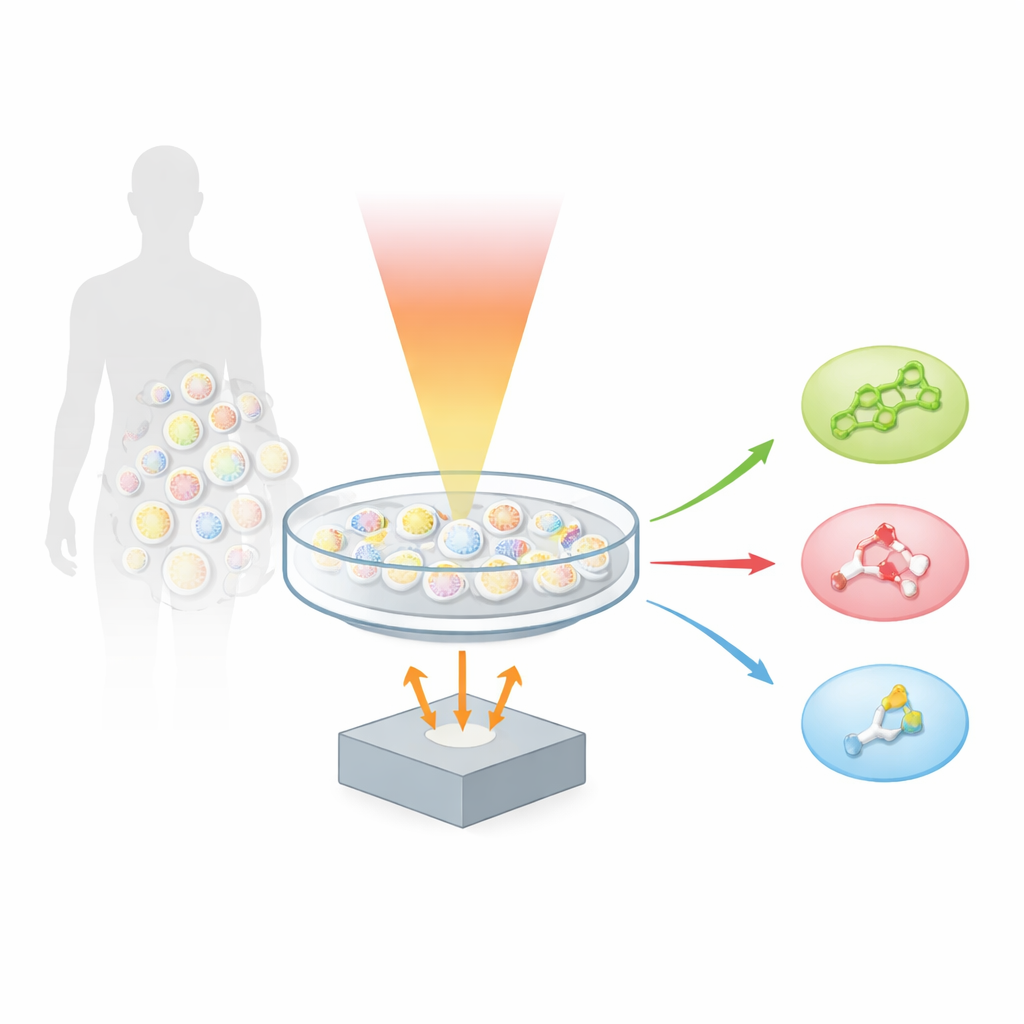
Een nieuwe manier om naar moleculen te luisteren
De auteurs bouwen voort op een techniek genaamd optoakoestiek, waarbij licht in geluid wordt omgezet. Wanneer een molecuul een korte puls infraroodlicht absorbeert, warmt het op en zet het heel licht uit, waardoor een klein ultrasoon golfje ontstaat. Door een monster te scannen met veel kleuren midden‑infraroodlicht en het resulterende geluid op te nemen, ontwikkelde het team "hyperspectrale vingerafdruk‑optoakoestische microscopie", of hyFOPM. Elk type lipide trilt op een karakteristieke manier wanneer het wordt belicht in het zogenoemde vingerafdrukgebied van het infraroodspectrum, ruwweg tussen 1730 en 900 inverse centimeters. Deze vibraties werken als streepjescodes, waardoor het systeem cholesterol kan onderscheiden van sphingomyeline en van een veelvoorkomend membraanlipide genaamd fosfatidylcholine, ook al leven deze moleculen samen in hetzelfde celmembraan.
De methode testen op vereenvoudigde monsters
Om te bepalen hoe goed hyFOPM lipiden kon scheiden, testten de onderzoekers het eerst op gecontroleerde monsters. Ze prepareerden kleine putjes met puur cholesterol, sphingomyeline, fosfatidylcholine en water, en scanden deze zowel in het brede koolstof‑waterstof stretchgebied als in het meer gedetailleerde vingerafdrukgebied. Door de opgenomen spectra wiskundig te ontmengen, lieten ze zien dat het vingerafdrukgebied veel rijkere informatie bevat. Daar gaf cholesterol sterke signalen die samenhingen met zijn stijve ringstructuur, terwijl sphingomyeline duidelijke kenmerken liet zien door zijn amidebindingen, en fosfatidylcholine een duidelijk signaal van zijn ester groepen vertoonde. Statistische analyse bevestigde dat deze spectrale vingerafdrukken de drie lipiden met ongeveer 96–97% nauwkeurigheid konden classificeren, waarbij het vingerafdrukgebied alleen de scherpste scheiding en de minste interferentie tussen de soorten gaf.
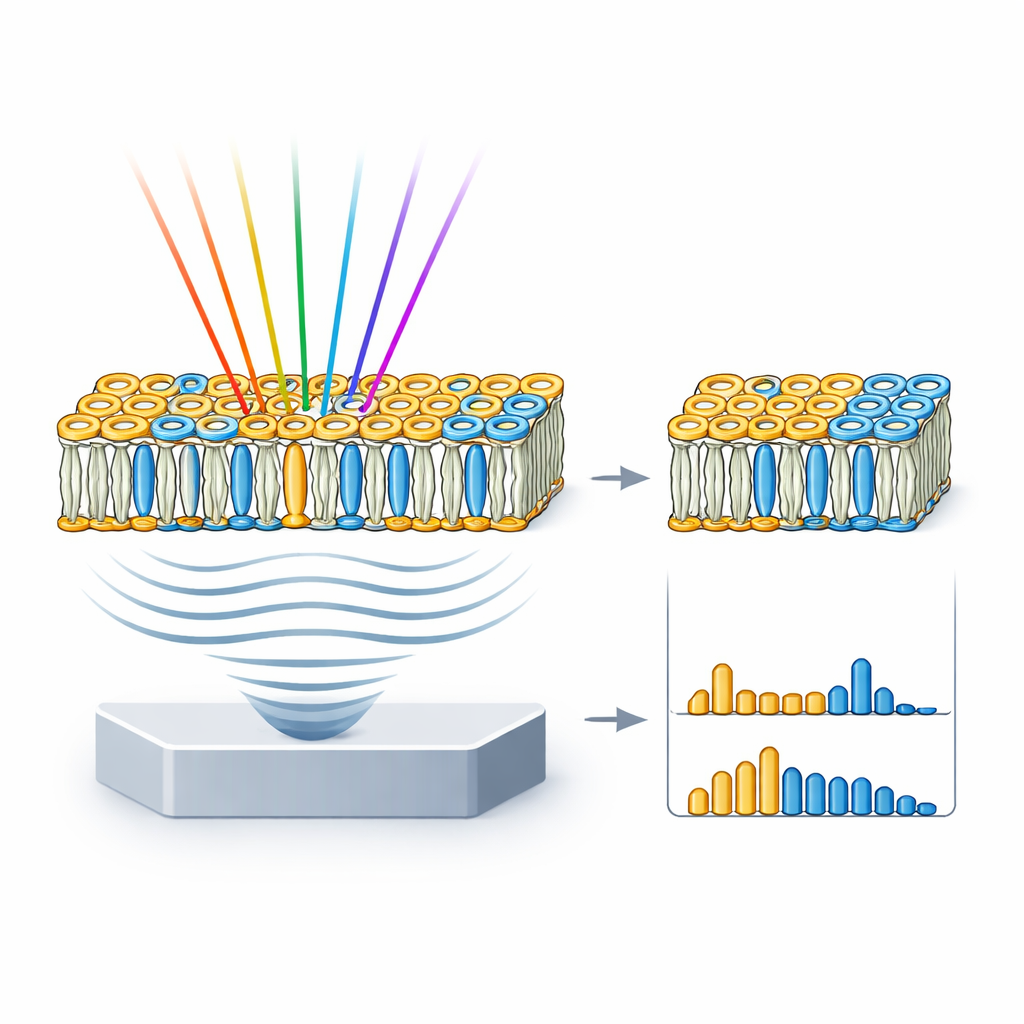
Van modelmembranen naar realistische celoppervlakken
Echte celmembranen zijn complexer dan pure lipideputjes, dus ging het team vervolgens over op gigantische unilamellaire vesikels, of GUVs—celgrote belletjes gemaakt van gekozen lipidemengsels. Ze maakten drie typen GUVs: één dicht gepakt met alleen sphingomyeline en cholesterol; één die de gemengde, vlekkerige aard van een typisch celmembraan nabootst; en één die alleen uit vloeibare fosfatidylcholine bestaat. HyFOPM‑beelden toonden deze vesikels duidelijk en lieten zien dat dicht gepakte membranen sterkere signalen produceerden dan losser gepakte. Door de vesikelspetra te vergelijken met die van de zuivere lipiden en de bijdragen te ontmengen, konden de onderzoekers de werkelijke lipidesamenstelling van elk vesikel terugvinden en zelfs batch‑tot‑batchvariatie tot ongeveer 40% detecteren. Dit betekent dat de techniek ook kan dienen als kwaliteitscontrolemiddel voor membraanmodellen die vaak worden gebruikt in biofysica en geneesmiddelenonderzoek.
Het zien veranderen van ziektegerelateerde lipiden in levende cellen
De echte test was of hyFOPM specifieke lipiden in levende cellen kon volgen terwijl die reageerden op behandelingen. In longkankercellen die werden blootgesteld aan een experimentele antitumorverbinding die bekendstaat om het verhogen van sphingomyeline, mat de methode een meer dan tweevoudige toename in het spectrale kenmerk dat aan dat lipide gekoppeld is over 72 uur, terwijl controlegroepen slechts een bescheiden verschuiving vertoonden. In een tweede experiment werden menselijke nieren cellen overspoeld met cholesterol toegediend via drager moleculen. HyFOPM detecteerde een scherpe toename in cholesterolgerelateerde signalen en een kleine afname in sphingomyeline, wat overeenkomt met bekende effecten van deze behandeling op celmembranen. Cruciaal is dat deze metingen werden bereikt met slechts een handvol zorgvuldig gekozen infraroodkleuren, wat suggereert dat toekomstige systemen sneller gemaakt kunnen worden door alleen de meest informatieve spectrale banden te bemonsteren.
Wat dit betekent voor gezondheid en ziekte
Door labelvrije, chemisch specifieke kaarten van lipiden in levende cellen te leveren, omzeilt hyFOPM veel nadelen van fluorescerende kleurstoffen en genetische tags. Onderzoekers kunnen nu belangrijke lipideklassen zoals cholesterol en sphingomyeline direct onderscheiden aan de hand van hun vibratievingerafdrukken, volgen hoe ze zich ophopen of verdwijnen tijdens medicijnbehandelingen, en de ware samenstelling van modelmembranen beoordelen. Omdat midden‑infrarood optoakoestische signalen op dieptes kunnen worden gedetecteerd die groter zijn dan wat conventionele microscopie toelaat, kunnen toekomstige versies van deze benadering lipide‑onevenwichten in weefsels en zelfs bij patiënten in beeld brengen. Dat zou uiteindelijk kunnen helpen bij het diagnosticeren en monitoren van ziekten — van atherosclerose tot neurodegeneratie — die deels worden aangedreven door de verborgen choreografie van vetten in onze cellen.
Bronvermelding: Gasparin, F., Prebeck, A., Soldà, A. et al. Differentiation of sphingomyelin and cholesterol by hyperspectral mid-infrared detection of single-bond vibrational modes in the fingerprint region. Nat Methods 23, 815–822 (2026). https://doi.org/10.1038/s41592-026-03025-w
Trefwoorden: lipidenbeeldvorming, cholesterol, sphingomyeline, optoakoestische microscopie, middeninfraroodspectroscopie