Clear Sky Science · ru
Дифференциация сфингомиелина и холестерина с помощью гиперспектрального среднеинфракрасного обнаружения колебаний одинарных связей в отпечаточной области
Почему жиры в наших клетках важны
Жиры, или липиды, — это не только запас калорий. Они участвуют в построении мембран клеток, управляют химическими сигналами и тесно связаны с такими заболеваниями, как рак, сердечно‑сосудистые болезни, ожирение и неврологические расстройства. Тем не менее наблюдать за конкретными типами липидов в живых клетках оказалось довольно сложно: часто для этого используют флуоресцентные красители, которые могут нарушать процессы, которые исследователи стремятся изучить. В этой работе представлен способ видеть и различать ключевые липиды в живых клетках без меток, что открывает окно в поведение этих молекул в реальном времени.
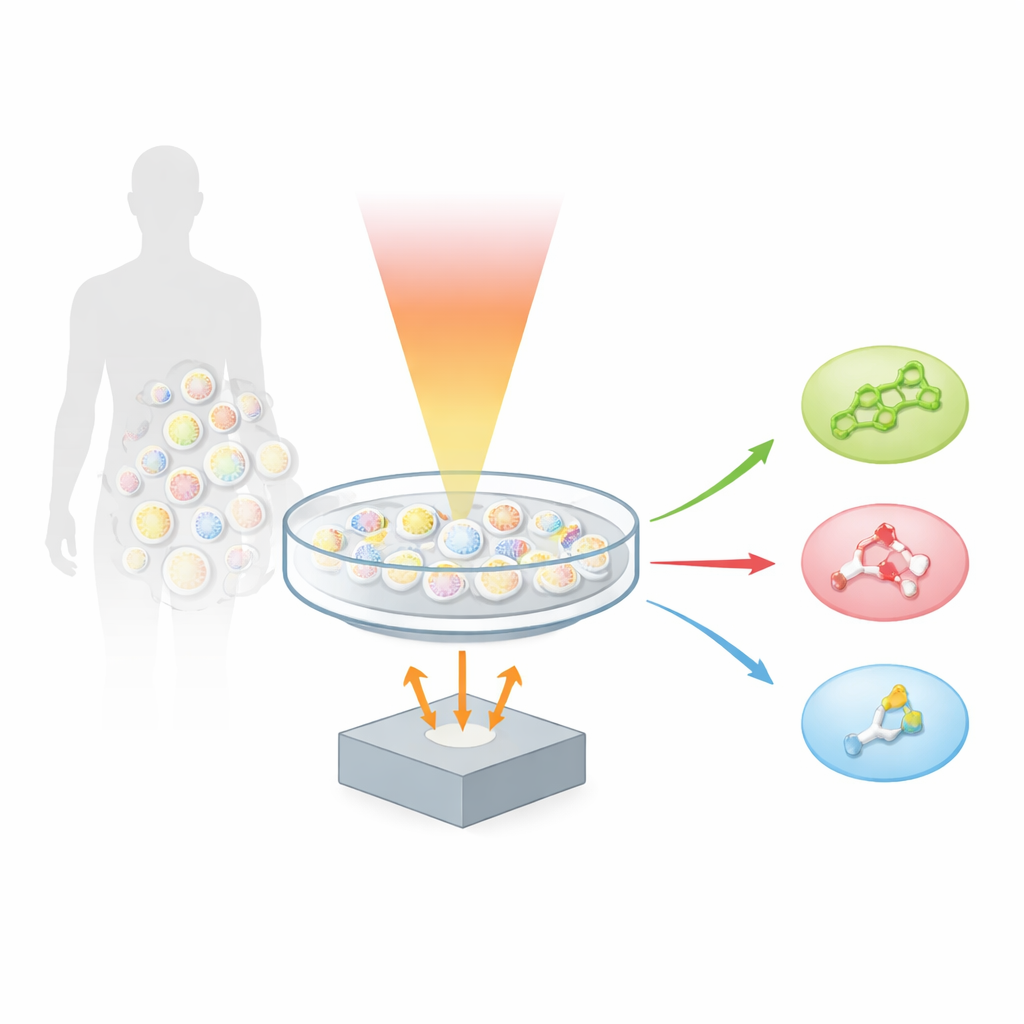
Новый способ «слушать» молекулы
Авторы опираются на технику, называемую оптоакустикой, которая превращает свет в звук. Когда молекула поглощает короткий импульс инфракрасного света, она слегка нагревается и расширяется, вызывая крошечную ультразвуковую волну. Сканируя образец множеством цветов среднеинфракрасного света и записывая полученный звук, команда создала «гиперспектральную отпечаточную оптоакустическую микроскопию», или hyFOPM. Каждый тип липида колеблется характерным образом при освещении в так называемой отпечаточной области инфракрасного спектра, примерно между 1730 и 900 обратных сантиметров. Эти колебания действуют как штрих‑коды, позволяя системе отличать холестерин от сфингомиелина и от распространённого мембранного липида фосфатидилхолина, хотя все эти молекулы сосуществуют в одной и той же клеточной мембране.
Проверка метода на упрощённых образцах
Чтобы оценить, насколько чётко hyFOPM может разделять липиды, исследователи сначала испытали метод на контролируемых образцах. Они приготовили маленькие лунки с чистым холестерином, сфингомиелином, фосфатидилхолином и водой и просканировали их как в широкой области растяжений углерод–водородных связей, так и в более детальной отпечаточной области. Математически разлагая записанные спектры, они показали, что отпечаточная область содержит гораздо более богатую информацию. Там холестерин давал сильные сигналы, связанные с его жёсткой кольцевой структурой, тогда как сфингомиелин проявлял отличительные особенности, связанные с амидными связями, а фосфатидилхолин давал ясную подпись от своих эфирных групп. Статистический анализ подтвердил, что эти спектральные отпечатки позволяли классифицировать три липида с точностью примерно 96–97%, при этом сама отпечаточная область обеспечивала наилучшее разделение и наименьшее взаимное наложение сигналов между видами.
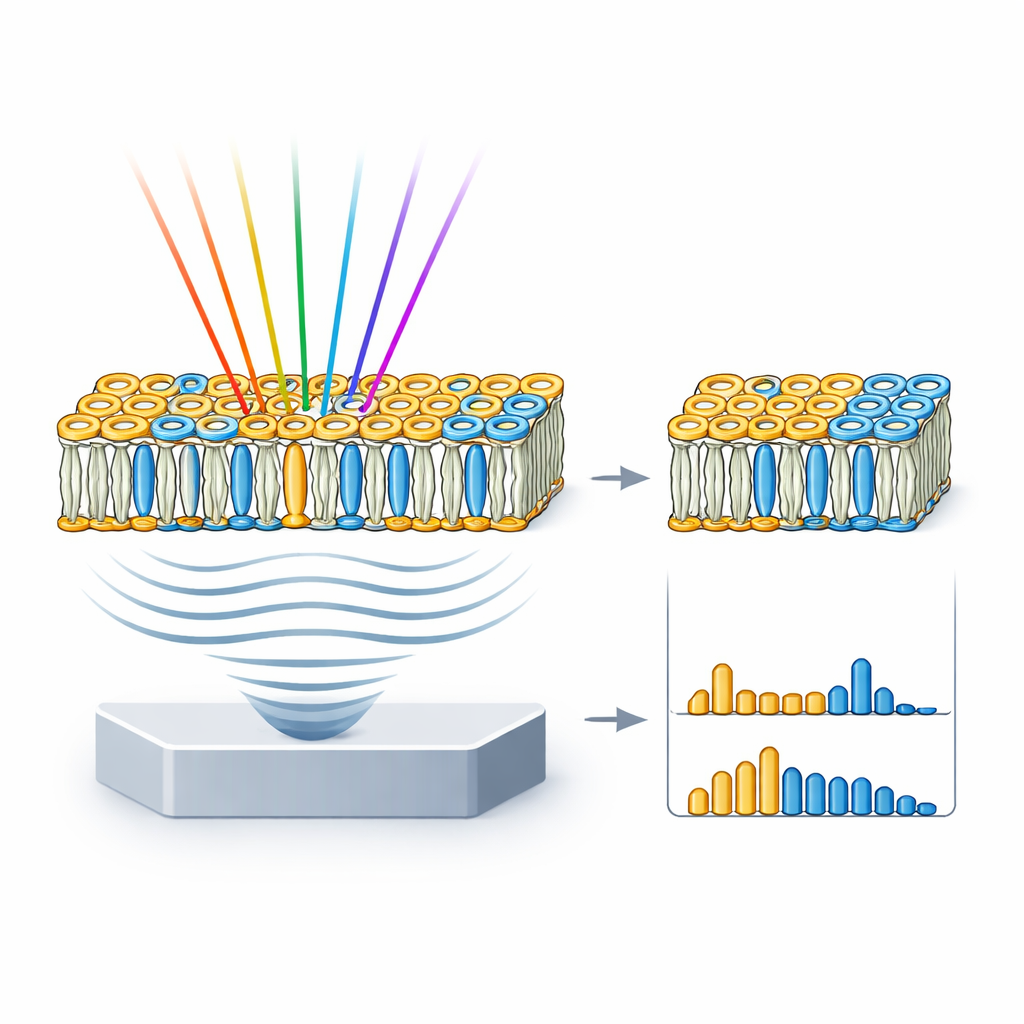
От модельных мембран к реалистичным поверхностям клеток
Реальные клеточные мембраны сложнее, чем чистые лунки с липидами, поэтому команда перешла к изучению гигантских униламеллярных везикул (GUV) — клеткоразмерных пузырьков, собранных из выбранных смесей липидов. Они собрали три типа GUV: один плотно упакованный только сфингомиелином и холестерином; один, имитирующий смешанную, пятнистую природу типичной клеточной мембраны; и один, состоящий только из текучего фосфатидилхолина. Изображения hyFOPM чётко выявляли эти везикулы и показали, что плотно упакованные мембраны давали более сильные сигналы, чем более рыхлые. Сравнивая спектры везикул со спектрами чистых липидов и разлагая вклады компонентов, исследователи могли восстановить фактический состав липидов в каждой везикуле и даже обнаружить различия между партиями до примерно 40%. Это означает, что метод может служить и средством контроля качества для мембранных моделей, часто используемых в биофизике и фармацевтических исследованиях.
Наблюдение изменений липидов, связанных с болезнями, в живых клетках
Ключевым испытанием было то, сможет ли hyFOPM отслеживать конкретные липиды в живых клетках по мере их реакции на воздействия. В клетках рака лёгкого, подвергнутых экспериментальному противоопухолевому соединению, известному тем, что повышает уровень сфингомиелина, метод за 72 часа зафиксировал более чем двукратное увеличение спектральной особенности, связанной с этим липидом, тогда как контрольные клетки показали лишь незначительные изменения. В другом эксперименте человеческие клетки почки насыщали холестерином, доставленным переносчиками. HyFOPM обнаружил резкое увеличение сигналов, связанных с холестерином, и небольшое уменьшение сфингомиелина, что согласуется с известными эффектами такого воздействия на мембраны клетки. Важно, что эти измерения были выполнены с использованием лишь нескольких тщательно выбранных инфракрасных цветов, что указывает на возможность создания более быстрых систем, которые будут измерять только наиболее информативные спектральные полосы.
Что это означает для здоровья и болезней
Предоставляя картины липидов в живых клетках без использования меток и с химической специфичностью, hyFOPM обходит многие недостатки флуоресцентных красителей и генетических меток. Исследователи теперь могут различать основные классы липидов, такие как холестерин и сфингомиелин, непосредственно по их колебательным отпечаткам, отслеживать, как они накапливаются или исчезают при лечении препаратами, и оценивать истинный состав модельных мембран. Поскольку среднеинфракрасные оптоакустические сигналы могут детектироваться на глубинах, превышающих возможности обычной микроскопии, будущие версии этого подхода могут визуализировать дисбалансы липидов в тканях и даже у пациентов. Это в конечном итоге может помочь в диагностике и мониторинге заболеваний — от атеросклероза до нейродегенерации — которые отчасти обусловлены скрытой хореографией жиров внутри наших клеток.
Цитирование: Gasparin, F., Prebeck, A., Soldà, A. et al. Differentiation of sphingomyelin and cholesterol by hyperspectral mid-infrared detection of single-bond vibrational modes in the fingerprint region. Nat Methods 23, 815–822 (2026). https://doi.org/10.1038/s41592-026-03025-w
Ключевые слова: визуализация липидов, холестерин, сфингомиелин, оптоакустическая микроскопия, среднеинфракрасная спектроскопия