Clear Sky Science · zh
肺纤维化免疫肽组分析为识别治疗靶点提供平台
让免疫系统反攻肺部瘢痕
肺纤维化,尤其是特发性肺纤维化,是一种致命的肺病,正常组织逐渐被僵硬的瘢痕取代。现有药物可以减缓这一过程,但很少能够阻止,更不用说逆转已经发生的损伤。本研究提出了一个大胆的问题:是否可以训练机体自身的免疫系统识别并选择性清除促成瘢痕形成的细胞,就像现代癌症免疫疗法对抗肿瘤那样?
为何肺部瘢痕如此难治
纤维化并非小众问题:全球约四分之一的人会出现某种形式的器官瘢痕,在工业化国家,高达45%的死亡与纤维化疾病相关。在特发性肺纤维化中,肺部的微小损伤无法完全愈合。取而代之的是,称为肌成纤维细胞和某些类型巨噬细胞的专门细胞沉积过多的结缔组织,将柔软、通气的肺转变为僵硬的蜂窝状瘢痕。获批药物可以抑制炎症并减缓进一步损伤,但对已经存在并维持瘢痕形成的细胞几乎无能为力。作者推测,如果这些关键病变细胞在表面展示出独特的分子“标记”,就可能诱导免疫系统识别并清除它们。
读取病变细胞隐藏的标记
每个细胞不断将其内部蛋白降解为短片段,并通过称为MHC I类的分子在表面展示其中一部分。这些片段共同构成了被T细胞检测以判断危险信号的“免疫肽组”。研究人员利用先进的质谱技术,编目了来自特发性肺纤维化患者瘢痕肺组织以及由药物博来霉素诱导的标准小鼠肺纤维化模型中的这些肽片段。他们发现,纤维化肺展现出比健康肺更广泛且截然不同的一组肽,多数肽的来源基因在参与组织重塑的成纤维细胞和巨噬细胞中高度活跃。
借助计算筛选最有前景的靶点
由于每个人携带独特的MHC组合,且同时可展示成千上万个肽,团队构建了一个名为Fib-SCORE的计算流程来优先排序在小鼠中最有潜力的肽靶点。Fib-SCORE根据肽的检测置信度、预测的MHC结合强度、在纤维化肺中出现的一致性以及其来源基因是否在促瘢痕细胞类型中特异性表达来筛选肽。这一流程将数千个候选者精炼为一份集中名单。三种肽——来源于蛋白MAF、APBB2和TNS3——在小鼠和人类肺中均与纤维化相关的肌成纤维细胞和巨噬细胞强烈相关,脱颖而出。
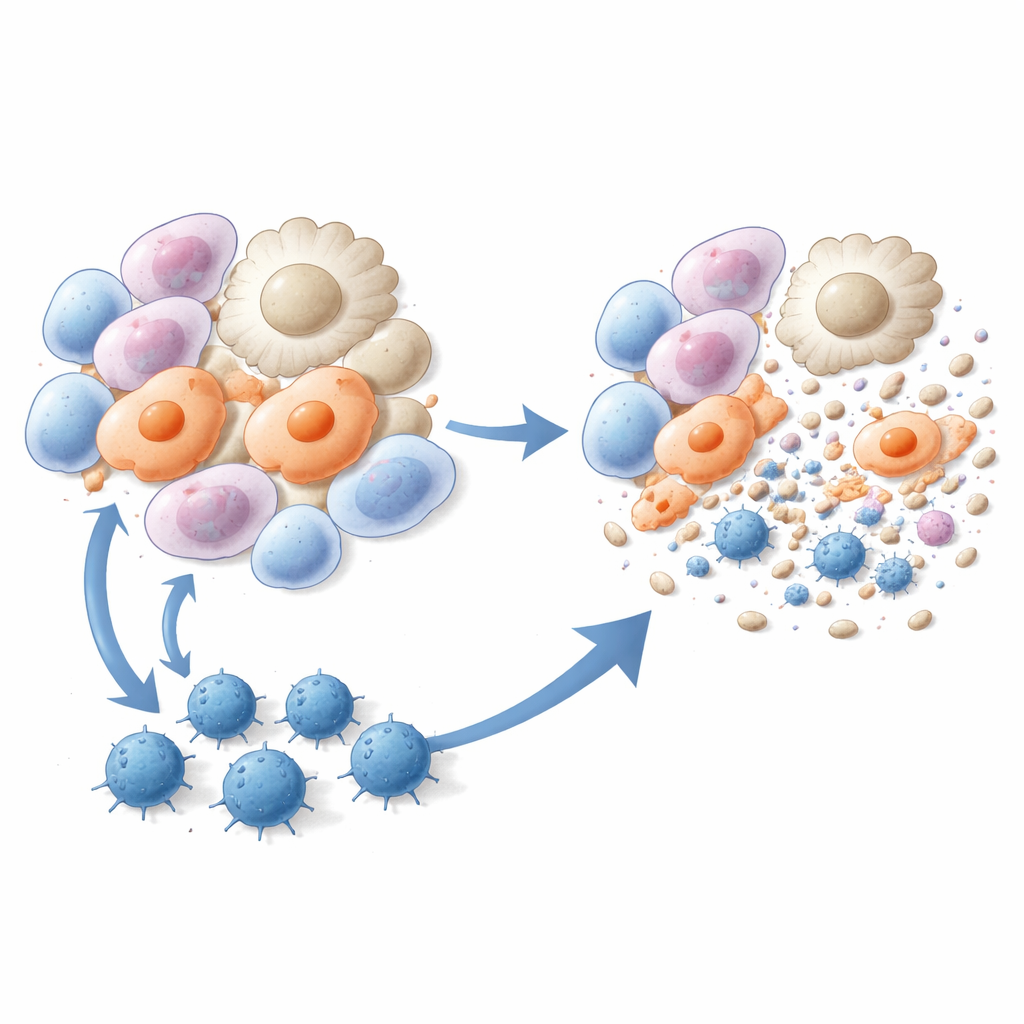
训练杀伤性T细胞清除纤维化细胞
随后研究人员将这三种肽制成疫苗。小鼠在博来霉素处理前或处理后不久接受装入脂质体、并含有免疫增强成分的肽注射。与未处理动物相比,接种疫苗的小鼠形成的纤维化病灶更少,肺内胶原沉积减少,组织结构在显微镜下明显改善。单细胞RNA测序显示,两类特别有害的细胞群——瘢痕相关巨噬细胞和肺泡肌成纤维细胞——在接种后显著减少。免疫学测试证实,肽疫苗能诱导出强大且具肽特异性的CD8 T细胞,这些细胞会增殖、产生干扰素-γ,并在体外培养和体内有效杀伤肌成纤维细胞与促纤维化巨噬细胞。
具有人体潜力的领先肽
在三种候选肽中,来源于MAF的肽(研究中称为MAF116–124)显示出最强的总体益处。在小鼠中,接种该肽疫苗可重塑肺内环境:有害的瘢痕相关细胞数量减少,记忆型CD8 T细胞在肺内积累,并观察到杀伤性T细胞与正在发生细胞死亡的肌成纤维细胞直接接触。由于MAF肽序列在小鼠与人类之间高度保守,团队进一步测试其是否也能激活人体T细胞。利用携带兼容HLA类型的健康供血者血液,他们体外生成了特异性针对MAF肽的人体细胞毒性T细胞。这些人T细胞对呈递肽的细胞产生增殖反应,并选择性破坏来自患者的肌成纤维细胞和类M2巨噬细胞,结果与小鼠实验一致。
对未来治疗的潜在意义
这项工作提出了一个新概念:利用纤维化细胞表面肽片段的精细图谱设计疫苗,使杀伤性T细胞针对瘢痕形成的主要驱动者。在小鼠中,这类疫苗不仅减缓了纤维化——它们还能减少瘢痕组织并耗竭维持瘢痕的细胞类型。尽管该研究存在局限性,包括人类组织样本量小以及依赖小鼠损伤模型,但它为将纤维化疾病转化为可通过精确免疫疗法靶向的病症提供了蓝图。如果类似的肽疫苗在特发性肺纤维化患者中被证明安全且有效,最终它们可能补充甚至超越现有药物,通过利用免疫系统寻找并清除将愈合变为有害的细胞来发挥作用。
引用: Bai, Z., Lan, T., Hong, W. et al. Immunopeptidome profiling in pulmonary fibrosis provides a platform for identifying therapeutic targets. Nat Immunol 27, 923–936 (2026). https://doi.org/10.1038/s41590-026-02501-x
关键词: 肺纤维化, 免疫疗法, 肽疫苗, CD8 T 细胞, 肌成纤维细胞