Clear Sky Science · ru
Профилирование иммунопептидомы при легочном фиброзе предоставляет платформу для выявления терапевтических мишеней
Превращение иммунной системы в оружие против легочных рубцов
Легочный фиброз, особенно идиопатический легочный фиброз, — смертельное заболевание лёгких, при котором нормальная ткань постепенно заменяется жёстким рубцом. Существующие препараты могут замедлить этот процесс, но редко останавливают его и тем более не обращают уже произошедшие повреждения. В этом исследовании поставлен смелый вопрос: можно ли обучить собственную иммунную систему организма распознавать и выборочно удалять клетки, приводящие к рубцеванию, подобно тому, как современные иммунотерапии борются с опухолями?
Почему с легочными рубцами так трудно справиться
Фиброз — не локальная проблема: примерно у каждого четвёртого человека в мире развивается та или иная форма рубцевания органов, и до 45% смертей в индустриализованных странах связаны с фиброзными заболеваниями. При идиопатическом легочном фиброзе микроскопические раны в лёгком никогда полностью не заживают. Вместо этого специализированные клетки — миофибробласты и определённые типы макрофагов — откладывают избыточную соединительную ткань, превращая мягкое, воздухопроницаемое лёгкое в жёсткую «сотовую» структуру рубца. Одобренные лекарства могут подавлять воспаление и замедлять дальнейшее повреждение, но они мало что делают для удаления уже закрепившихся клеток, формирующих рубец. Авторы предположили, что если эти ключевые виновники выставляют на своей поверхности отличительные молекулярные «флажки», иммунную систему можно будет направить на их распознавание и устранение.
Чтение скрытых флажков на больных клетках
Каждая клетка постоянно расщепляет свои внутренние белки на короткие фрагменты и демонстрирует часть этих фрагментов на поверхности с помощью молекул MHC класса I. В совокупности эти фрагменты образуют «иммунопептидом» — набор пептидов, который T-клетки просматривают в поисках признаков опасности. Исследователи использовали продвинутую масс-спектрометрию, чтобы каталогизировать эти пептидные фрагменты из рубцовой ткани лёгких пациентов с идиопатическим легочным фиброзом и из стандартной мышиной модели фиброза лёгких, индуцированного блеомицином. Они обнаружили, что фиброзные лёгкие представляют гораздо более широкий и отличительный набор пептидов по сравнению со здоровыми лёгкими, при этом многие источники пептидов особенно активны в фибробластах и макрофагах, вовлечённых в ремоделирование ткани.
Компьютеры помогают выбрать наиболее перспективные мишени
Поскольку у каждого человека уникальный набор молекул MHC, и одновременно может отображаться тысячи пептидов, команда создала вычислительный конвейер под названием Fib-SCORE для приоритизации наиболее перспективных пептидных мишеней в мышах. Fib-SCORE фильтровал пептиды по уверенности их детекции, по силе прогнозируемого связывания с MHC, по согласованности появления в фиброзных лёгких и по тому, включены ли соответствующие гены преимущественно в клетках, формирующих рубец. Этот процесс сузил тысячи кандидатов до фокусного шорт-листа. Три пептида — происходящие из белков MAF, APBB2 и TNS3 — выделились благодаря тесной связи с миофибробластами и макрофагами, ассоциированными с фиброзом, как у мышей, так и у людей.
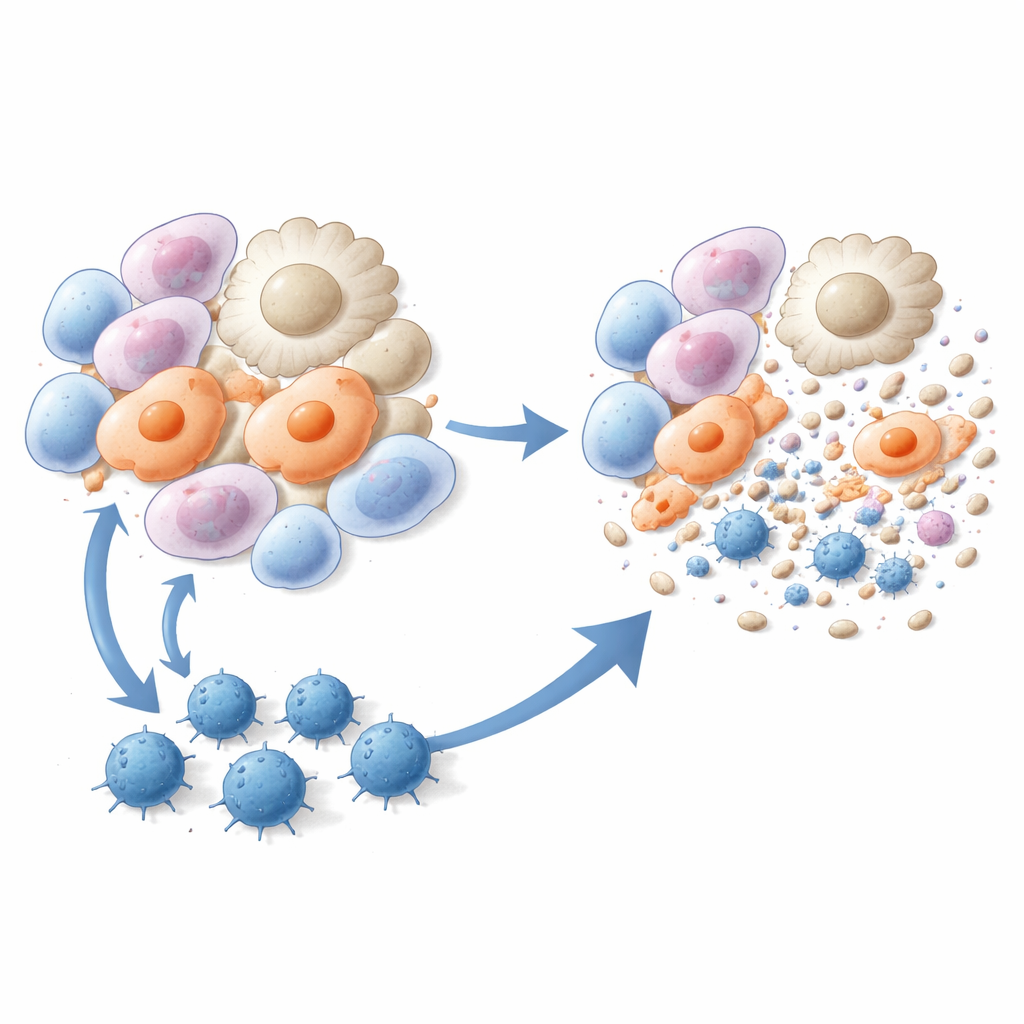
Обучение киллерных T-клеток очищать фиброзные клетки
Исследователи затем превратили эти три пептида в вакцины. Мышам вводили липосомальные инъекции, содержащие один из пептидов плюс иммуномодулирующий компонент, до или вскоре после воздействия блеомицина. По сравнению с необработанными животными у вакцинированных мышей развивалось меньше фиброзных очагов, в лёгких откладывалось меньше коллагена, и структура лёгочной ткани под микроскопом выглядела значительно лучше. Одинарное клеточное секвенирование РНК показало, что две особенно вредные популяции клеток — ассоциированные с рубцом макрофаги и альвеолярные миофибробласты — сильно сокращались после вакцинации. Иммунные тесты подтвердили, что пептидная вакцинация вызвала формирование мощных, пептид-специфичных CD8 T-клеток, которые пролиферировали, продуцировали интерферон-гамма и эффективно уничтожали миофибробласты и профибротические макрофаги in vitro и in vivo.
Ведущий пептид с потенциалом для человека
Среди трёх кандидатов пептид, происходящий из MAF (в исследовании обозначенный как MAF116–124), показал наибольшую общую пользу. У мышей вакцинация этим пептидом изменила лёгочную среду: количество вредных ассоциированных с рубцом клеток уменьшилось, в лёгких накопились CD8-памятные клетки, и киллерные T-клетки наблюдались в непосредственном контакте с миофибробластами, пребывающими в состоянии клеточной гибели. Так как последовательность пептида MAF высоко консервативна между мышами и человеком, команда проверила, может ли он активировать человеческие T-клетки. Используя кровь здоровых доноров с подходящим типом HLA, они получили человеческие цитотоксические T-клетки, специфичные к пептиду MAF. Эти человеческие T-клетки пролиферировали в ответ на клетки, представляющие пептид, и селективно разрушали миофибробласты, полученные от пациентов, и макрофаги типа M2 in vitro, повторяя мышиные результаты.
Что это может означать для будущих методов лечения
Эта работа вводит новую концепцию: использование детальных карт пептидных фрагментов на поверхности фиброзных клеток для разработки вакцин, направляющих киллерные T-клетки против основных двигателей рубцевания. У мышей такие вакцины не только замедляли фиброз — они сокращали рубцовую ткань и истощали клеточные типы, которые её поддерживают. Хотя у исследования есть ограничения, включая небольшое число человеческих образцов и опору на мышиную модель травмы, оно предлагает план преобразования фиброзных заболеваний в состояния, которые можно адресовать прицельной иммунотерапией. Если подобные пептидные вакцины окажутся безопасными и эффективными у людей с идиопатическим легочным фиброзом, они в конечном счёте могут дополнять или даже превосходить существующие лекарства, задействуя способность иммунной системы находить и удалять клетки, превращающие заживление в ущерб.
Цитирование: Bai, Z., Lan, T., Hong, W. et al. Immunopeptidome profiling in pulmonary fibrosis provides a platform for identifying therapeutic targets. Nat Immunol 27, 923–936 (2026). https://doi.org/10.1038/s41590-026-02501-x
Ключевые слова: легочный фиброз, иммунотерапия, пептидная вакцина, CD8 T-клетки, миофибробласты