Clear Sky Science · pl
Profilowanie immunopeptydomu w zwłóknieniu płucnym dostarcza platformy do identyfikacji celów terapeutycznych
Skierowanie układu odpornościowego przeciw bliznom w płucach
Zwłóknienie płuc, a w szczególności idiopatyczne zwłóknienie płuc, to śmiertelna choroba, w której prawidłowa tkanka jest stopniowo zastępowana sztywną blizną. Obecne leki mogą spowalniać ten proces, ale rzadko go zatrzymują, nie mówiąc już o odwróceniu uszkodzeń. W tym badaniu postawiono odważne pytanie: czy można przeszkolić własny układ odpornościowy organizmu, by rozpoznawał i selektywnie usuwał komórki napędzające bliznowacenie, podobnie jak nowoczesne immunoterapie przeciwnowotworowe eliminują komórki nowotworowe?
Dlaczego leczenie bliznowacenia płuc jest tak trudne
Zwłóknienie to problem powszechny: mniej więcej jedna na cztery osoby na świecie rozwija jakąś formę bliznowacenia narządów, a nawet do 45% zgonów w krajach uprzemysłowionych wiąże się z chorobami włókniejącymi. W idiopatycznym zwłóknieniu płuc mikroskopijne uszkodzenia w płucu nigdy nie goją się całkowicie. Zamiast tego wyspecjalizowane komórki zwane miofibroblastami oraz pewne typy makrofagów odkładają nadmierne ilości tkanki łącznej, przekształcając miękkie, napowietrzone płuco w sztywną «plaster miodu» z blizn. Zatwierdzone leki mogą tłumić stan zapalny i spowalniać dalsze uszkodzenia, ale niewiele robią, by usunąć już utrwalone komórki tworzące blizny. Autorzy wysnuli hipotezę, że jeśli ci kluczowi sprawcy eksponują charakterystyczne molekularne «flagowe» znaczniki na swojej powierzchni, układ odpornościowy mógłby zostać nakłoniony do ich rozpoznania i eliminacji.
Odczytywanie ukrytych znaków na chorych komórkach
Każda komórka nieustannie rozkłada własne białka na krótkie fragmenty i prezentuje część z nich na powierzchni przy użyciu cząsteczek MHC klasy I. Te fragmenty tworzą «immunopeptydom», który limfocyty T skanują w poszukiwaniu oznak zagrożenia. Badacze użyli zaawansowanej spektrometrii mas do skatalogowania tych peptydów pochodzących z tkanki płuc zbliznowaciałych u pacjentów z idiopatycznym zwłóknieniem płuc oraz z standardowego modelu mysiego zwłóknienia płuc wywołanego lekiem bleomycyną. Stwierdzili, że płuca z zwłóknieniem prezentują znacznie szerszy i odmienny zestaw peptydów niż zdrowe płuca, przy czym wiele źródeł peptydów jest silnie aktywnych we fibroblastach i makrofagach zaangażowanych w przebudowę tkanki.
Komputery pomagają wybrać najbardziej obiecujące cele
Ponieważ każda osoba ma unikalny zestaw cząsteczek MHC, a jednocześnie na powierzchni mogą być prezentowane tysiące peptydów, zespół opracował pipeline obliczeniowy o nazwie Fib-SCORE, aby priorytetyzować najbardziej obiecujące cele peptydowe u myszy. Fib-SCORE filtrował peptydy według pewności detekcji, siły przewidywanego wiązania z MHC, konsekwencji pojawiania się w płucach z bliznami oraz tego, czy geny źródłowe były aktywowane specyficznie w typach komórek napędzających bliznowacenie. Ten proces skondensował tysiące kandydatów do wąskiej listy. Trzy peptydy — pochodzące z białek MAF, APBB2 i TNS3 — wyróżniały się silnym powiązaniem z miofibroblastami i makrofagami związanymi ze zwłóknieniem zarówno u myszy, jak i u ludzi.
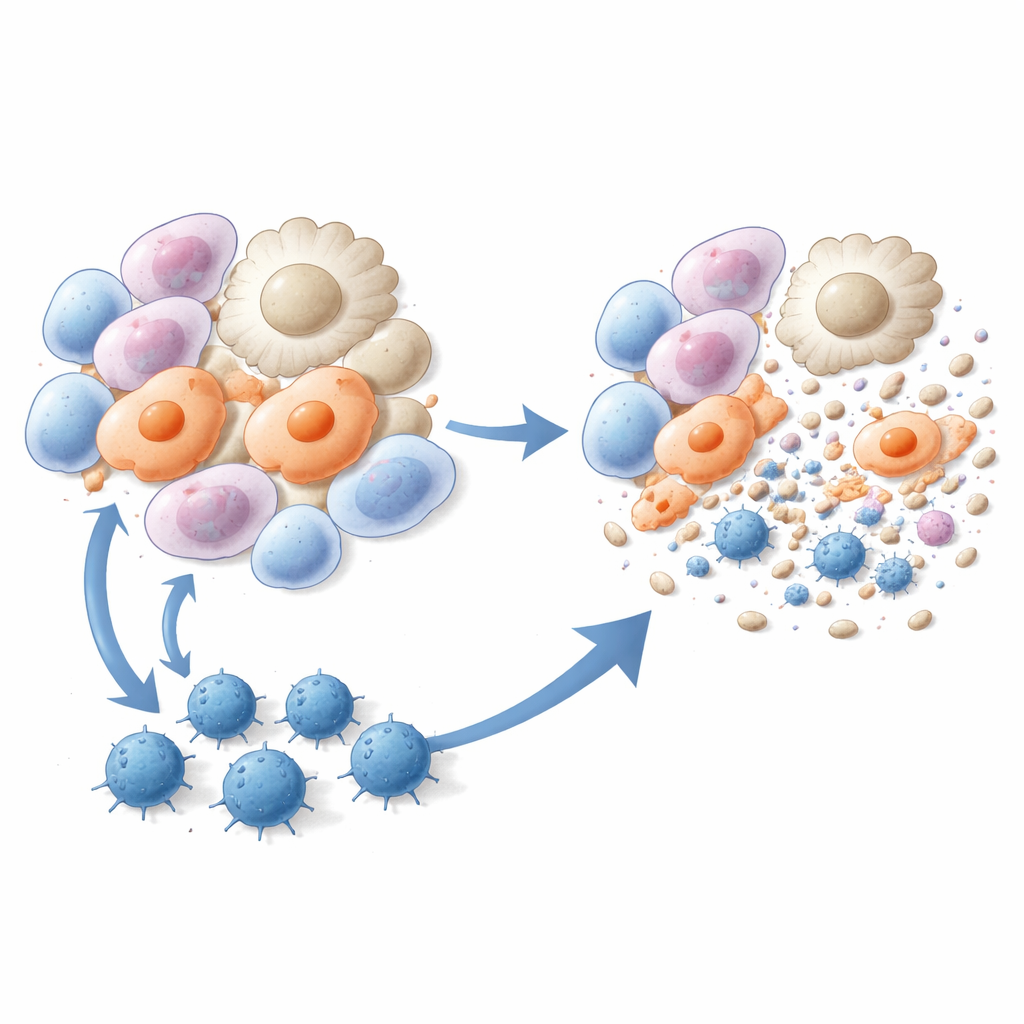
Szkolenie zabójczych limfocytów T do usuwania komórek włókniejących
Następnie badacze przekształcili te trzy peptydy w szczepionki. Myszy otrzymywały iniekcje w formie liposomów zawierające jeden z peptydów oraz składnik wzmacniający odpowiedź immunologiczną, podawane przed lub krótko po ekspozycji na bleomycynę. W porównaniu z nieleczonymi zwierzętami, zaszczepione myszy miały mniej zmian włóknieniowych, mniej odkładanej kolagenu w płucach oraz wyraźnie poprawioną strukturę tkanki płucnej w obrazie mikroskopowym. Sekwencjonowanie RNA pojedynczych komórek wykazało, że dwie szczególnie szkodliwe populacje komórek — makrofagi związane z bliznami i pęcherzykowe miofibroblasty — zostały silnie zredukowane po szczepieniu. Testy immunologiczne potwierdziły, że szczepionki peptydowe wygenerowały silne, peptydowo-specyficzne limfocyty CD8, które proliferowały, wytwarzały interferon-gamma i efektywnie zabijały miofibroblasty oraz prowłóknieniowe makrofagi zarówno in vitro, jak i in vivo.
Wiodący peptyd z potencjałem do zastosowań u ludzi
Wśród trzech kandydatów peptyd pochodzący z MAF (oznaczony w badaniu jako MAF116–124) wykazał najsilniejszy ogólny efekt. U myszy szczepienie tym peptydem przekształciło środowisko płucne: szkodliwe komórki związane z bliznami zmniejszyły swoją liczbę, pamięciowe limfocyty CD8 nagromadziły się w płucach, a zabójcze limfocyty T obserwowano w bezpośrednim kontakcie z miofibroblastami przechodzącymi apoptozę. Ponieważ sekwencja peptydu MAF jest wysoko zachowana między myszami a ludźmi, zespół sprawdził, czy może on również aktywować ludzkie komórki T. Korzystając z krwi od zdrowych dawców posiadających kompatybilny typ HLA, wytworzyli ludzkie cytotoksyczne limfocyty T swoiste dla peptydu MAF. Te ludzkie komórki T proliferowały w odpowiedzi na komórki prezentujące peptyd i selektywnie niszczyły wyizolowane od pacjentów miofibroblasty oraz makrofagi typu M2 in vitro, odzwierciedlając wyniki uzyskane u myszy.
Co to może oznaczać dla przyszłych terapii
Ta praca wprowadza nową koncepcję: wykorzystanie szczegółowych map peptydowych fragmentów prezentowanych na powierzchni komórek włókniejących do projektowania szczepionek, które kierują zabójcze limfocyty T przeciw głównym czynnikom napędzającym bliznowacenie. U myszy takie szczepionki nie tylko spowolniły włóknienie — zmniejszyły tkankę bliznowatą i wyczerpały typy komórek, które ją podtrzymują. Choć badanie ma ograniczenia, w tym niewielką liczbę próbek ludzkich i opieranie się na mysim modelu urazowym, dostarcza planu działania pozwalającego przekształcić choroby włókniejące w schorzenia możliwe do zaatakowania precyzyjną immunoterapią. Jeśli podobne szczepionki peptydowe okażą się bezpieczne i skuteczne u osób z idiopatycznym zwłóknieniem płuc, mogłyby w przyszłości uzupełniać, a być może przewyższać obecne leki, wykorzystując zdolność układu odpornościowego do wyszukiwania i usuwania komórek, które przekształcają proces gojenia w szkodę.
Cytowanie: Bai, Z., Lan, T., Hong, W. et al. Immunopeptidome profiling in pulmonary fibrosis provides a platform for identifying therapeutic targets. Nat Immunol 27, 923–936 (2026). https://doi.org/10.1038/s41590-026-02501-x
Słowa kluczowe: zwłóknienie płuc, immunoterapia, szczepionka peptydowa, limfocyty CD8, mięśniakomiocyty