Clear Sky Science · fr
Profilage de l’immunopéptidome dans la fibrose pulmonaire fournit une plateforme pour identifier des cibles thérapeutiques
Retourner le système immunitaire contre les cicatrices pulmonaires
La fibrose pulmonaire, en particulier la fibrose pulmonaire idiopathique, est une maladie pulmonaire mortelle dans laquelle le tissu normal est progressivement remplacé par une cicatrice rigide. Les traitements actuels peuvent ralentir ce processus mais rarement l’arrêter, et encore moins inverser les dommages. Cette étude pose une question audacieuse : peut‑on entraîner le propre système immunitaire du corps à reconnaître et éliminer sélectivement les cellules qui provoquent la cicatrisation, à l’instar des immunothérapies modernes contre le cancer ?
Pourquoi la cicatrisation pulmonaire est si difficile à traiter
La fibrose n’est pas un problème marginal : environ une personne sur quatre dans le monde développe une forme de cicatrisation d’organe, et jusqu’à 45 % des décès dans les pays industrialisés sont liés à des maladies fibreuses. Dans la fibrose pulmonaire idiopathique, des blessures microscopiques dans le poumon ne se résorbent jamais complètement. À la place, des cellules spécialisées appelées myofibroblastes et certains types de macrophages déposent un excès de tissu conjonctif, transformant un poumon souple et aérien en un réseau rigide de cicatrice. Les médicaments approuvés peuvent atténuer l’inflammation et ralentir les dommages supplémentaires, mais font peu pour éliminer les cellules productrices de cicatrice déjà installées. Les auteurs ont émis l’hypothèse que si ces principaux coupables présentent des « drapeaux » moléculaires distinctifs à leur surface, il serait possible de pousser le système immunitaire à les reconnaître et à les éliminer.
Lire les drapeaux cachés des cellules malades
Chaque cellule dégrade en permanence ses protéines internes en courts fragments et expose un sous‑ensemble de ces fragments à sa surface via des molécules appelées CMH de classe I. Ensemble, ces fragments forment un « immunopéptidome » que les cellules T scrutent à la recherche de signes de danger. Les chercheurs ont utilisé la spectrométrie de masse avancée pour cataloguer ces fragments peptidiques à partir de tissus pulmonaires cicatriciels de patients atteints de fibrose pulmonaire idiopathique et d’un modèle murin standard de fibrose pulmonaire induite par la bléomycine. Ils ont constaté que les poumons fibreux présentent un ensemble de peptides beaucoup plus large et distinct de celui des poumons sains, avec de nombreuses sources peptidiques fortement actives dans les fibroblastes et les macrophages impliqués dans le remodelage tissulaire.
Des ordinateurs pour sélectionner les cibles les plus prometteuses
Parce que chaque personne porte un mélange unique de molécules CMH et que des milliers de peptides peuvent être présentés simultanément, l’équipe a construit un pipeline computationnel nommé Fib‑SCORE pour prioriser les cibles peptidiques les plus prometteuses chez la souris. Fib‑SCORE a filtré les peptides selon la confiance de détection, la force prédite de liaison au CMH, la fréquence d’apparition dans les poumons fibreux et si les gènes sources étaient activés spécifiquement dans les types cellulaires responsables de la cicatrisation. Ce processus a réduit des milliers de candidats à une courte liste ciblée. Trois peptides — dérivés des protéines MAF, APBB2 et TNS3 — se sont distingués par leur lien étroit avec les myofibroblastes et les macrophages associés à la fibrose, tant chez la souris que chez l’humain.
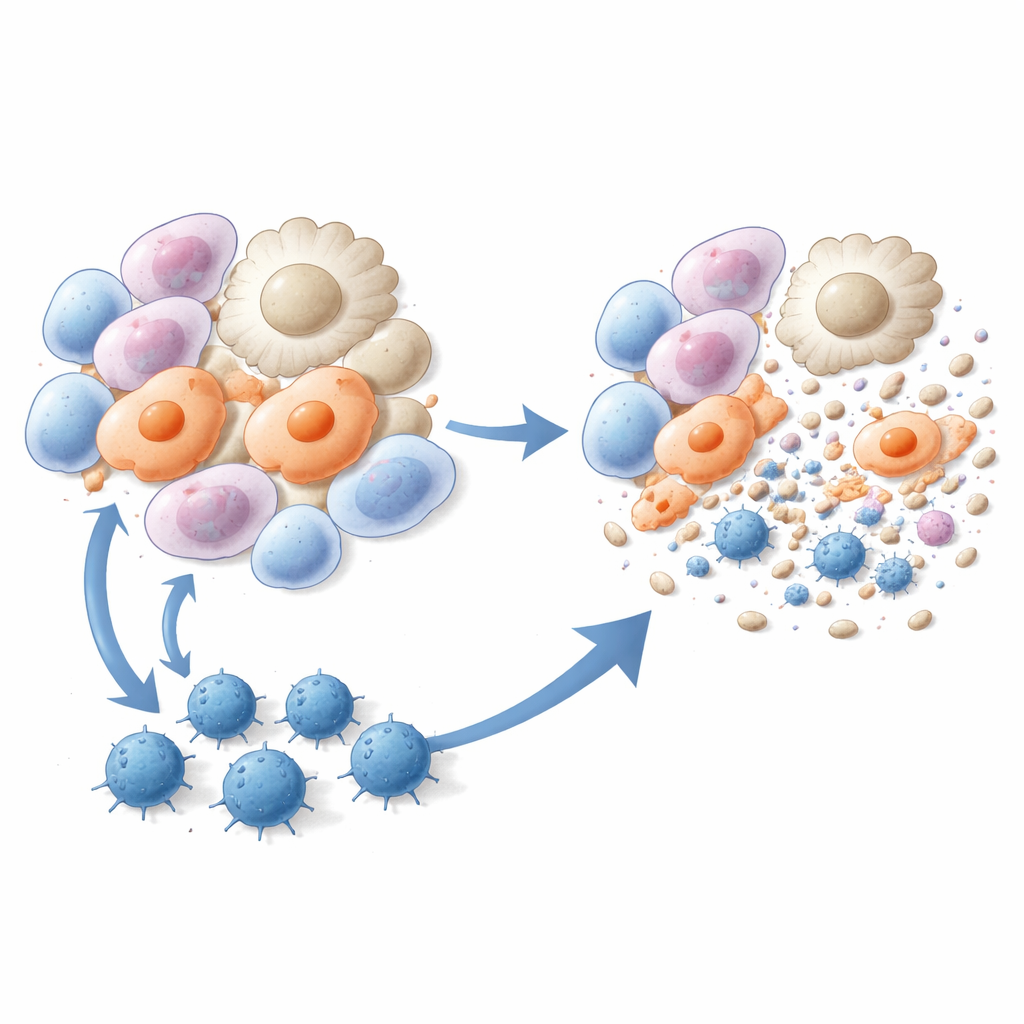
Entraîner des cellules T tueuses à éliminer les cellules fibreuses
Les chercheurs ont ensuite transformé ces trois peptides en vaccins. Des souris ont reçu des injections à base de liposomes contenant l’un des peptides plus un adjuvant immunostimulant, soit avant, soit peu après l’exposition à la bléomycine. Par rapport aux animaux non traités, les souris vaccinées ont développé moins de lésions fibreuses, ont présenté moins de collagène déposé dans le poumon et ont montré une structure tissulaire pulmonaire nettement améliorée au microscope. Le séquençage ARN unicellulaire a révélé que deux populations cellulaires particulièrement nocives — les macrophages associés à la cicatrice et les myofibroblastes alvéolaires — ont été fortement réduites après vaccination. Des tests immunitaires ont confirmé que la vaccination peptidique générait des cellules T CD8 robustes et spécifiques du peptide qui proliféraient, produisaient de l’interféron‑gamma et tuaient efficacement les myofibroblastes et les macrophages pro‑fibrotiques en culture et chez l’animal vivant.
Un peptide principal avec un potentiel humain
Parmi les trois candidats, le peptide dérivé de MAF (appelé MAF116–124 dans l’étude) a montré le bénéfice le plus net. Chez la souris, la vaccination avec ce peptide a remodelé l’environnement pulmonaire : le nombre de cellules nocives associées à la cicatrice a diminué, des cellules T CD8 mémoire se sont accumulées dans le poumon, et des cellules T tueuses ont été observées en contact direct avec des myofibroblastes en train de mourir. Parce que la séquence du peptide MAF est fortement conservée entre la souris et l’homme, l’équipe a testé sa capacité à activer des cellules T humaines. À partir du sang de donneurs sains porteurs d’un type HLA compatible, ils ont généré des cellules T cytotoxiques humaines spécifiques du peptide MAF. Ces cellules T humaines ont proliféré en réponse à des cellules présentant le peptide et ont détruit sélectivement, in vitro, des myofibroblastes dérivés de patients et des macrophages de type M2, reflétant les résultats murins.
Ce que cela pourrait signifier pour les traitements futurs
Cet travail introduit un concept nouveau : utiliser des cartes détaillées des fragments peptidiques à la surface des cellules fibreuses pour concevoir des vaccins qui dirigent les cellules T tueuses contre les principaux moteurs de la cicatrisation. Chez la souris, de tels vaccins n’ont pas seulement ralenti la fibrose — ils ont réduit le tissu cicatriciel et épuisé les types cellulaires qui le maintiennent. Bien que l’étude présente des limites, notamment le faible nombre d’échantillons humains et la dépendance à un modèle murin de lésion, elle offre un plan pour transformer les maladies fibreuses en affections susceptibles d’être ciblées par une immunothérapie de précision. Si des vaccins peptidiques similaires s’avèrent sûrs et efficaces chez des personnes atteintes de fibrose pulmonaire idiopathique, ils pourraient éventuellement compléter ou même surpasser les traitements actuels en mobilisant la capacité du système immunitaire à repérer et éliminer les cellules qui transforment la réparation en dommage.
Citation: Bai, Z., Lan, T., Hong, W. et al. Immunopeptidome profiling in pulmonary fibrosis provides a platform for identifying therapeutic targets. Nat Immunol 27, 923–936 (2026). https://doi.org/10.1038/s41590-026-02501-x
Mots-clés: fibrose pulmonaire, immunothérapie, vaccin peptidique, cellules T CD8, myofibroblastes