Clear Sky Science · sv
Immunopeptidomprofilering vid lungsarkom ger en plattform för att identifiera terapeutiska mål
Att vända immunförsvaret mot lungsår
Pulmonell fibros, särskilt idiopatisk pulmonell fibros, är en dödlig lungsjukdom där normalt vävnad gradvis ersätts av stel ärrvävnad. Nuvarande läkemedel kan bromsa denna process men sällan stoppa den, än mindre vända skadan. Denna studie ställer en djärv fråga: kan vi träna kroppens eget immunförsvar att känna igen och selektivt avlägsna de celler som driver ärrbildning, på samma sätt som moderna cancerimmunterapier gör mot tumörer?
Varför lungsår är så svåra att behandla
Fibros är inte ett nischproblem: ungefär en av fyra människor globalt utvecklar någon form av organfibros, och upp till 45 % av dödsfallen i industrialiserade länder är kopplade till fibrotisk sjukdom. Vid idiopatisk pulmonell fibros läker mikroskopiska skador i lungan aldrig helt. Istället avsätter specialiserade celler kallade myofibroblaster och vissa typer av makrofager överdriven bindväv och förvandlar den mjuka, luftfyllda lungan till en stel, honungsliknande struktur av ärr. Godkända läkemedel kan dämpa inflammation och bromsa fortsatt skada, men de gör lite för att avlägsna de redan etablerade ärrbildande cellerna. Författarna antog att om dessa nyckelaktörer visar utmärkande molekylära “flaggor” på sin yta, så skulle immunförsvaret kunna lockas att känna igen och eliminera dem.
Läsa de dolda flaggorna på sjuka celler
Varje cell bryter ständigt ner sina interna proteiner till korta fragment och visar en delmängd av dessa fragment på sin yta med hjälp av molekyler kallade MHC klass I. Tillsammans bildar dessa fragment ett “immunopeptidom” som T‑celler skannar efter tecken på fara. Forskarna använde avancerad masspektrometri för att kartlägga dessa peptidfragment från ärrad lungvävnad hos patienter med idiopatisk pulmonell fibros och från en standard musmodell av lungsfibros inducerad med läkemedlet bleomycin. De fann att fibrotiska lungor presenterar ett mycket bredare och distinkt uppsättning peptider än friska lungor, med många peptidkällor som är mycket aktiva i fibroblaster och makrofager involverade i vävnadsombyggnad.
Datorer hjälper till att välja de mest lovande målen
Eftersom varje person bär en unik blandning av MHC‑molekyler och tusentals peptider kan visas samtidigt, byggde teamet ett beräkningsrörledningsverktyg kallat Fib‑SCORE för att prioritera de mest lovande peptidmålen i möss. Fib‑SCORE filtrerade peptider efter hur säkert de upptäcktes, hur starkt de förutspåddes binda MHC, hur konsekvent de förekom i fibrotiska lungor och om deras kängen var aktiverade specifikt i de ärrdrivande celltyperna. Denna process destillerade tusentals kandidater till en fokuserad kortlista. Tre peptider—härledda från proteinerna MAF, APBB2 och TNS3—stod ut för att vara starkt kopplade till fibrosassocierade myofibroblaster och makrofager i både mus‑ och människolungor.
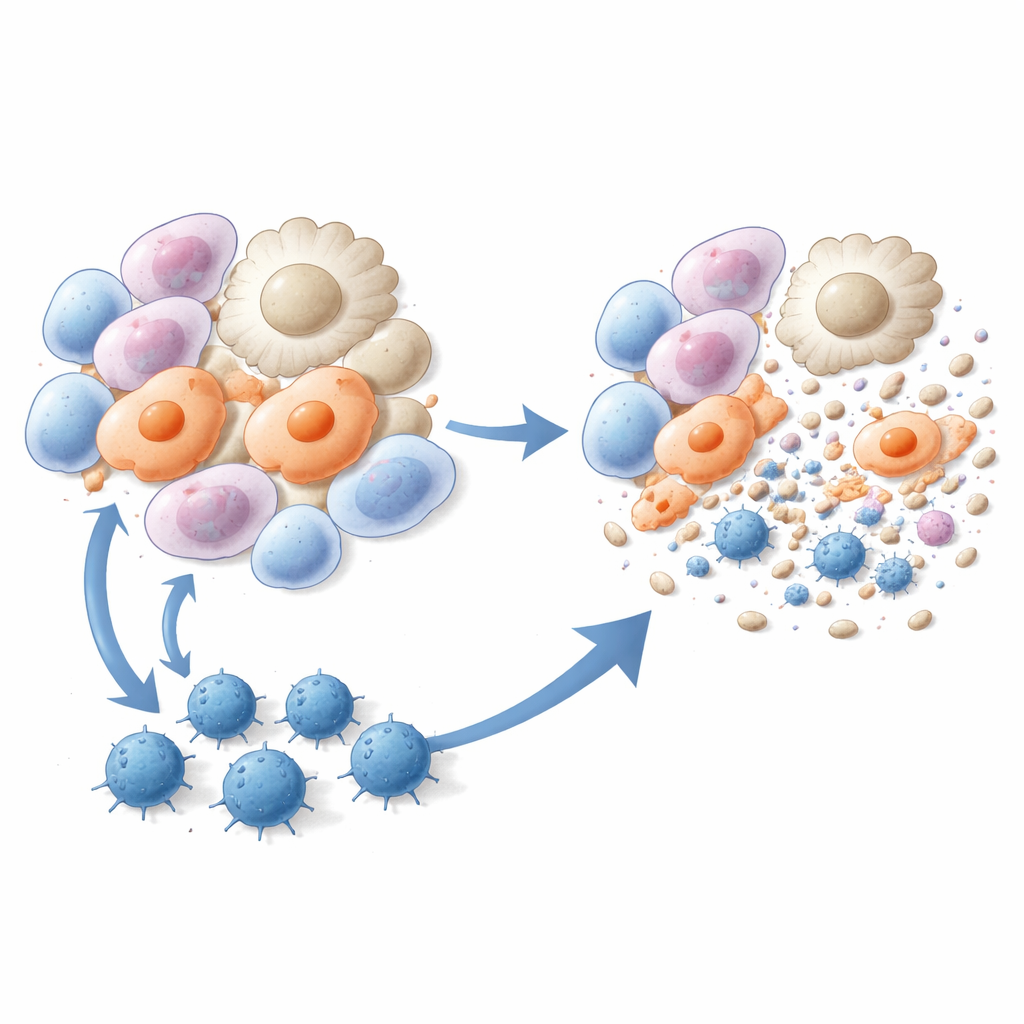
Träna mördande T‑celler att rensa fibrotiska celler
Forskarna gjorde sedan dessa tre peptider till vaccin. Möss gavs liposombaserade injektioner som innehöll en av peptiderna plus en immunförstärkande ingrediens, antingen före eller kort efter bleomycinexponering. Jämfört med obehandlade djur utvecklade vaccinerade möss färre fibrotiska lesioner, hade mindre kollagen deponerat i lungan och visade markant förbättrad lungvävnadsstruktur i mikroskopet. Enkelcells‑RNA‑sekvensering avslöjade att två särskilt skadliga cellpopulationer—ärrassocierade makrofager och alveolära myofibroblaster—var starkt reducerade efter vaccination. Immuntester bekräftade att peptidvaccination genererade robusta, peptidspecifika CD8 T‑celler som prolifererade, producerade interferon‑gamma och effektivt dödade myofibroblaster och profibrotiska makrofager i odling och i levande djur.
En ledande peptid med mänsklig potential
Bland de tre kandidaterna visade MAF‑härledda peptiden (kallad MAF116–124 i studien) den starkaste övergripande nyttan. I möss förändrade vaccination med denna peptid lungmiljön: skadliga ärrassocierade celler minskade i antal, minnes‑CD8 T‑celler ackumulerades i lungan, och mördande T‑celler sågs i direkt kontakt med myofibroblaster som genomgick celldöd. Eftersom MAF‑peptidens sekvens är högt bevarad mellan möss och människor testade teamet om den också kunde aktivera mänskliga T‑celler. Med blod från friska givare som bar en kompatibel HLA‑typ genererade de mänskliga cytotoxiska T‑celler specifika för MAF‑peptiden. Dessa mänskliga T‑celler prolifererade som svar på peptidpresenterande celler och förstörde selektivt patient‑härledda myofibroblaster och M2‑liknande makrofager in vitro, vilket speglade muskresultaten.
Vad detta kan innebära för framtida behandlingar
Detta arbete introducerar ett nytt koncept: att använda detaljerade kartor över peptidfragment på ytan av fibrotiska celler för att designa vaccin som riktar mördande T‑celler mot huvudaktörerna i ärrbildning. I möss gjorde sådana vaccin inte bara att fibrosen bromsade—de minskade ärrvävnaden och utarmade de celltyper som upprätthöll den. Även om studien har begränsningar, inklusive små mängder mänsklig vävnad och beroende av en musmodell för skada, erbjuder den en ritning för att omvandla fibrotiska sjukdomar till tillstånd som kan angripas med precisionsimmunterapi. Om liknande peptidvaccin visar sig säkra och effektiva hos människor med idiopatisk pulmonell fibros, skulle de så småningom kunna komplettera eller till och med överträffa nuvarande läkemedel genom att utnyttja immunförsvarets förmåga att söka upp och avlägsna de celler som förvandlar läkning till skada.
Citering: Bai, Z., Lan, T., Hong, W. et al. Immunopeptidome profiling in pulmonary fibrosis provides a platform for identifying therapeutic targets. Nat Immunol 27, 923–936 (2026). https://doi.org/10.1038/s41590-026-02501-x
Nyckelord: lungsarkom, immunterapi, peptidvaccin, CD8 T‑celler, myofibroblaster