Clear Sky Science · he
פרופיילינג של אימונופפטידום בפיברוזיס ריאתי מספק פלטפורמה לזיהוי מטרות טיפוליות
לכוון את המערכת החיסונית כנגד צלקות בריאה
פיברוזיס ריאתי, ובפרט פיברוזיס ריאתי אידיופתי, הוא מחלה ריאתית קטלנית שבה רקמה רגילה מוחלפת בהדרגה בצלקת נוקשה. התרופות הקיימות יכולות להאט תהליך זה אך נדיר שהן עוצרות אותו, שלא לדבר על היפוך הנזק. המחקר הזה שואל שאלה נועזת: האם אפשר לאמן את המערכת החיסונית של הגוף לזהות ולהסיר באופן סלקטיבי את התאים שמניעים את היווצרות הצלקת, באופן דומה לאימונותרפיות מודרניות נגד סרטן?
למה צלקות בריאה כל כך קשה לטיפול
פיברוזיס אינו בעיה שולית: כ־25% מהאנושות מפתחים צורת צלקת באיבר מסוים, ועד 45% מהתמותות במדינות המפותחות מקושרות למחלות פיברוטיות. בפיברוזיס ריאתי אידיופטי, פצעים מיקרוסקופיים בריאה לעולם לא מחלימים לחלוטין. במקום זאת, תאים מיוחדים הנקראים מייאופיברובלסטים וסוגים מסוימים של מקרופאגים מטילים רקמת חיבור עודפת, והופכים ריאה רכה ומלאת אוויר לחללית צלקת נוקשה בדומה לכוורת. תרופות מאושרות יכולות להשקיט דלקת ולהאט נזק נוסף, אך הן עושות מעט כדי להסיר את תאי יוצרי הצלקת המעוגנים שכבר קיימים. המחברים ניחשו שאם התועמים הללו מציגים "דגלים" מולקולריים מובחנים על פני השטח שלהם, ניתן יהיה לפתות את המערכת החיסונית לזהות ולהשמידם.
לקרוא את הדגלים הנסתרים על התאים החולים
כל תא מפרק באופן מתמיד את חלבוניו הפנימיים לפסגות קצרות ומציג חלק מהן על פני השטח באמצעות מולקולות מסוג MHC class I. יחד, קטעים אלו יוצרים "אימונופפטידום" שתאי T סורקים כדי לחפש סימני סכנה. החוקרים השתמשו במסת-ספקטרומטריה מתקדמת כדי לרשום קטלג של פפטידים מרקמות ריאה פיברוטיות של חולים עם פיברוזיס ריאתי אידיופטי ומדגם עכבר סטנדרטי של פיברוזיס ריאתי שנגרם על ידי תכשיר הבלאומיצין. הם גילו שריאות פיברוטיות מציגות מערך רחב ושונה בהרבה של פפטידים בהשוואה לריאות בריאות, כאשר מקורות רבים של פפטידים פעילים מאוד בפיברובלסטים ובמקרופאגים המעורבים ברה־מודלינג של רקמה.
מחשבים עוזרים לבחור את המטרות המבטיחות ביותר
מאחר שלכל אדם קומבינציה ייחודית של מולקולות MHC ואלפי פפטידים עלולים להיות מוצגים בו־בזמן, הצוות בנה צינור חישובי בשם Fib-SCORE כדי לתת עדיפות למטרות הפפטיד המבטיחות ביותר בעכברים. Fib-SCORE סינן פפטידים לפי רמת הביטחון בגילוים, חוזק התחזית לקשירת MHC, התאמצותם להופיע בריאות פיברוטיות וכיצד גני המקור שלהם דולקים באופן ספציפי בסוגי התאים שמניעים את הצלקת. התהליך דילל אלפי מועמדים לרשימה ממוקדת. שלושה פפטידים — שמקורם בחלבונים MAF, APBB2 ו־TNS3 — בלטו בהיותם קשורים באופן חזק למייאופיברובלסטים ולמקרופאגים הקשורים לפיברוזיס הן בריאות עכבר והן בריאות אדם.
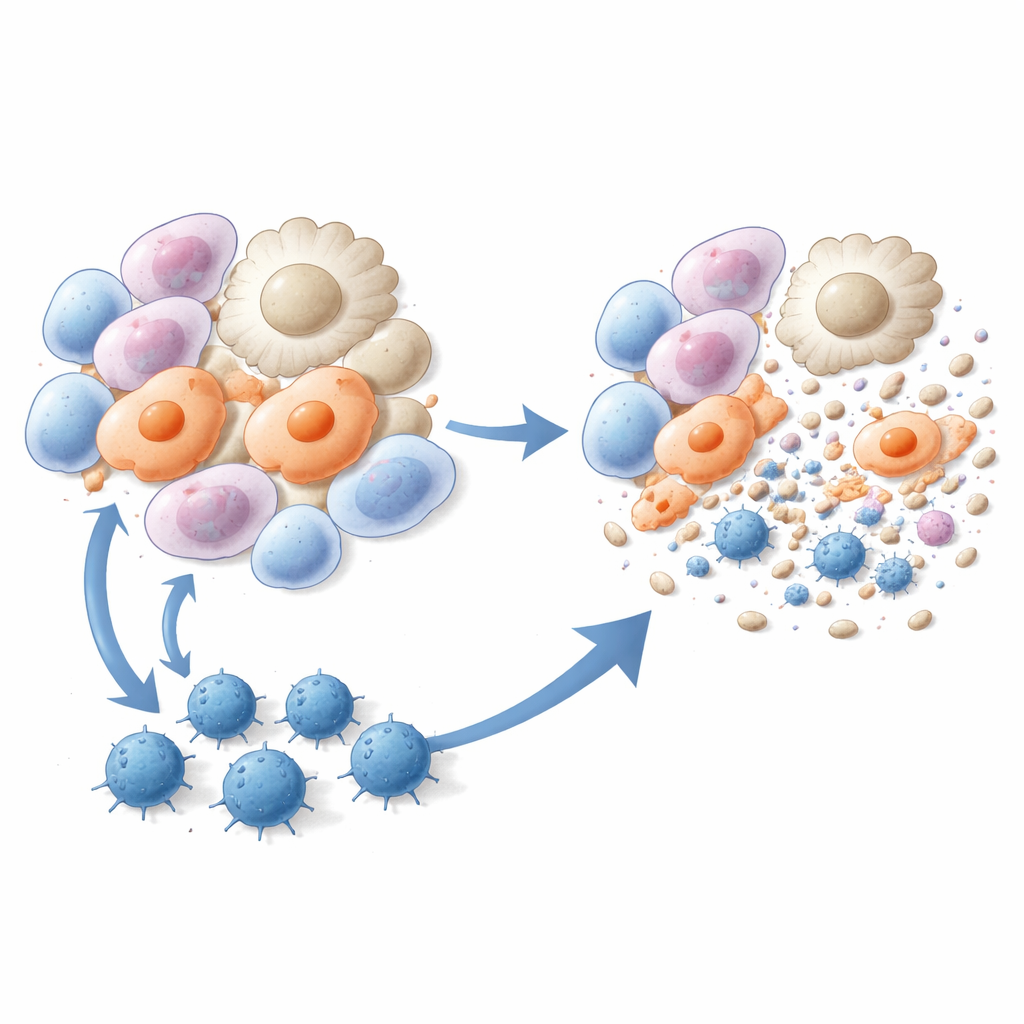
ללמד תאי T קטלניים לנקות תאים פיברוטיים
החוקרים הפכו אחר כך את שלושת הפפטידים הללו לחיסונים. לעכברים הוזרקו חיסונים מבוססי ליפוזומים שכללו אחד מהפפטידים בתוספת מרכיב מחזק חסוני, לפני או זמן קצר אחרי חשיפה לבלאומיצין. בהשוואה לחיות שלא טופלו, עכברים מחוסנים פיתחו פחות מוקדי פיברוזיס, הצטברות הקולגן בריאה היתה מופחתת והמבנה הריאתי תחת המיקרוסקופ השתפר משמעותית. רצף RNA בתא יחיד חשף ששתי אוכלוסיות תאים מזיקות במיוחד — מקרופאגים קשורים לצלקת ומייאופיברובלסטים אלבלאריים — הופחתו בעוצמה לאחר החיסון. בדיקות חיסוניות איששו שחיסון בפפטידים ייצר תאי CD8 ספציפיים לפפטיד שהתרבו, ייצרו אינטרפרון-גאמא והרגו ביעילות מייאופיברובלסטים ומקרופאגים פרו־פיברוטיים בתרבית ובבעלי חיים חיים.
פפטיד מוביל עם פוטנציאל אנושי
מבין שלושת המועמדים, הפפטיד שמקורו ב־MAF (המכונה במחקר MAF116–124) הראה את התועלת הכוללת החזקה ביותר. בעכברים, חיסון עם פפטיד זה עיצב מחדש את המיקרו־סביבה הריאתית: תאי צלקת מזיקים הצטמצמו במספרם, תאי CD8 זכרון הצטברו בריאה ותאי הרג נראו במגע ישיר עם מייאופיברובלסטים שעברו אפופטוזיס. מאחר שסדרת הפפטיד של MAF שמורה מאוד בין עכבר לאדם, הצוות בדק האם היא יכולה גם להפעיל תאי T אנושיים. באמצעות דם מתורמים בריאים הנושאים סוג HLA תואם, הם גידלו תאי T ציטוטוקסיים אנושיים ספציפיים לפפטיד MAF. תאים אנושיים אלה התרבו בתגובה לתאי מציגים את הפפטיד והשמידו באופן סלקטיבי מייאופיברובלסטים מקור-חולה ומקרופאגים דמויי M2 בתרחיש מבחנה, מה שהשקף את התוצאות בעכבר.
מה זה יכול להצביע לגבי טיפולים עתידיים
עבודה זו מציגה רעיון חדש: שימוש במפות מפורטות של קטעי פפטיד על פני שטח תאים פיברוטיים כדי לעצב חיסונים שמכוונים תאי הרג כנגד המניעים העיקריים של היווצרות הצלקת. בעכברים, חיסונים כאלה לא רק האטו פיברוזיס — הם הקטינו את רקמת הצלקת ורוקנו את סוגי התאים שאחראים על תחזוקתה. למרות שמחקר זה מוגבל בכמויות רקמות אנושיות ובתלות במודל פציעה של עכבר, הוא מספק תבנית להפיכת מחלות פיברוטיות למצבים שניתנים למיקוד באמצעות אימונותרפיה מדויקת. אם חיסוני פפטידים דומים יוכחו כבטוחים ויעילים באנשים עם פיברוזיס ריאתי אידיופטי, הם עשויים בסופו של דבר להשלים או אף לעלות על התרופות הנוכחיות על ידי ניצול יכולת המערכת החיסונית לאתר ולהסיר את התאים שהופכים ריפוי לנזק.
ציטוט: Bai, Z., Lan, T., Hong, W. et al. Immunopeptidome profiling in pulmonary fibrosis provides a platform for identifying therapeutic targets. Nat Immunol 27, 923–936 (2026). https://doi.org/10.1038/s41590-026-02501-x
מילות מפתח: פיברוזיס ריאתי, אימונותרפיה, חיסון פפטידי, תאי CD8, מייאופיברובלסטים