Clear Sky Science · nl
Immunopeptidoomprofilering bij longfibrose biedt een platform voor het identificeren van therapeutische doelen
Het immuunsysteem tegen longlittekens keren
Longfibrose, en in het bijzonder idiopathische longfibrose, is een dodelijke longziekte waarbij normaal weefsel langzaam wordt vervangen door stijf littekenweefsel. Huidige geneesmiddelen kunnen dit proces vertragen, maar zelden stoppen en al helemaal niet het bestaande littekenweefsel herstellen. Deze studie stelt een gedurfde vraag: kunnen we het eigen immuunsysteem zo trainen dat het de cellen herkent en selectief verwijdert die littekenvorming aansturen, zoals moderne kankerimmunotherapieën dat doen bij tumoren?
Waarom longlittekens zo moeilijk te behandelen zijn
Fibrose is geen klein probleem: ongeveer één op de vier mensen wereldwijd ontwikkelt enige vorm van orgaanfibrose en tot 45% van de sterfgevallen in geïndustrialiseerde landen hangt samen met fibrotische aandoeningen. Bij idiopathische longfibrose genezen microscopische verwondingen in de long nooit volledig. In plaats daarvan leggen gespecialiseerde cellen, myofibroblasten en bepaalde typen macrofagen, te veel bindweefsel neer, waardoor zachte, luchtige longen veranderen in een stijf, honingraatachtig litteken. Goedgekeurde medicijnen kunnen ontsteking remmen en verdere schade vertragen, maar doen weinig om de al aanwezige, vastzittende littekenvormende cellen te verwijderen. De auteurs redeneerden dat als deze sleutelveroorzakers onderscheidende moleculaire “vlaggen” op hun oppervlak tonen, het immuunsysteem mogelijk kan worden aangezet om ze te herkennen en te elimineren.
De verborgen vlaggen op zieke cellen lezen
Elke cel breekt voortdurend zijn interne eiwitten af in korte fragmenten en presenteert een subset van die fragmenten op het oppervlak met behulp van moleculen die MHC klasse I heten. Samen vormen die fragmenten een “immunopeptidoom” dat T-cellen aftasten op tekenen van gevaar. De onderzoekers gebruikten geavanceerde massaspectrometrie om deze peptiden te catalogiseren uit littekenlongweefsel van patiënten met idiopathische longfibrose en uit een standaard muismodel van longfibrose dat geïnduceerd werd met het medicijn bleomycine. Ze vonden dat gefibrotiseerde longen een veel breder en onderscheidend scala aan peptiden presenteren dan gezonde longen, waarbij veel peptidebronnen sterk actief waren in fibroblasten en macrofagen die betrokken zijn bij weefselherstel.
Computers helpen de meest veelbelovende doelen te kiezen
Aangezien elke persoon een unieke mix van MHC-moleculen draagt en duizenden peptiden tegelijk kunnen worden gepresenteerd, bouwde het team een computationele pijplijn genaamd Fib-SCORE om de meest veelbelovende peptiedoelen in muizen te prioriteren. Fib-SCORE filterde peptiden op basis van hoe betrouwbaar ze werden gedetecteerd, hoe sterk ze werden voorspeld MHC te binden, hoe consistent ze in gefibrotiseerde longen voorkwamen en of hun brongenen specifiek aanstonden in de sleutelceltypes die littekenvorming aandrijven. Dit proces destilleerde duizenden kandidaten tot een gerichte shortlist. Drie peptiden — afkomstig van de eiwitten MAF, APBB2 en TNS3 — vielen op doordat ze sterk gekoppeld waren aan fibrose-geassocieerde myofibroblasten en macrofagen in zowel muis- als mensenlongen.
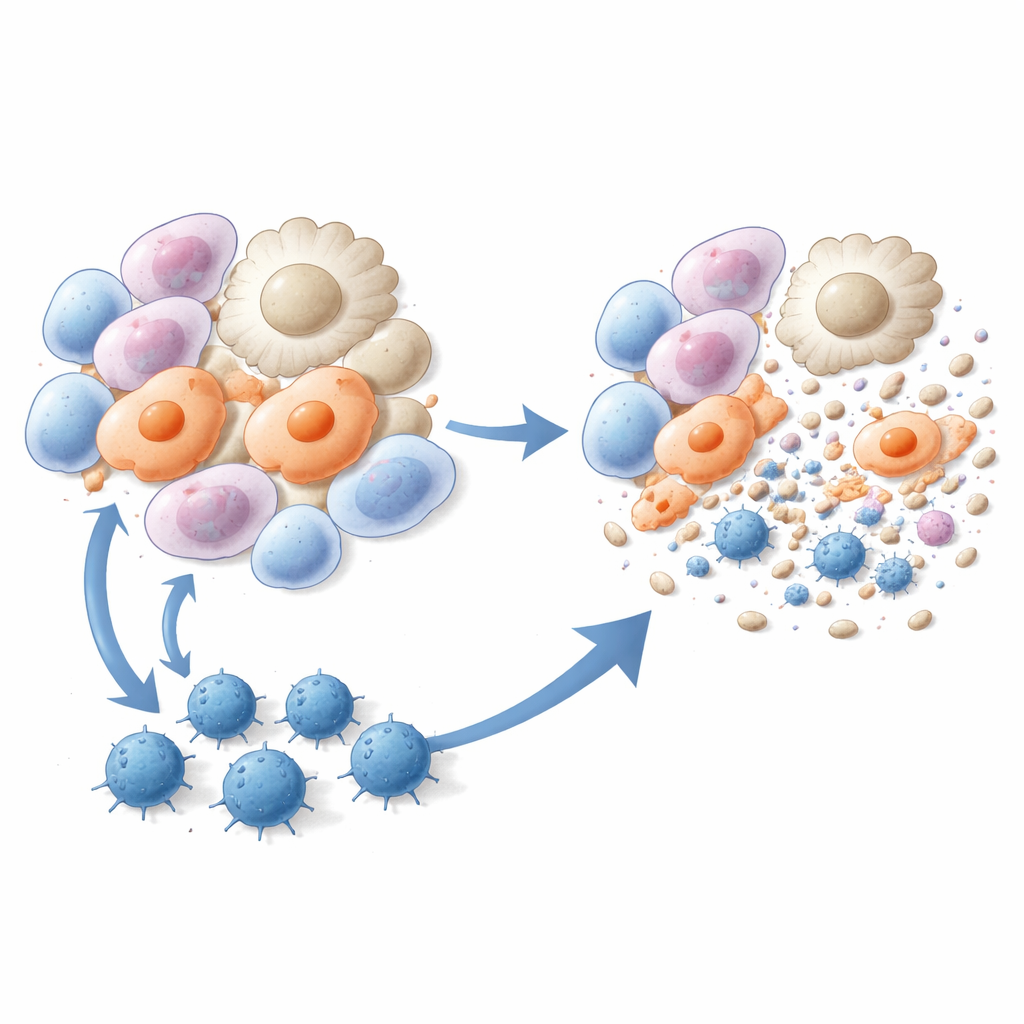
Moordende T-cellen trainen om fibrotische cellen te verwijderen
De onderzoekers zetten deze drie peptiden vervolgens om in vaccins. Muizen kregen liposoom-gebaseerde injecties met één van de peptiden plus een immuunversterkend ingrediënt, zowel vóór als kort na blootstelling aan bleomycine. Vergeleken met onbehandelde dieren ontwikkelden gevaccineerde muizen minder fibrotische laesies, werd er minder collageen in de long afgezet en toonde de longweefselstructuur onder de microscoop duidelijke verbetering. Single-cell RNA-sequencing toonde aan dat twee bijzonder schadelijke celpopulaties — litteken-geassocieerde macrofagen en alveolaire myofibroblasten — sterk verminderd waren na vaccinatie. Immunologische tests bevestigden dat peptidevaccinatie robuuste, peptide-specifieke CD8 T-cellen genereerde die zich vermenigvuldigden, interferon-gamma produceerden en myofibroblasten en pro-fibrotische macrofagen efficiënt in cultuur en in levende dieren doodden.
Een leidend peptide met potentie voor mensen
Van de drie kandidaten toonde het MAF-afgeleide peptide (in de studie MAF116–124 genoemd) het sterkste algemene voordeel. Bij muizen hervormde vaccinatie met dit peptide de longomgeving: schadelijke litteken-geassocieerde cellen namen af, geheugen-CD8 T-cellen stapelden zich op in de long en moordende T-cellen werden gezien in direct contact met myofibroblasten die celdood ondergingen. Omdat de MAF-peptidesequentie sterk geconserveerd is tussen muizen en mensen, testte het team of het ook menselijke T-cellen kon activeren. Met bloed van gezonde donoren met een compatibel HLA-type genereerden ze menselijke cytotoxische T-cellen specifiek voor het MAF-peptide. Deze menselijke T-cellen vermenigvuldigden zich als reactie op peptide-presenterende cellen en vernietigden selectief patiënt-afgeleide myofibroblasten en M2-achtige macrofagen in vitro, waarmee de muisresultaten werden weerspiegeld.
Wat dit kan betekenen voor toekomstige behandelingen
Dit werk introduceert een nieuw concept: het gebruik van gedetailleerde kaarten van peptidefragmenten op het oppervlak van gefibrotiseerde cellen om vaccins te ontwerpen die moordende T-cellen richten tegen de belangrijkste aanjagers van littekenvorming. Bij muizen vertraagden zulke vaccins niet alleen de fibrose — ze verminderden het littekenweefsel en putten de celtypes uit die het in stand houden. Hoewel de studie beperkingen heeft, waaronder een klein aantal menselijke weefsels en het vertrouwen op een muisverwondingsmodel, biedt het een blauwdruk om fibrotische ziekten te transformeren naar aandoeningen die met precisie-immunotherapie kunnen worden aangepakt. Als vergelijkbare peptidevaccins veilig en effectief blijken bij mensen met idiopathische longfibrose, zouden ze uiteindelijk huidige geneesmiddelen kunnen aanvullen of zelfs overtreffen door het immuunsysteem te benutten om de cellen op te sporen en te verwijderen die genezing in schade veranderen.
Bronvermelding: Bai, Z., Lan, T., Hong, W. et al. Immunopeptidome profiling in pulmonary fibrosis provides a platform for identifying therapeutic targets. Nat Immunol 27, 923–936 (2026). https://doi.org/10.1038/s41590-026-02501-x
Trefwoorden: longfibrose, immunotherapie, peptidevaccin, CD8 T-cellen, myofibroblasten