Clear Sky Science · zh
甲硝唑及其醚衍生物通过同时诱导应激与抑制机制靶向幽门螺杆菌
为什么胃部细菌与老药仍然重要
幽门螺杆菌是一种螺旋形细菌,悄然定殖于全球近一半人口的胃中。大多数人并无明显症状,但长期感染可能导致溃疡甚至胃癌。几十年来,医生依赖一种较老的药物甲硝唑来清除这种病菌,然而不断上升的耐药性迫使使用更高剂量和多种药物联合方案——这些方案可能扰乱肠道的有益微生物。本研究提出了一个简单但影响深远的问题:我们能否重新设计这款老药,使其在更低剂量下更强效,并减少对肠道的附带损害?
一种意外强劲的升级药物
研究人员以甲硝唑的核心化学结构为起点,连接了称为醚基的小“把手”,合成了一系列与原药相近的新化合物。在体外对幽门螺杆菌的测试中,部分变体的效力比甲硝唑本身高出多达60倍,在极低浓度即可抑制细菌生长。重要的是,这种效力提升并不只是通过标准的氧化还原化学更容易“激活”药物来实现,表明这些改造分子在细菌细胞内必然起到定性不同的作用。
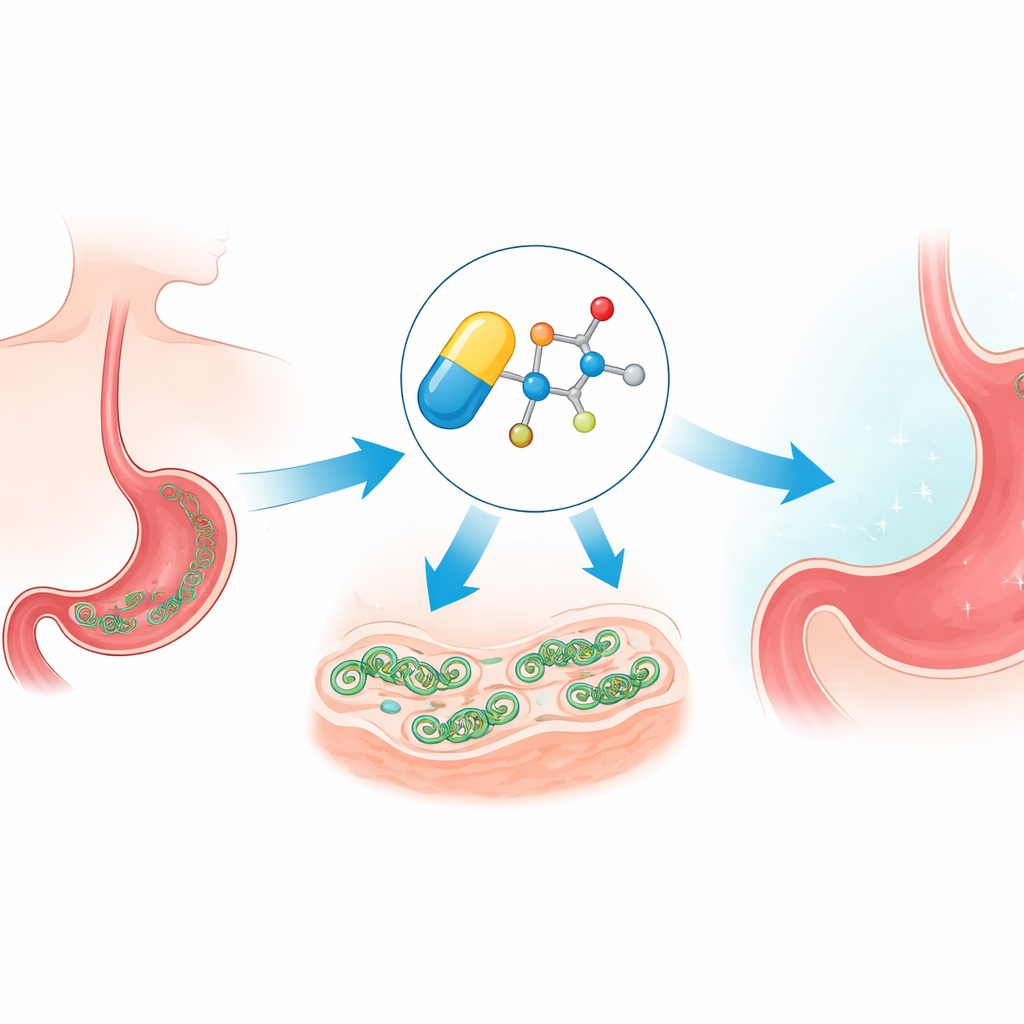
药物如何潜入并使细胞超载
甲硝唑是一种所谓的前药:进入微生物后,其硝基被化学还原生成具攻击性的自由基。这些反应性片段会攻击诸如DNA和蛋白质等重要分子,产生氧化应激。团队证实,新型醚衍生物仍沿此途径产生应激,攻击幽门螺杆菌。但由于这些反应依赖于低氧条件,这些化合物在富氧的人体组织中大多保持不活跃,这也解释了为何该药家族长期对微生物有效同时对患者相对安全。
打击细菌的紧急修复队伍
为探明改造药物的其他作用,科学家们使用了基于活性的蛋白质分析法,这是一种化学“钓鱼”方法,药物样探针可与靶标结合并被拉出鉴定。结果显示幽门螺杆菌中有两类主要蛋白被捕获:一个称为HpGroEL的折叠辅助蛋白,类似分子伴侣负责重新折叠受损蛋白;另一个是名为HpTpx的酶,能中和有害的过氧物并保护DNA免受氧化损伤。醚基化合物尤其强烈地与HpTpx结合,在其活性位点的关键半胱氨酸处形成永久性连接,显著降低了其清除过氧化物的能力。实际上,这些药物既制造氧化混乱,又同时瘫痪细胞的“灭火”队伍。
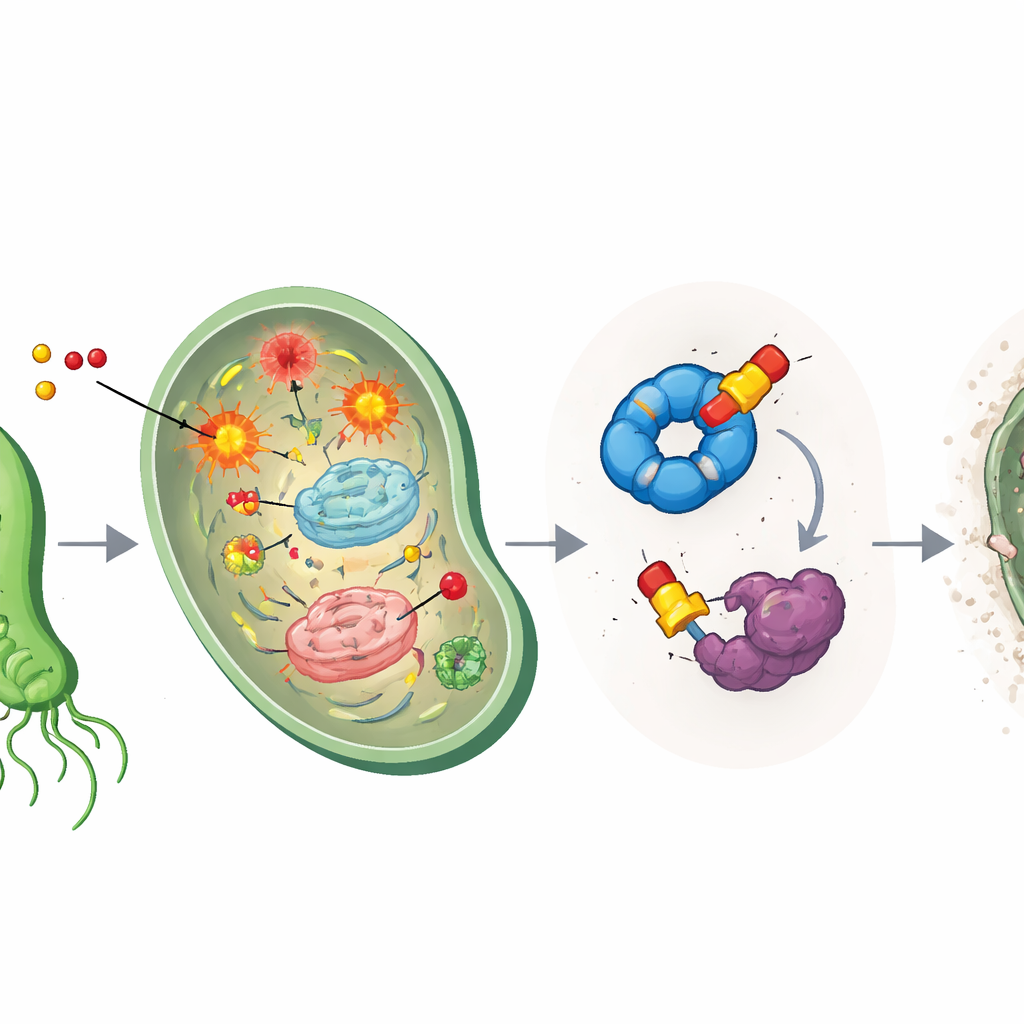
从试管到小鼠胃内的验证
强效抗生素只有在体内表现良好才有用,因此团队考察了新分子的毒性与在动物体内的分布。在人类细胞培养中,这些醚衍生物表现出极低的毒性,化学稳定性测试显示它们在血浆中能较好存活。小鼠药代动力学研究显示了一种表现突出的化合物MF‑01,其在肠道中达到有利浓度并保持良好稳定性。在模拟人类治疗的幽门螺杆菌感染模型中——与克拉霉素和抑酸药物联合使用——MF‑01以约甲硝唑标准剂量的五十分之一剂量完全清除细菌。在如此低剂量下,对正常肠道微生物组的总体影响比传统三联疗法温和,常见的有益小鼠肠道细菌对MF‑01的敏感性也低于对甲硝唑的敏感性。
这对患者与未来药物意味着什么
综上所述,该研究表明甲硝唑及其醚衍生物通过一种强有力的二段击打发挥作用:它们在幽门螺杆菌内诱发氧化应激,同时阻断本可救援细胞的关键应激反应系统。这种双重攻击解释了效力的显著提升,并提示经过精细调整的衍生物可能重振并改良这一老旧抗生素类别。由于这些新分子源于长期获批的药物,它们在安全性评估上已有一定优势。如果后续临床研究证实小鼠中的结果,像MF‑01这样的化合物有望实现更短、更低剂量的方案,更可靠地治愈幽门螺杆菌感染,同时对肠道生态的伤害更小。
引用: Fiedler, M.K., Pandler, M.S.I., Gong, R. et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition. Nat Microbiol 11, 1049–1063 (2026). https://doi.org/10.1038/s41564-026-02291-w
关键词: 幽门螺杆菌, 甲硝唑, 抗生素耐药性, 氧化应激, 肠道微生物组