Clear Sky Science · ru
Метронидазол и его эфирные производные нацеливаются на Helicobacter pylori через одновременное индуцирование стресса и ингибирование
Почему желудочные микробы и старые лекарства все еще важны
Helicobacter pylori — спиралевидная бактерия, которая тихо колонизирует желудки почти половины населения Земли. Большинство людей ничего не чувствует, но длительная инфекция может привести к язвам и даже раку желудка. Врачи десятилетиями полагались на старый препарат метронидазол для борьбы с этой бактерией, однако растущая устойчивость требует более высоких доз и комбинированных схем лечения — режимов, которые могут нарушать дружелюбную микрофлору кишечника. В этом исследовании поставлен простой, но важный вопрос: можно ли переработать этого проверенного временем препарата так, чтобы он сильнее поражал H. pylori при более низких дозах и с меньшим побочным вредом?
Улучшенный препарат с неожиданной мощью
Исследователи взяли за основу химический каркас метронидазола и присоединили к нему небольшие «ручки», называемые эфирными группами, создав серию новых соединений, которые по свойствам близки к исходному лекарству. При испытаниях этих вариантов на H. pylori в лаборатории некоторые из них оказались до 60 раз более активными, чем сам метронидазол, подавляя рост бактерий при крохотных концентрациях. Важно, что такое усиление активности не объяснялось просто повышенной склонностью препарата к стандартной редокс‑химии, что указывает на то, что модифицированные молекулы выполняют внутри бактериальной клетки качественно иные действия.
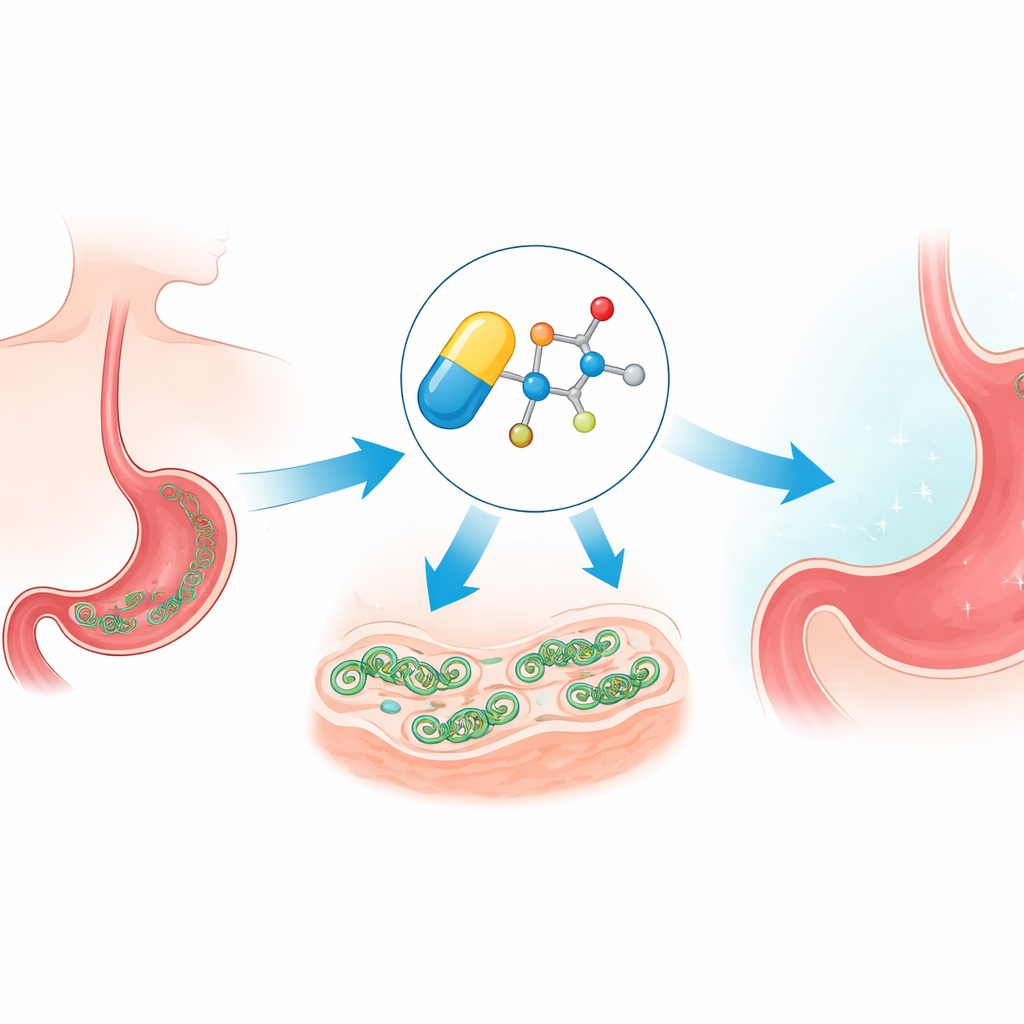
Как препарат проникает и перегружает клетку
Метронидазол — так называемый прозелек: попадая в микроб, его нитрогруппа химически восстанавливается с образованием агрессивных радикальных видов. Эти реактивные фрагменты атакуют жизненно важные молекулы, такие как ДНК и белки, создавая окислительный стресс. Команда подтвердила, что новые эфирные версии по‑прежнему следуют этому пути, вызывая стресс внутри H. pylori. Но поскольку эти реакции зависят от низкого уровня кислорода, соединения остаются в значительной мере неактивными в хорошо оксигенированных тканях человека, что помогает объяснить, почему это семейство препаратов эффективно против микробов и относительно безопасно для пациентов.
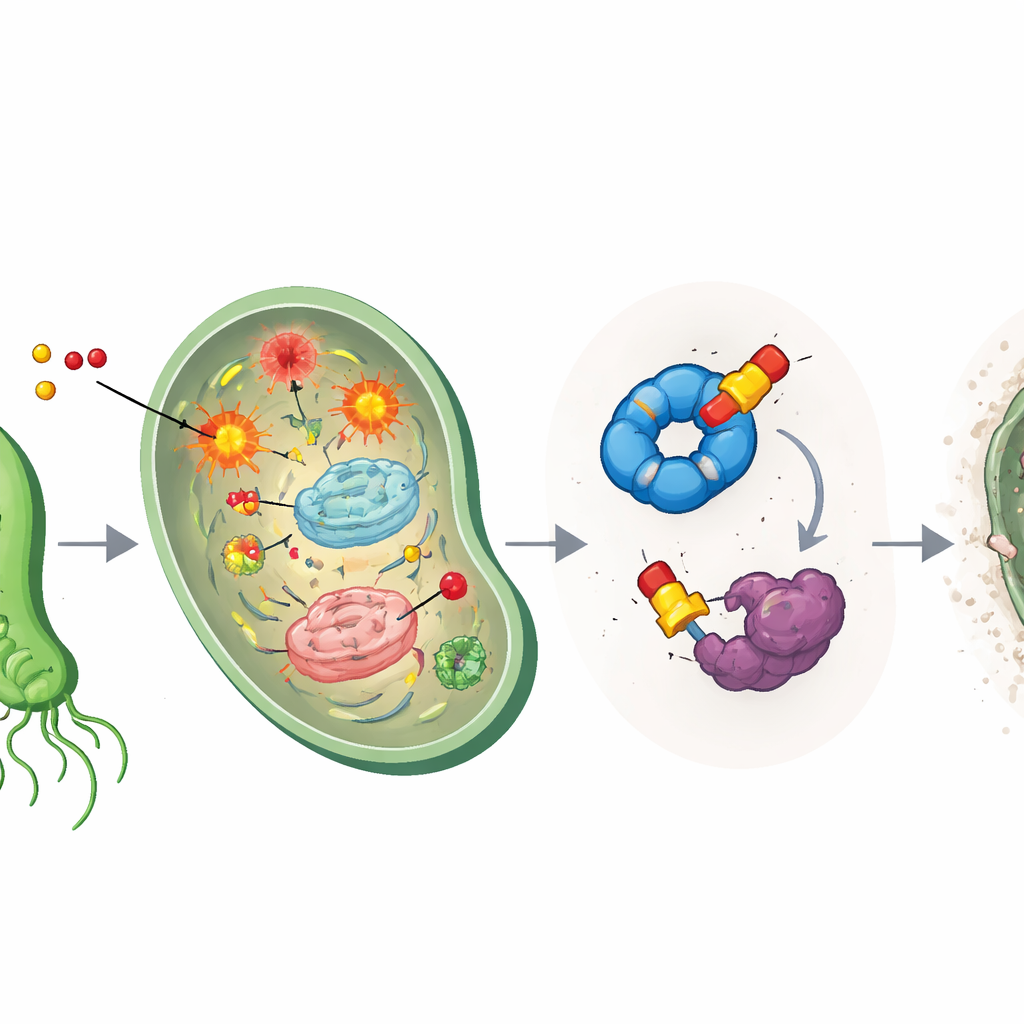
Удар по аварийным ремонтным бригадам бактерии
Чтобы выяснить, чем еще занимаются модифицированные препараты, ученые использовали профилирование активности белков — химический «удочний» метод, при котором зонды, похожие на лекарства, цепляются за свои мишени и затем извлекаются для идентификации. Это выявило две основные «пойманные» белковые мишени в H. pylori: вспомогательный белок сворачивания HpGroEL, который действует как шаперон, помогая реставрировать поврежденные белки, и фермент HpTpx, нейтрализующий пероксиды и защищающий ДНК от окислительного повреждения. Эфирные соединения особенно прочно связывались с HpTpx, образуя постоянные присоединения к критической цистеину в его активном центре и резко снижая его способность детоксифицировать пероксиды. Фактически препараты одновременно создают окислительный хаос и выводят из строя пожарную команду клетки.
От пробирки до желудка мыши
Потенциально мощные антибиотики полезны только если они хорошо ведут себя в организме, поэтому команда изучила токсичность и фармакокинетику новых молекул в животных системах. В культурах человеческих клеток эфирные производные показали очень низкую токсичность, а тесты стабильности указали, что они сохраняются в плазме крови. Фармакокинетические исследования у мышей выделили одно перспективное соединение, MF‑01, которое достигало благоприятных уровней в кишечнике при хорошей стабильности. В модели инфекции H. pylori, имитирующей терапию у человека — в комбинации с кларитромицином и блокатором кислоты желудка — MF‑01 полностью устранял бактерии примерно при одной пятидесятой стандартной дозы метронидазола. При таких низких дозах общее влияние на нормальный микробиом кишечника было мягче, чем при обычной тройной терапии, а типичные полезные бактерии кишечника мышей были менее восприимчивы к MF‑01, чем к метронидазолу.
Что это означает для пациентов и будущих лекарств
В сумме работа показывает, что метронидазол и его эфирные аналоги действуют через мощное «комбо»: они индуцируют окислительный стресс внутри H. pylori и одновременно блокируют ключевые системы ответа на стресс, которые в норме спасают клетку. Эта двойная атака объясняет драматическое повышение активности и позволяет предположить, что тщательно подобранные производные могут реабилитировать и улучшить старый класс антибиотиков. Поскольку новые молекулы развиваются из давно одобренного препарата, у них есть преимущество в виде уже имеющихся данных по безопасности. Если будущие клинические исследования подтвердят результаты у мышей, такие соединения, как MF‑01, могут позволить более короткие схемы с низкими дозами, которые надежнее вылечивают инфекции H. pylori и при этом меньше вредят остальному экосистему кишечника.
Цитирование: Fiedler, M.K., Pandler, M.S.I., Gong, R. et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition. Nat Microbiol 11, 1049–1063 (2026). https://doi.org/10.1038/s41564-026-02291-w
Ключевые слова: Helicobacter pylori, метронидазол, устойчивость к антибиотикам, окислительный стресс, микробиом кишечника