Clear Sky Science · it
Metronidazolo e derivati eterei prendono di mira Helicobacter pylori attraverso induzione simultanea di stress e inibizione
Perché i batteri dello stomaco e i vecchi farmaci sono ancora importanti
Helicobacter pylori è un germe a forma di spirale che colonizza in modo silenzioso lo stomaco di quasi la metà della popolazione mondiale. La maggior parte delle persone non avverte nulla, ma un’infezione prolungata può portare a ulcere e persino al cancro gastrico. Per decenni i medici si sono affidati a un farmaco più datato chiamato metronidazolo per debellare questo batterio, tuttavia l’aumento della resistenza richiede dosi più elevate e cocktail di farmaci — regimi che possono alterare i microrganismi “amici” dell’intestino. Questo studio pone una domanda semplice ma dalle grandi conseguenze: possiamo riprogettare questo vecchio cavallo di battaglia in modo che colpisca H. pylori più efficacemente, a dosi inferiori e con meno danni collaterali?
Un medicinale aggiornato con forza sorprendente
I ricercatori sono partiti dalla struttura chimica di base del metronidazolo e vi hanno collegato piccoli “manici” detti gruppi eterei, creando una serie di nuovi composti che si comportano come stretti parenti del farmaco originale. Quando hanno testato queste varianti contro H. pylori in laboratorio, alcune si sono rivelate fino a 60 volte più potenti del metronidazolo stesso, bloccando la crescita batterica a concentrazioni minime. È importante notare che questo aumento non deriva semplicemente dal rendere il farmaco più facilmente “attivabile” tramite la chimica redox standard, il che suggerisce che le molecole modificate stanno facendo qualcosa di qualitativamente diverso all’interno della cellula batterica.
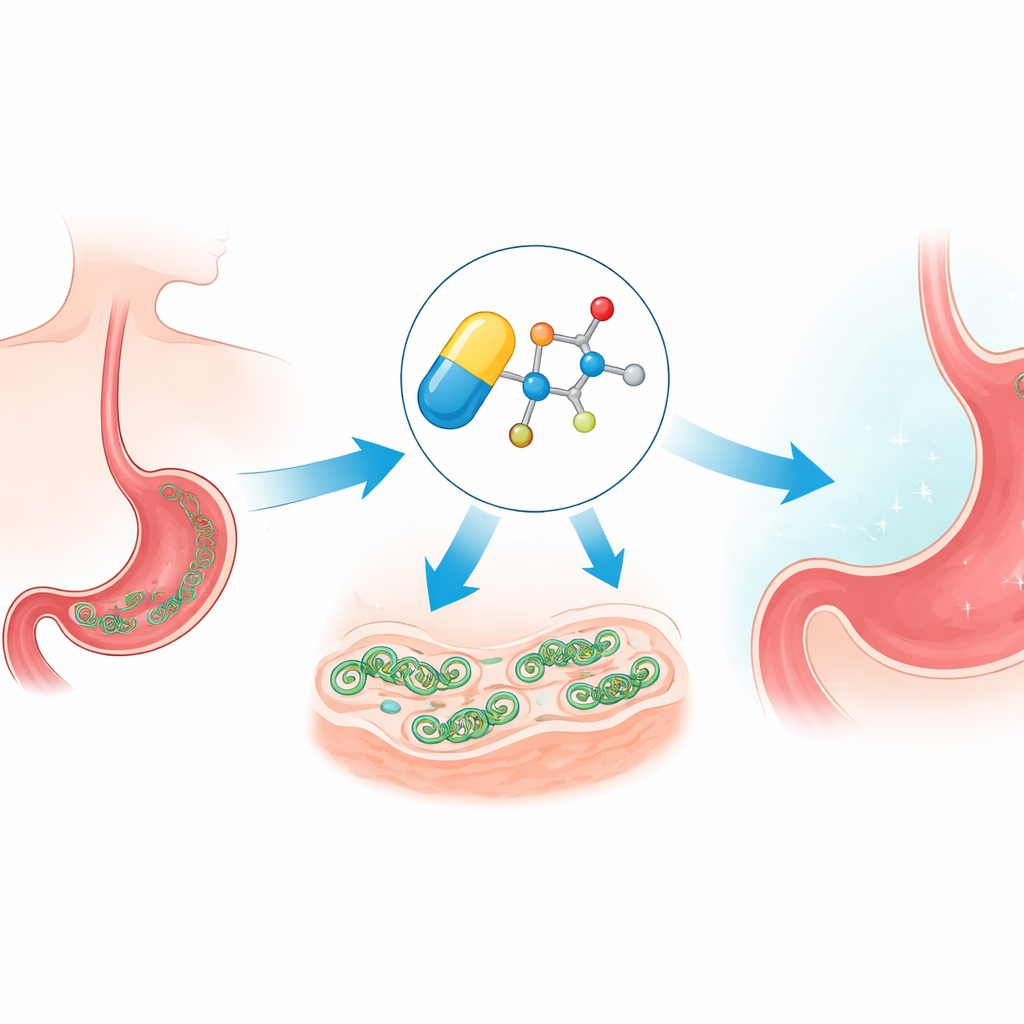
Come il farmaco si insinua e sovraccarica la cellula
Il metronidazolo è un cosiddetto profarmaco: una volta che penetra in un microbo, il suo gruppo nitro viene chimicamente ridotto a formare specie radicaliche aggressive. Questi frammenti reattivi attaccano molecole vitali come il DNA e le proteine, creando stress ossidativo. Il team ha confermato che le nuove versioni eteree seguono ancora questa via, generando stress all’interno di H. pylori. Ma poiché queste reazioni dipendono da condizioni a basso contenuto di ossigeno, i composti rimangono in gran parte inattivi nei tessuti umani ben ossigenati, il che aiuta a spiegare perché questa famiglia di farmaci è stata a lungo utile contro i microbi e relativamente sicura per i pazienti.
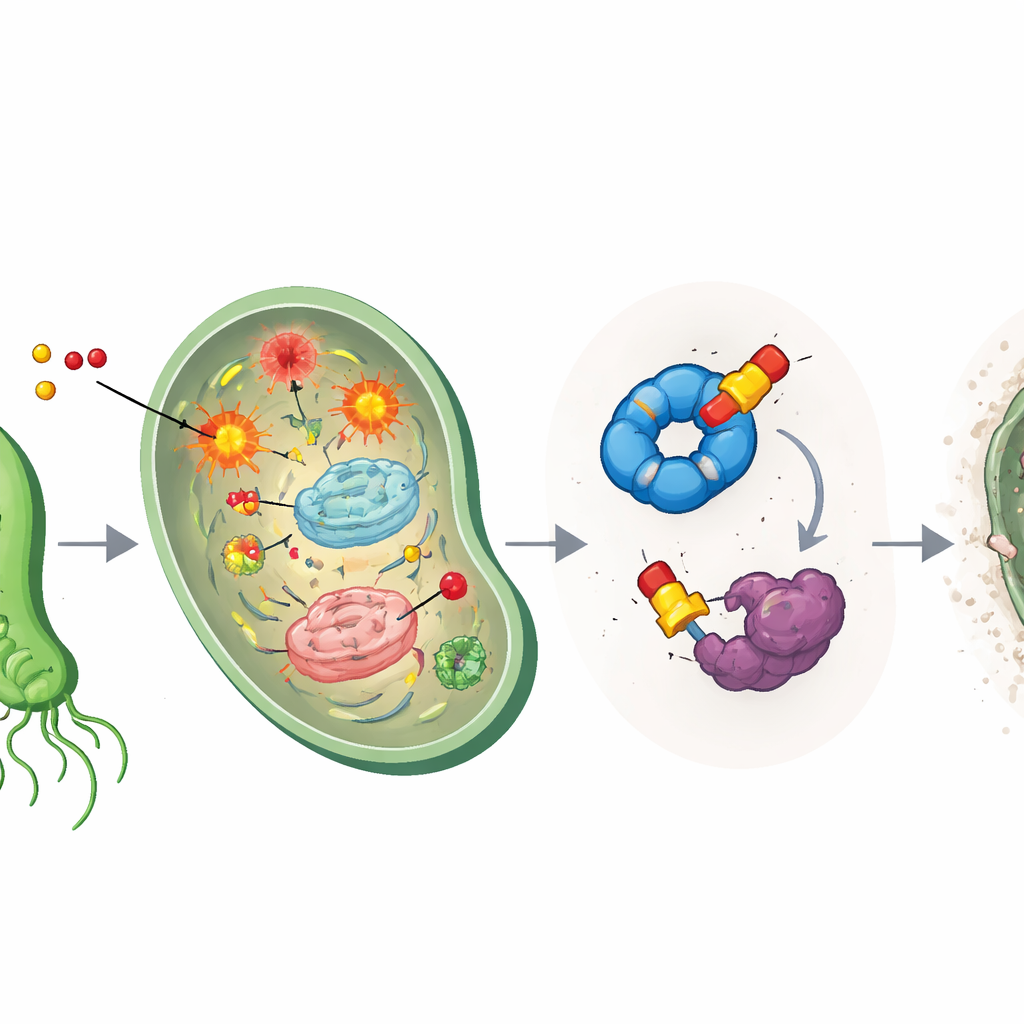
Colpire le squadre di soccorso della cellula
Per capire cos’altro facessero i farmaci modificati, gli scienziati hanno usato il profiling proteico basato sull’attività, un metodo chimico di pesca in cui sonde simili a farmaci si agganciano ai loro bersagli e possono essere estratte e identificate. Questo ha rivelato due principali “prede” proteiche in H. pylori: un aiuto per il ripiegamento chiamato HpGroEL, che agisce come chaperone per ripiegare le proteine danneggiate, e un enzima chiamato HpTpx, che neutralizza perossidi dannosi e protegge il DNA dallo stress ossidativo. I composti a base di etere si legavano in modo particolarmente forte a HpTpx, formando legami permanenti in una cisteina critica nel sito attivo e riducendo nettamente la sua capacità di detossificare i perossidi. In pratica, i farmaci creano caos ossidativo e nel contempo disabilitano la squadra antincendio della cellula.
Dal provetta allo stomaco del topo
Antibiotici potenti sono utili solo se si comportano bene nell’organismo, così il team ha esaminato la tossicità e come le nuove molecole si distribuiscono negli animali. Nelle colture di cellule umane, i derivati eterei hanno mostrato una tossicità molto bassa e i test di stabilità chimica hanno indicato che resistono bene nel plasma sanguigno. Gli studi farmacocinetici nei topi hanno evidenziato un composto di spicco, MF-01, che raggiungeva livelli favorevoli nell’intestino mantenendo buona stabilità. In un modello di infezione da H. pylori che imita il trattamento umano — usando una combinazione con claritromicina e un inibitore dell’acidità gastrica — MF-01 ha eliminato completamente i batteri a circa un cinquantesimo della dose standard di metronidazolo. A tali dosi basse, l’impatto complessivo sul microbioma intestinale normale è stato più lieve rispetto alla convenzionale terapia tripla, e i comuni batteri intestinali benefici nei topi sono risultati meno sensibili a MF-01 che al metronidazolo.
Cosa significa per i pazienti e per i farmaci futuri
Nel complesso, il lavoro mostra che il metronidazolo e i suoi parenti eterei agiscono tramite un potente colpo combinato: scatenano stress ossidativo all’interno di H. pylori mentre bloccano simultaneamente i principali sistemi di risposta allo stress che normalmente salverebbero la cellula. Questo attacco doppio spiega l’aumento drammatico della potenza e suggerisce che derivati opportunamente tarati potrebbero rivitalizzare e migliorare una classe di antibiotici invecchiata. Poiché queste nuove molecole derivano da un farmaco a lungo approvato, partono con un vantaggio nel profilo di sicurezza. Se studi clinici futuri confermeranno i risultati nei topi, composti come MF-01 potrebbero permettere regimi più brevi e a dose più bassa che curano più affidabilmente le infezioni da H. pylori pur risultando più gentili con il resto dell’ecosistema intestinale.
Citazione: Fiedler, M.K., Pandler, M.S.I., Gong, R. et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition. Nat Microbiol 11, 1049–1063 (2026). https://doi.org/10.1038/s41564-026-02291-w
Parole chiave: Helicobacter pylori, metronidazolo, resistenza agli antibiotici, stress ossidativo, microbioma intestinale