Clear Sky Science · fr
Le métronidazole et ses dérivés éthers ciblent Helicobacter pylori via une induction de stress simultanée et une inhibition
Pourquoi les microbes gastriques et les vieux médicaments comptent encore
Helicobacter pylori est un germe en forme de spirale qui colonise discrètement l’estomac de près de la moitié de la population mondiale. La plupart des personnes ne ressentent rien, mais une infection chronique peut conduire à des ulcères et même au cancer gastrique. Depuis des décennies, les médecins s’appuient sur un ancien médicament, le métronidazole, pour éliminer ce germe, mais l’augmentation de la résistance nécessite désormais des doses plus élevées et des cocktails antibiotiques — des schémas susceptibles de perturber les microbes bénéfiques de l’intestin. Cette étude pose une question simple aux conséquences importantes : peut‑on repenser ce vieux cheval de bataille pour frapper H. pylori plus fort, à moindre dose, et avec moins de dommages collatéraux ?
Un médicament amélioré d’une force surprenante
Les chercheurs sont partis du noyau chimique du métronidazole et y ont ajouté de petites « poignées » appelées groupes éthers, créant une série de nouveaux composés qui se comportent comme des cousins proches du médicament d’origine. Lorsqu’ils ont testé ces variantes contre H. pylori en laboratoire, certaines se sont révélées jusqu’à 60 fois plus puissantes que le métronidazole lui‑même, arrêtant la croissance bactérienne à des concentrations infimes. Fait important, ce gain d’efficacité ne s’expliquait pas simplement par une activation plus facile du médicament via la chimie rédox classique, ce qui suggère que les molécules modifiées accomplissent quelque chose de qualitativement différent à l’intérieur de la cellule bactérienne.
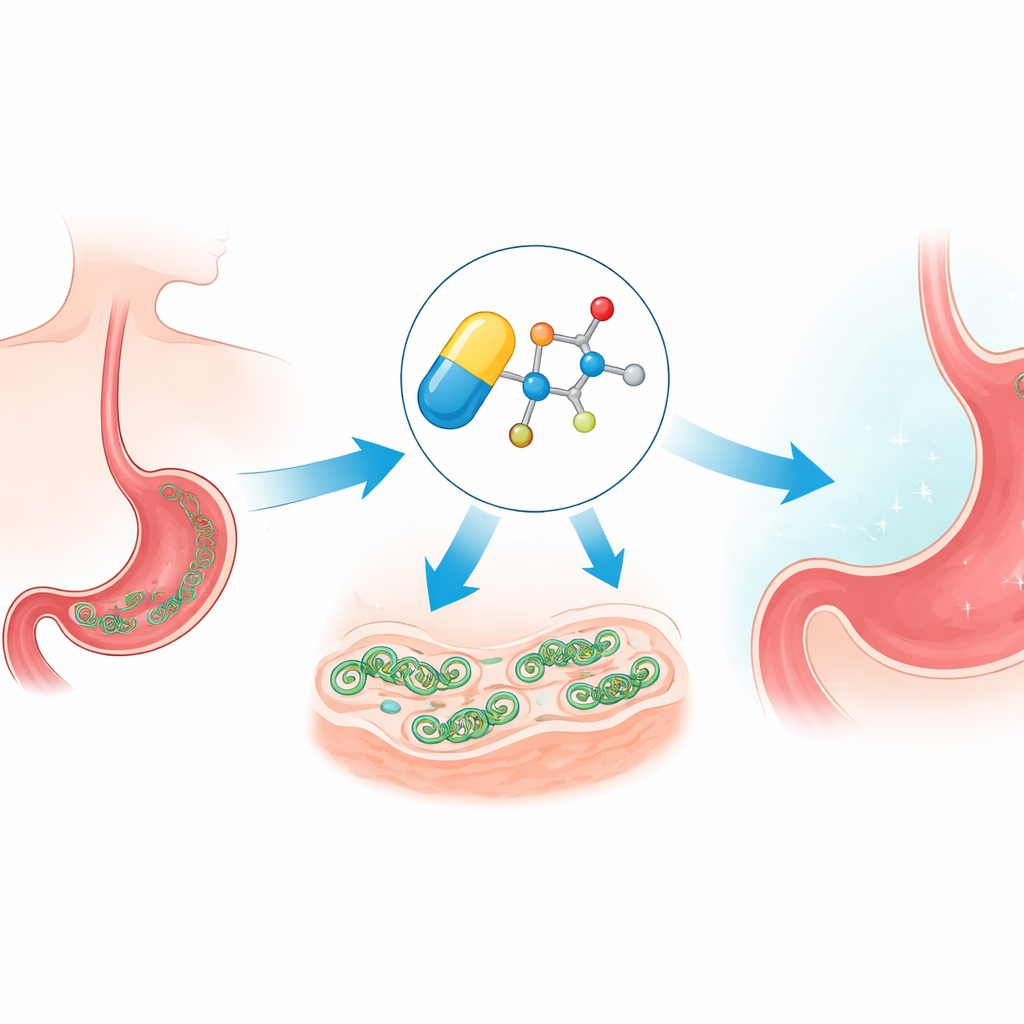
Comment le médicament se faufile et surcharge la cellule
Le métronidazole est un pseudo‑médicament (pro‑médicament) : une fois qu’il pénètre dans un microbe, son groupe nitro est réduit chimiquement pour former des espèces radicalaires agressives. Ces fragments réactifs attaquent des molécules vitales telles que l’ADN et les protéines, générant un stress oxydatif. L’équipe a confirmé que les nouvelles versions éther suivent toujours cette voie, générant du stress au sein de H. pylori. Mais parce que ces réactions dépendent de conditions pauvres en oxygène, les composés restent largement inactifs dans les tissus humains bien oxygénés, ce qui aide à expliquer pourquoi cette famille de médicaments a longtemps été efficace contre les microbes tout en restant relativement sûre pour les patients.
Frapper les équipes de réparation d’urgence du germe
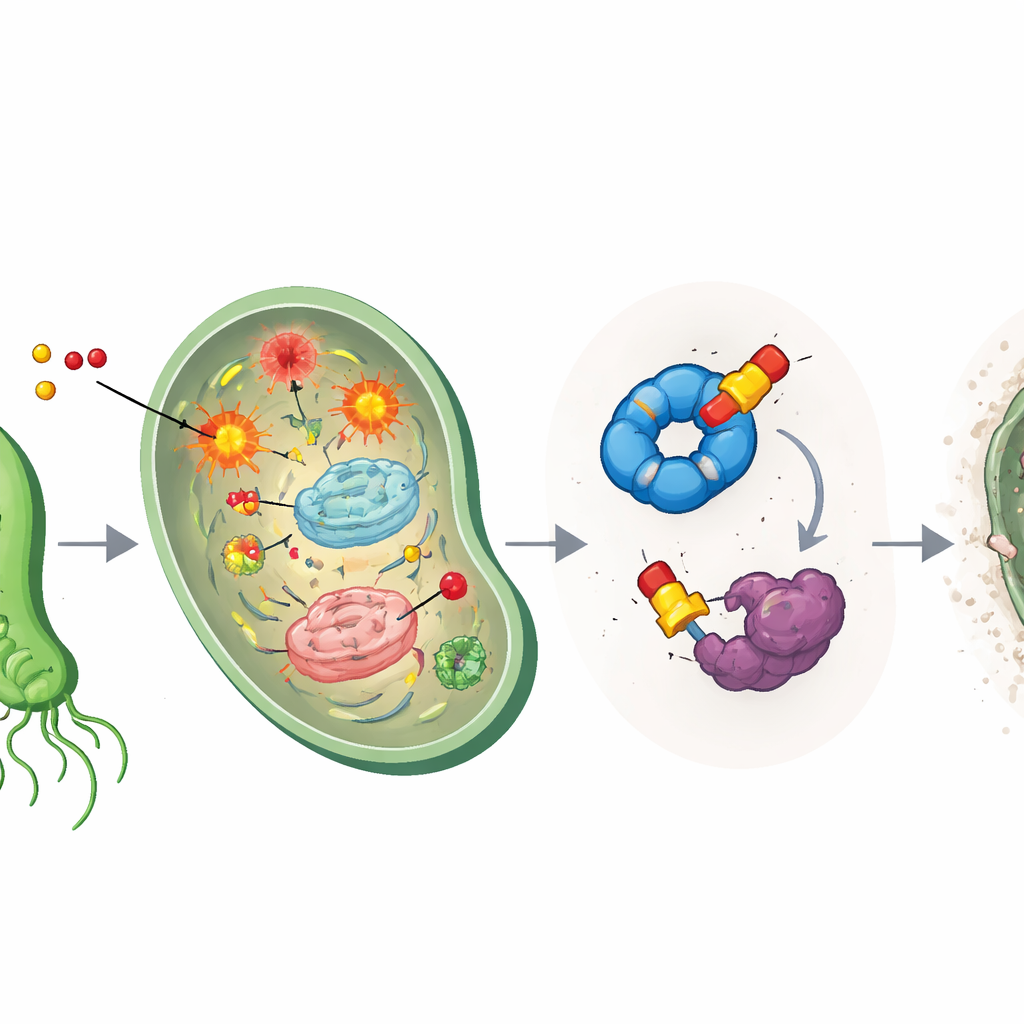
Pour savoir ce que faisaient d’autre les médicaments modifiés, les scientifiques ont utilisé le profilage d’activité des protéines, une méthode chimique d’« appât » où des sondes de type médicament se lient à leurs cibles puis sont isolées et identifiées. Cela a révélé deux principales « prises » protéiques dans H. pylori : une aide au repliement appelée HpGroEL, qui agit comme une chaperonne pour refoldre les protéines endommagées, et une enzyme appelée HpTpx, qui neutralise les peroxydes nocifs et protège l’ADN du stress oxydatif. Les composés à base d’éther se sont liés particulièrement fortement à HpTpx, formant des attachements permanents sur une cystéine critique du site actif et réduisant fortement sa capacité à neutraliser les peroxydes. En pratique, les médicaments créent à la fois le chaos oxydatif et désactivent simultanément les pompiers cellulaires.
Du tube à essai à l’estomac de la souris
Des antibiotiques puissants ne sont utiles que s’ils se comportent bien dans l’organisme, aussi l’équipe a‑t‑elle examiné la toxicité et la pharmacocinétique des nouvelles molécules chez l’animal. Dans des cultures de cellules humaines, les dérivés éther ont montré une toxicité très faible, et des tests de stabilité chimique ont indiqué qu’ils survivaient bien dans le plasma sanguin. Des études pharmacocinétiques chez la souris ont mis en évidence un composé remarquable, MF‑01, qui atteignait des niveaux favorables dans l’intestin tout en conservant une bonne stabilité. Dans un modèle d’infection par H. pylori qui imite le traitement humain — utilisant une combinaison avec la clarithromycine et un bloqueur d’acide gastrique — MF‑01 a éliminé complètement les bactéries à environ un cinquantième de la dose standard de métronidazole. À de telles faibles doses, l’impact global sur le microbiote intestinal normal était moins marqué que celui de la thérapie triple conventionnelle, et les bactéries intestinales bénéfiques courantes chez la souris étaient moins sensibles à MF‑01 qu’au métronidazole.
Ce que cela signifie pour les patients et les médicaments futurs
Dans l’ensemble, le travail montre que le métronidazole et ses proches éthers agissent par un puissant double coup : ils déclenchent un stress oxydatif à l’intérieur de H. pylori tout en bloquant simultanément des systèmes clés de réponse au stress qui sauveraient normalement la cellule. Cette attaque double explique l’augmentation spectaculaire de la puissance et suggère que des dérivés soigneusement ajustés pourraient faire renaître et améliorer une classe d’antibiotiques vieillissante. Comme ces nouvelles molécules proviennent d’un médicament approuvé de longue date, elles partent avec une avance sur le profilage de sécurité. Si de futures études cliniques confirment les résultats chez la souris, des composés comme MF‑01 pourraient permettre des schémas plus courts et à plus faible dose qui guérissent plus sûrement les infections à H. pylori tout en étant plus respectueux du reste de l’écosystème intestinal.
Citation: Fiedler, M.K., Pandler, M.S.I., Gong, R. et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition. Nat Microbiol 11, 1049–1063 (2026). https://doi.org/10.1038/s41564-026-02291-w
Mots-clés: Helicobacter pylori, métronidazole, résistance aux antibiotiques, stress oxydatif, microbiote intestinal