Clear Sky Science · ar
الميترونيدازول ومشتقات الإيثر تستهدف Helicobacter pylori عبر تحفيز الإجهاد وكبحه في آن واحد
لماذا لا تزال بكتيريا المعدة والأدوية القديمة مهمة
Helicobacter pylori هي بكتيريا لوالبية الشكل تستعمر معدة نحو نصف سكان العالم بهدوء. معظم الأشخاص لا يشعرون بأي شيء، لكن العدوى طويلة الأمد قد تؤدي إلى قرح وحتى سرطان المعدة. اعتمد الأطباء لعقود على دواء قديم يسمى الميترونيدازول للمساعدة في القضاء على هذه البكتيريا، غير أنّ تزايد المقاومة يعني الحاجة إلى جرعات أعلى وتركيبات متعددة الأدوية—أنظمة علاجية قد تضرّ بالميكروبات المفيدة في الأمعاء. تطرح هذه الدراسة سؤالًا بسيطًا له عواقب كبيرة: هل يمكننا إعادة تصميم هذا الدواء القديم ليضرب H. pylori بقوة أكبر، بجرعات أقل، ومع ضرر جانبي أقل؟
دواء مطوَّر بقوة مفاجئة
بدأ الباحثون من الهيكل الكيميائي الأساسي للميترونيدازول وأضافوا «مقابض» صغيرة تُسمى مجموعات الإيثر، مكوّنين سلسلة من المركبات الجديدة التي تتصرف كأقارب قريبة من الدواء الأصلي. عند اختبار هذه المتغيرات ضد H. pylori في المختبر، كان بعضها أقوى بما يصل إلى 60 ضعفًا من الميترونيدازول نفسه، موقفة نمو البكتيريا عند تراكيز ضئيلة. ومن المهم أن هذه الزيادة في الفعالية لم تنجم ببساطة عن جعل الدواء "نشطًا" بسهولة أكبر عبر كيمياء الاختزال المألوفة، ما يشير إلى أنّ الجزيئات المعدَّلة تقوم بشيء مختلف نوعيًا داخل الخلية البكتيرية.
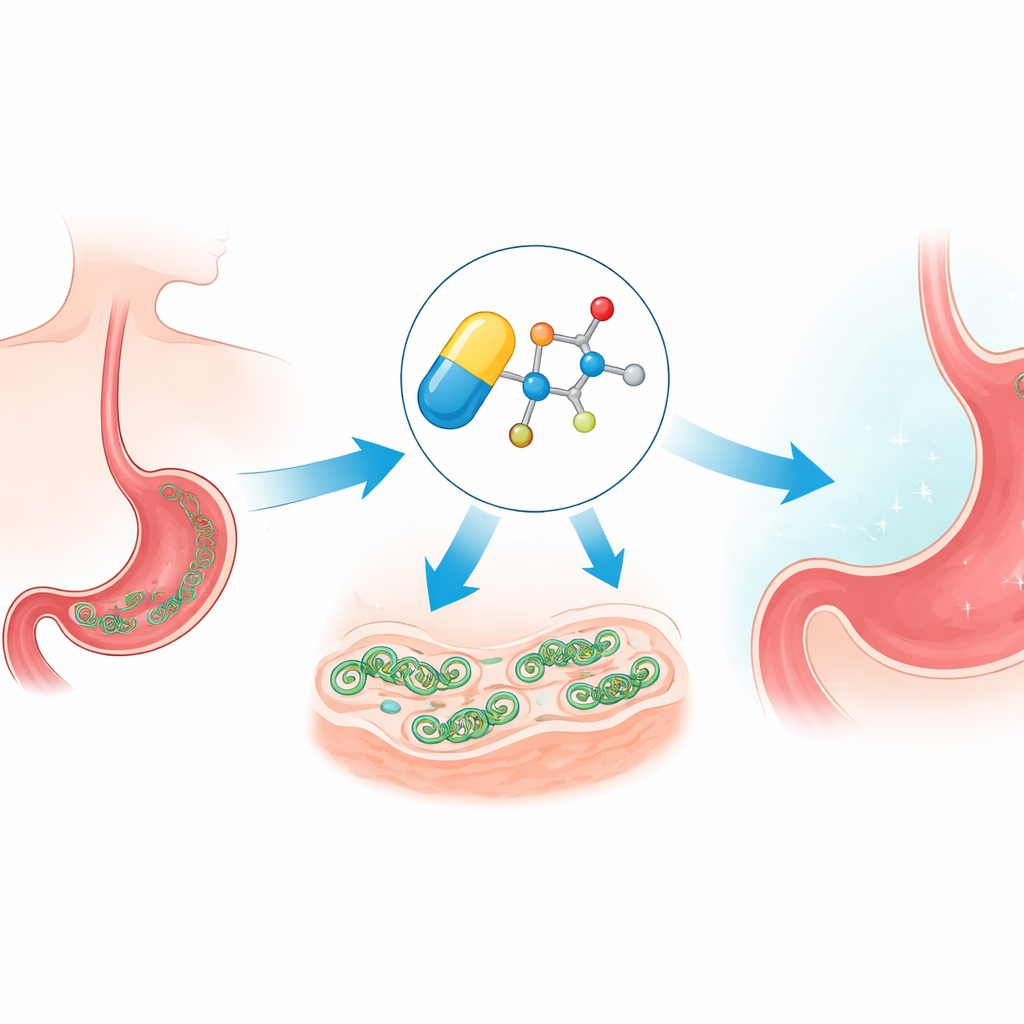
كيف يتسلل الدواء ويحمّل الخلية فوق طاقتها
الميترونيدازول معروف كدواء سابق النشاط: بمجرد دخوله الميكروب، يتم اختزال مجموعة النيترو فيه كيميائيًا لتشكل أنواعًا جذريّة عدوانية. تهاجم هذه الشظايا التفاعلية جزيئات حيوية مثل الحمض النووي والبروتينات، مخلّفة إجهادًا تأكسديًا. أكدت المجموعة أن نسخ الإيثر الجديدة لا تزال تتبع هذا المسار، مولدة إجهادًا داخل H. pylori. لكن لأن هذه التفاعلات تعتمد على ظروف منخفضة الأكسجين، تظل المركبات في الغالب غير نشطة في أنسجة الإنسان الغنية بالأكسجين، ما يساعد على تفسير لماذا كانت عائلة الأدوية هذه فعالة ضد الميكروبات وآمنة نسبيًا للمرضى.
استهداف طواقم الإصلاح الطارئ لدى البكتيريا
لاكتشاف ما الذي تفعله الأدوية المعدّلة أيضًا، استخدم العلماء تقنية تتبع البروتين النشط، وهي طريقة صيد كيميائية حيث تلتصق مجسات شبيهة بالأدوية بأهدافها ويمكن سحبها وتحديدها. كشف ذلك عن «التقاطين» بروتينيين رئيسيين في H. pylori: مساعد طي يُسمى HpGroEL، الذي يعمل كمشرف لإعادة طي البروتينات المتضررة، وإنزيم يُدعى HpTpx، الذي يحيد البيروكسيدات الضارة ويحمي الحمض النووي من التلف التأكسدي. ارتبطت مركبات الإيثر بقوة خاصة مع HpTpx، مكونة ارتباطات دائمة عند سيستئين حاسم في موقعه النشط ومقللة بشدة قدرته على تحييد البيروكسيدات. فعليًا، تولد هذه الأدوية فوضى تأكسدية وتُعطّل في الوقت نفسه فرقة مكافحة الحرائق في الخلية.
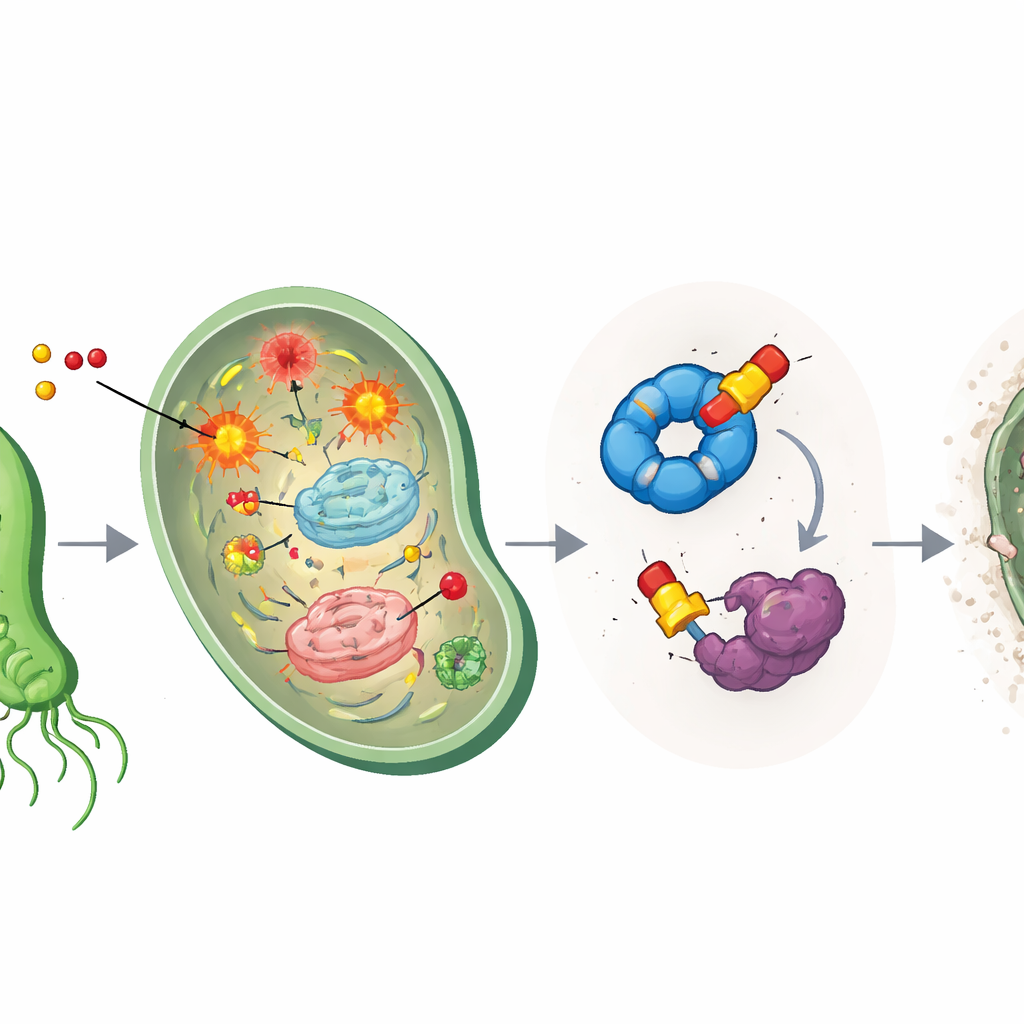
من أنبوب الاختبار إلى معدة الفأر
المضادات الحيوية الفعالة مفيدة فقط إذا كانت تتصرف جيدًا داخل الجسم، لذا فحص الفريق السمية وكيفية تنقّل الجزيئات الجديدة في أنظمة الحيوان. في مزروعات خلايا بشرية، أظهرت مشتقات الإيثر سميّة منخفضة جدًا، وأشارت اختبارات ثباتها الكيميائي إلى أنها صمدت جيدًا في بلازما الدم. أظهرت دراسات الحرائك الدوائية في الفئران مركبًا واحدًا مميزًا، MF‑01، الذي بلغ مستويات ملائمة في الأمعاء مع حفاظه على ثبات جيد. في نموذج عدوى H. pylori الذي يحاكي العلاج البشري—باستخدام تركيبة مع كلاريثروميسين ومانع لحموضة المعدة—أزال MF‑01 البكتيريا تمامًا بجرعة تقارب واحدًا من خمسين من جرعة الميترونيدازول القياسية. عند مثل هذه الجرعات المنخفضة، كان الأثر العام على الميكروبيوم المعوي الطبيعي أخف من العلاج الثلاثي التقليدي، وكانت بكتيريا معوية نافعة شائعة لدى الفئران أقل حساسية تجاه MF‑01 مقارنةً بالميترونيدازول.
ماذا يعني هذا للمرضى والأدوية المستقبلية
مجمل القول، تُظهر الدراسة أن الميترونيدازول ومشتقاته الإيثرية تعمل عبر ضربة مزدوجة قوية: تحفّزان الإجهاد التأكسدي داخل H. pylori بينما تمنعان في الوقت نفسه أنظمة الاستجابة للإجهاد الأساسية التي كانت ستنقذ الخلية عادة. يفسر هذا الهجوم المزدوج الزيادة الدرامية في الفعالية ويقترح أن مشتقات مضبوطة بعناية يمكن أن تُحيي وتحسّن فئة مضادات حيوية متقادمة. وبما أن هذه الجزيئات الجديدة مشتقة من دواء مُصادق عليه منذ زمن طويل، فإنها تبدأ مع ميزة في تقييمات السلامة. إذا أكدت الدراسات السريرية المستقبلية نتائج الفئران، فإن مركبات مثل MF‑01 قد تمكّن من نظم علاج أقصر وبجرعات أدنى تشفي H. pylori بشكل أكثر موثوقية مع تأثير أرحم على النظام البيئي المعوي.
الاستشهاد: Fiedler, M.K., Pandler, M.S.I., Gong, R. et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition. Nat Microbiol 11, 1049–1063 (2026). https://doi.org/10.1038/s41564-026-02291-w
الكلمات المفتاحية: Helicobacter pylori, الميترونيدازول, مقاومة المضادات الحيوية, الإجهاد التأكسدي, الميكروبيوم المعوي