Clear Sky Science · pl
Metronidazol i pochodne eterowe celują w Helicobacter pylori przez jednoczesne wywoływanie stresu i jego hamowanie
Dlaczego bakterie żołądkowe i stare leki wciąż mają znaczenie
Helicobacter pylori to spiralnie skręcona bakteria, która skrycie kolonizuje żołądki niemal połowy populacji świata. Większość osób nic nie odczuwa, ale długotrwała infekcja może prowadzić do wrzodów, a nawet raka żołądka. Przez dekady lekarze polegali na starszym leku o nazwie metronidazol, by zwalczać tę bakterię, jednak rosnąca oporność wymusza wyższe dawki i terapie wielolekowe — schematy, które mogą zaburzać przyjazne mikroorganizmy jelitowe. To badanie stawia proste pytanie o dalekosiężnych konsekwencjach: czy można przeprojektować tego starego środka, żeby silniej działał na H. pylori, przy niższych dawkach i z mniejszymi skutkami ubocznymi?
Ulepszony lek o zaskakującej sile
Naukowcy zaczęli od rdzeniowej struktury chemicznej metronidazolu i dodali małe „uchwyty” zwane grupami eterowymi, tworząc serię nowych związków będących bliskimi krewnymi oryginalnego leku. Gdy testowali te warianty przeciwko H. pylori w laboratorium, niektóre były nawet do 60 razy bardziej aktywne niż sam metronidazol, hamując wzrost bakterii przy bardzo niskich stężeniach. Co ważne, wzrost skuteczności nie wynikał po prostu z łatwiejszego „włączenia” leku przez standardową chemię redoks, co sugeruje, że zmodyfikowane cząsteczki robią wewnątrz komórki bakteryjnej coś jakościowo innego.
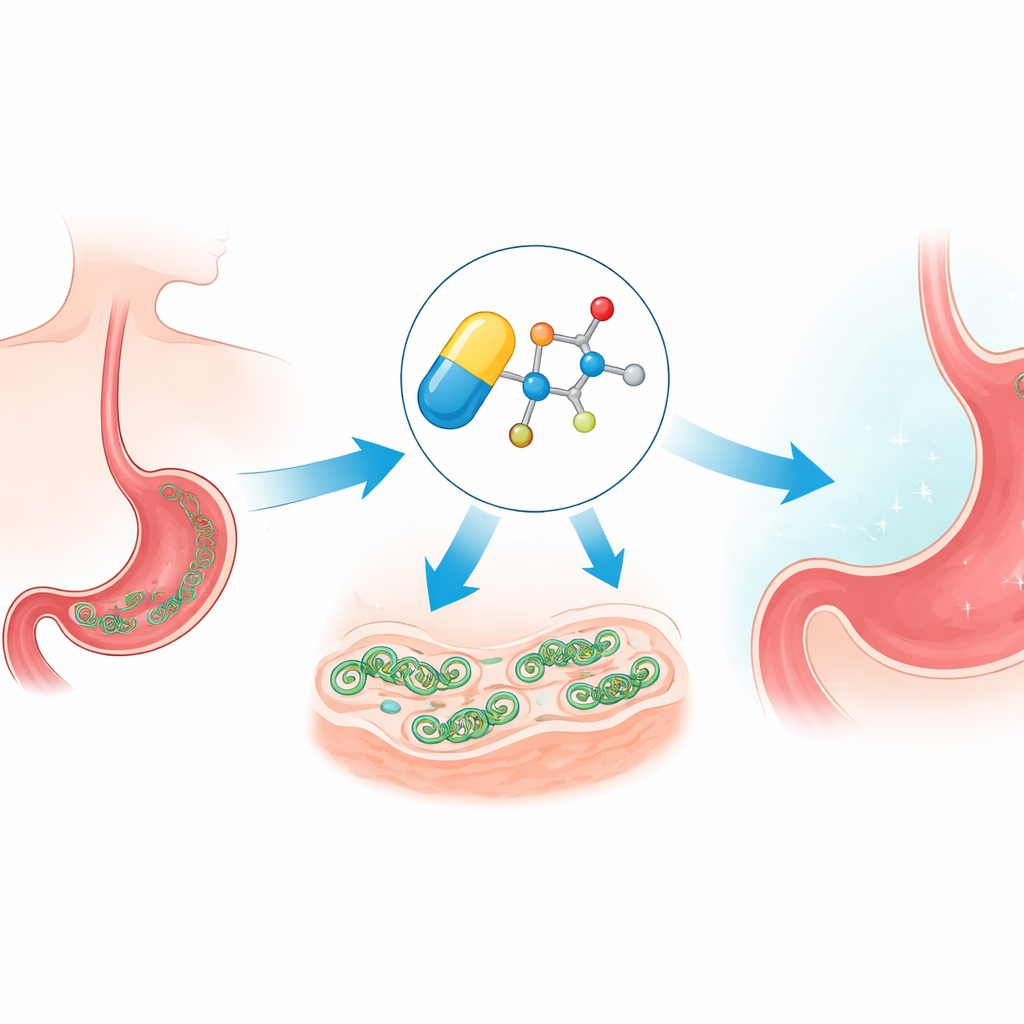
Jak lek wnika i przeciąża komórkę
Metronidazol to tzw. prolek: gdy przedostaje się do mikroorganizmu, jego grupa nitrowa ulega redukcji chemicznej, tworząc agresywne rodnikowe fragmenty. Te reaktywne fragmenty atakują kluczowe cząsteczki, takie jak DNA i białka, wywołując stres oksydacyjny. Zespół potwierdził, że nowe eterowe wersje również podążają tą ścieżką, generując stres wewnątrz H. pylori. Ponieważ jednak te reakcje zależą od niskiego stężenia tlenu, związki pozostają w dużej mierze nieaktywne w dobrze natlenowanych tkankach ludzkich, co pomaga wyjaśnić, dlaczego ta rodzina leków od dawna jest skuteczna przeciwko mikrobom, a jednocześnie stosunkowo bezpieczna dla pacjentów.
Atak na „służby ratownicze” bakterii
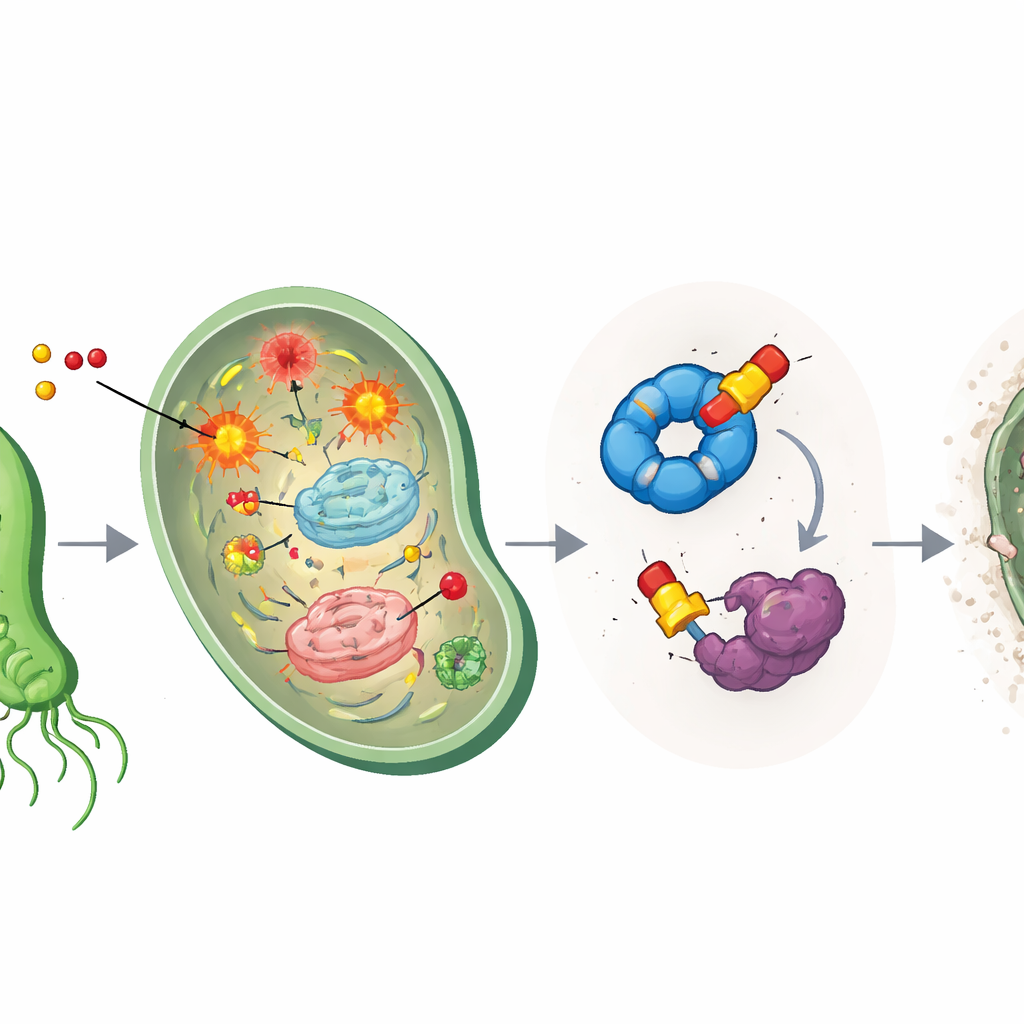
Aby ustalić, co jeszcze robią zmodyfikowane leki, naukowcy użyli profilowania białek opartego na aktywności, chemicznej metody „łowienia”, w której sondy podobne do leku przyłączają się do celów i mogą być wyciągnięte oraz zidentyfikowane. Wykazało to dwie główne „zdobyczne” białka w H. pylori: pomocnika w fałdowaniu o nazwie HpGroEL, działającego jak chaperon odtwarzający zniszczone białka, oraz enzymu HpTpx, który neutralizuje szkodliwe nadtlenki i chroni DNA przed uszkodzeniami oksydacyjnymi. Związki eterowe szczególnie silnie wiązały się z HpTpx, tworząc trwałe przyłączenia przy krytycznej cysteinie w miejscu aktywnym i wyraźnie zmniejszając jego zdolność do detoksykacji nadtlenków. W praktyce leki jednocześnie wywołują chaos oksydacyjny i wyłączają „straż pożarną” komórki.
Od probówki do żołądka myszy
Silne antybiotyki są przydatne tylko wtedy, gdy zachowują się korzystnie w organizmie, dlatego zespół badał toksyczność i dystrybucję nowych cząsteczek w organizmach zwierzęcych. W hodowlach komórek ludzkich pochodne eterowe wykazały bardzo niską toksyczność, a testy stabilności chemicznej wskazały, że dobrze przetrwały w osoczu krwi. Badania farmakokinetyczne na myszach wyodrębniły jeden wyróżniający się związek, MF‑01, który osiągał korzystne stężenia w przewodzie pokarmowym przy jednoczesnym zachowaniu dobrej stabilności. W modelu infekcji H. pylori naśladującym leczenie u ludzi — zastosowanym w połączeniu z klarytromycyną i blokerem kwasu żołądkowego — MF‑01 całkowicie wyeliminował bakterie przy dawce około jednej pięćdziesiątej standardowej dawki metronidazolu. Przy tak niskich dawkach ogólny wpływ na normalny mikrobiom jelitowy był łagodniejszy niż przy konwencjonalnej terapii potrójnej, a powszechne korzystne bakterie jelitowe myszy były mniej wrażliwe na MF‑01 niż na metronidazol.
Co to oznacza dla pacjentów i przyszłych leków
Sumarycznie praca pokazuje, że metronidazol i jego eterowe krewni działają poprzez silne uderzenie „jeden‑dwa”: wywołują stres oksydacyjny wewnątrz H. pylori, jednocześnie blokując kluczowe systemy reagowania na stres, które normalnie ratowałyby komórkę. Ten podwójny atak tłumaczy dramatyczny wzrost mocy działania i sugeruje, że starannie dostrojone pochodne mogą ożywić i poprawić starzejącą się klasę antybiotyków. Ponieważ nowe cząsteczki wyrosły z długo zatwierdzonego leku, zaczynają z przewagą w profilowaniu bezpieczeństwa. Jeśli przyszłe badania kliniczne potwierdzą wyniki u myszy, związki takie jak MF‑01 mogłyby umożliwić krótsze, niższe dawki leczenia, które skuteczniej wyleczą zakażenia H. pylori, jednocześnie będąc łagodniejszymi dla reszty ekosystemu jelitowego.
Cytowanie: Fiedler, M.K., Pandler, M.S.I., Gong, R. et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition. Nat Microbiol 11, 1049–1063 (2026). https://doi.org/10.1038/s41564-026-02291-w
Słowa kluczowe: Helicobacter pylori, metronidazol, oporność na antybiotyki, stres oksydacyjny, mikrobiom jelitowy