Clear Sky Science · de
Metronidazol und Etherderivate zielen auf Helicobacter pylori durch gleichzeitige Stressinduktion und Hemmung
Warum Magenkeime und alte Medikamente noch relevant sind
Helicobacter pylori ist ein spiralförmiges Bakterium, das stillschweigend die Mägen von fast der Hälfte der Weltbevölkerung besiedelt. Die meisten Menschen spüren nichts, doch eine langfristige Infektion kann zu Geschwüren und sogar Magenkrebs führen. Ärztinnen und Ärzte verlassen sich seit Jahrzehnten auf ein älteres Medikament namens Metronidazol, um diesen Keim zu bekämpfen. Steigende Resistenzen erfordern jedoch inzwischen höhere Dosen und Kombinationsschemata mit mehreren Wirkstoffen — Regime, die das nützliche Mikrobiom im Darm stören können. Diese Studie stellt eine einfache Frage mit großen Konsequenzen: Können wir dieses altbewährte Medikament so umgestalten, dass es H. pylori stärker trifft, in niedrigeren Dosen wirkt und weniger Kollateralschäden verursacht?
Ein aufgerüstetes Medikament mit überraschender Stärke
Die Forschenden begannen mit der Kernstruktur von Metronidazol und setzten kleine „Griffe“ namens Ethergruppen daran, wodurch eine Reihe neuer Verbindungen entstand, die wie nahe Verwandte des Originals funktionieren. Als sie diese Varianten im Labor gegen H. pylori testeten, waren einige bis zu 60‑mal wirksamer als Metronidazol selbst und stoppten das Bakterienwachstum bei sehr geringen Konzentrationen. Wichtig ist, dass dieser Wirkungszuwachs nicht einfach daherkommt, dass das Medikament über die übliche Redoxchemie leichter „aktiviert“ wird. Das deutet darauf hin, dass die modifizierten Moleküle im Inneren der Bakterienzelle qualitativ anders wirken müssen.
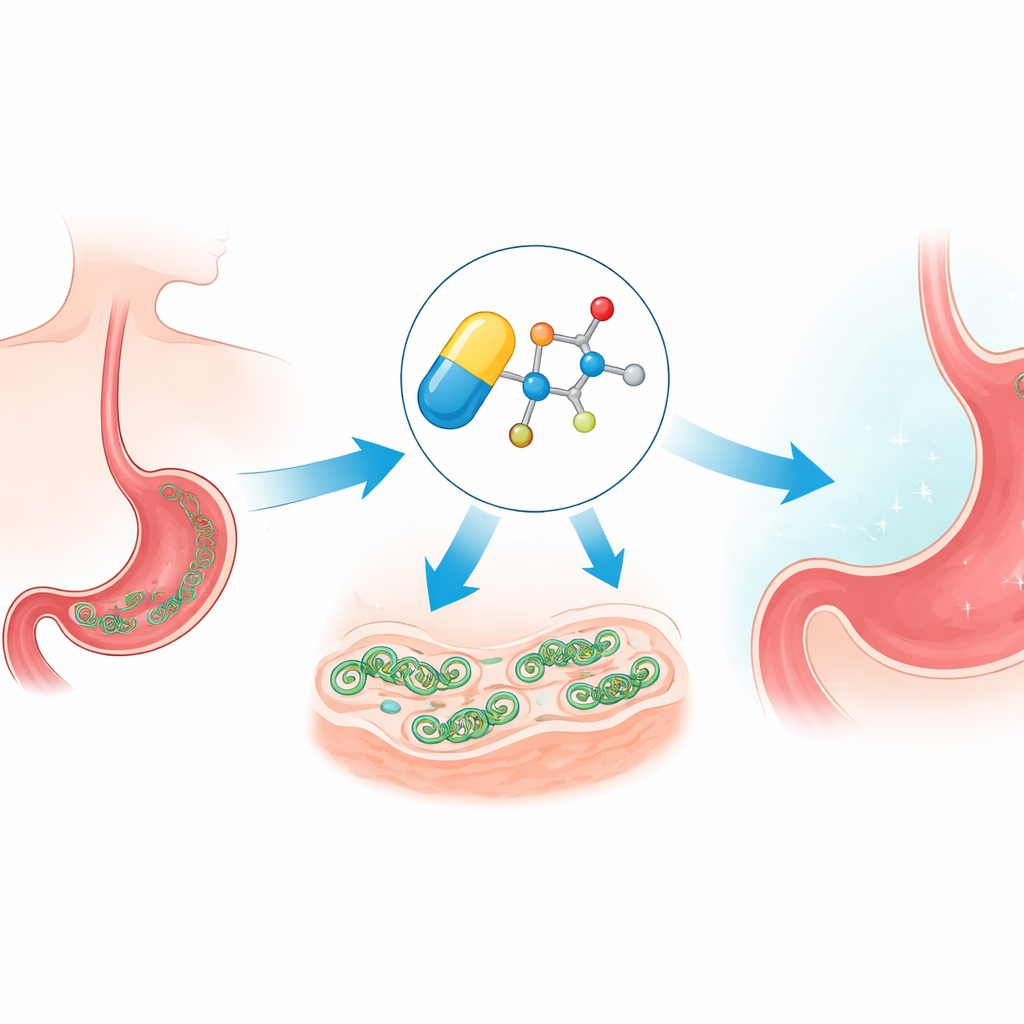
Wie das Medikament eindringt und die Zelle überlädt
Metronidazol ist ein sogenanntes Prodrug: Sobald es in ein Mikroorganismus gelangt, wird seine Nitrogruppe chemisch reduziert und bildet aggressive Radikalarten. Diese reaktiven Fragmente greifen lebenswichtige Moleküle wie DNA und Proteine an und erzeugen oxidativen Stress. Das Team bestätigte, dass die neuen Ether‑Versionen diesem Pfad weiterhin folgen und in H. pylori Stress erzeugen. Da diese Reaktionen jedoch auf sauerstoffarmen Bedingungen beruhen, bleiben die Verbindungen in gut mit Sauerstoff versorgten menschlichen Geweben größtenteils inaktiv, was erklärt, warum diese Wirkstofffamilie schon lange gegen Mikroben nützlich und gleichzeitig für Patientinnen und Patienten relativ sicher ist.
Treffer für die Notfallreparaturmannschaften des Keims
Um herauszufinden, was die modifizierten Medikamente sonst noch bewirkten, nutzten die Wissenschaftlerinnen und Wissenschaftler activity‑basierte Proteinprofilierung, eine chemische Fangmethode, bei der medikamentähnliche Sonden an ihre Ziele binden und dann herausgezogen und identifiziert werden können. Dies enthüllte zwei Hauptprotein„fänge“ in H. pylori: ein Faltungshelfer namens HpGroEL, der wie ein Chaperon beschädigte Proteine wieder auffaltet, und ein Enzym namens HpTpx, das schädliche Peroxide neutralisiert und die DNA vor oxidativen Schäden schützt. Die etherbasierten Verbindungen banden besonders stark an HpTpx, bildeten dauerhafte Bindungen an einer kritischen Cysteinstelle im aktiven Zentrum und reduzierten dessen Fähigkeit, Peroxide zu entgiften, deutlich. Effektiv erzeugen die Medikamente oxidatives Chaos und deaktivieren gleichzeitig die Feuerwehreinheiten der Zelle.
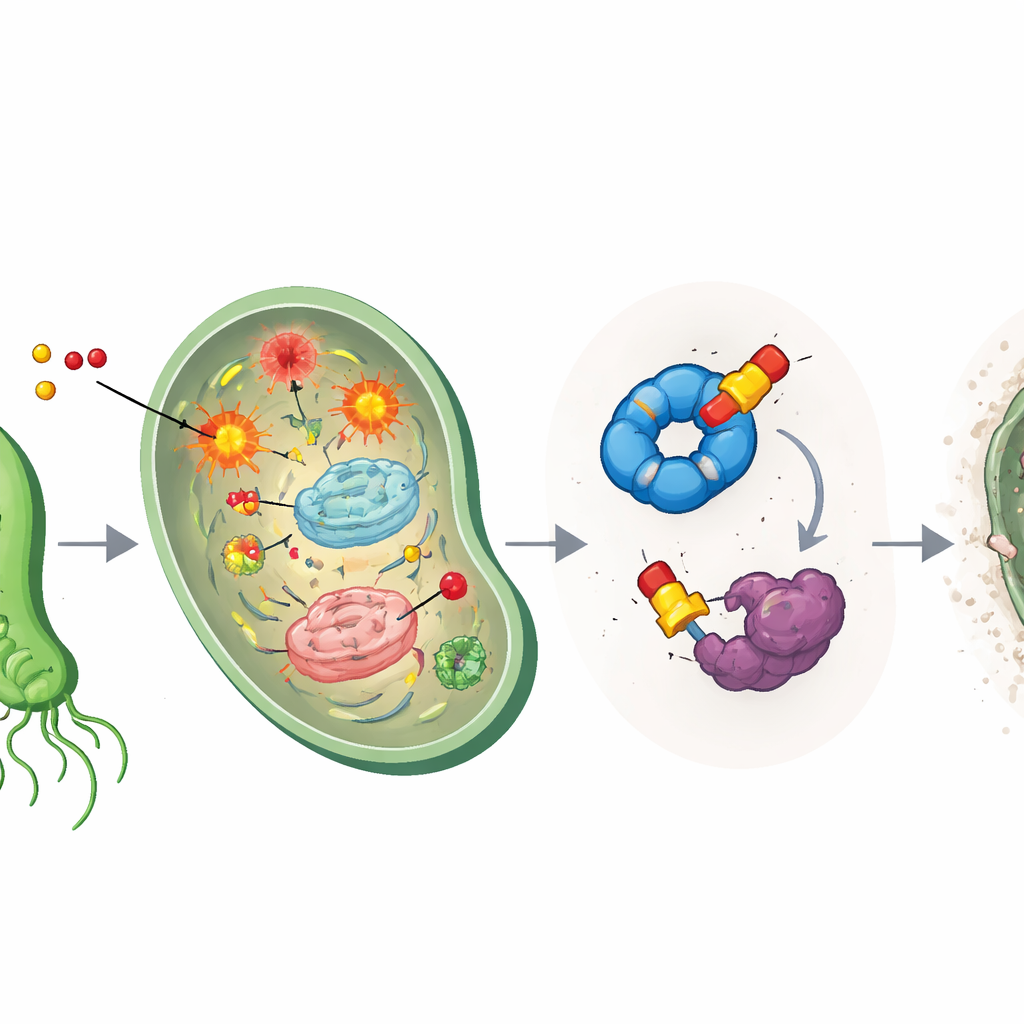
Vom Reagenzglas zum Mäusemagen
Potente Antibiotika sind nur dann nützlich, wenn sie sich im Körper gut verhalten. Daher untersuchte das Team Toxizität und die Verteilung der neuen Moleküle im tierischen Organismus. In Kulturen menschlicher Zellen zeigten die Etherderivate sehr geringe Toxizität, und Stabilitätstests deuteten darauf hin, dass sie im Blutplasma gut überleben. Pharmakokinetische Untersuchungen in Mäusen hoben eine herausragende Verbindung, MF‑01, hervor, die günstige Konzentrationen im Darm erreichte und zugleich gute Stabilität aufwies. In einem H. pylori‑Infektionsmodell, das die Behandlung beim Menschen nachahmt — in Kombination mit Clarithromycin und einem Magensäureblocker — eliminierte MF‑01 die Bakterien vollständig bei etwa einem Fünfzigstel der üblichen Metronidazol‑Dosis. Bei so niedrigen Dosen war die Gesamtwirkung auf das normale Darmmikrobiom milder als bei der konventionellen Dreifachtherapie, und häufig vorkommende nützliche Maus‑Darmbakterien waren gegenüber MF‑01 weniger empfindlich als gegenüber Metronidazol.
Was das für Patientinnen, Patienten und zukünftige Wirkstoffe bedeutet
In der Summe zeigt die Arbeit, dass Metronidazol und seine Etherverwandten durch einen kraftvollen Doppelangriff wirken: Sie lösen oxidativen Stress in H. pylori aus und blockieren zugleich zentrale Stressantwortsysteme, die normalerweise die Zelle retten würden. Dieser doppelte Angriff erklärt die dramatische Zunahme der Wirksamkeit und legt nahe, dass sorgfältig abgestimmte Derivate eine alternde Antibiotikaklasse wiederbeleben und verbessern könnten. Da diese neuen Moleküle aus einem lange zugelassenen Medikament hervorgehen, haben sie einen Vorsprung bei der Sicherheitsbewertung. Bestätigen zukünftige klinische Studien die Mäuseergebnisse, könnten Verbindungen wie MF‑01 kürzere, niedrigerdosierte Behandlungsregime ermöglichen, die H. pylori‑Infektionen verlässlicher heilen und gleichzeitig das übrige Darmökosystem schonender behandeln.
Zitation: Fiedler, M.K., Pandler, M.S.I., Gong, R. et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition. Nat Microbiol 11, 1049–1063 (2026). https://doi.org/10.1038/s41564-026-02291-w
Schlüsselwörter: Helicobacter pylori, Metronidazol, antibiotische Resistenz, oxidativer Stress, Darmmikrobiom