Clear Sky Science · nl
Metronidazol en etherafgeleiden richten zich op Helicobacter pylori door gelijktijdige stressverhoging en remming
Waarom maagbacteriën en oude geneesmiddelen nog steeds belangrijk zijn
Helicobacter pylori is een spiraalvormige bacterie die stilletjes de maag van bijna de helft van de wereldbevolking koloniseert. De meeste mensen voelen er niets van, maar een langdurige infectie kan leiden tot zweren en zelfs maagkanker. Artsen vertrouwen al tientallen jaren op een ouder geneesmiddel genaamd metronidazol om deze bacterie uit te roeien, maar de toenemende resistentie betekent dat nu hogere doses en combinaties van meerdere middelen nodig zijn—regimes die de vriendelijke microben van de darm kunnen verstoren. Deze studie stelt een eenvoudige vraag met grote gevolgen: kunnen we deze oude krachtpatser herontwerpen zodat hij H. pylori harder treft, bij lagere doses en met minder nevenschade?
Een verbeterd middel met verrassende kracht
De onderzoekers begonnen met de kernchemie van metronidazol en voegden kleine “handvatten” toe, zogenaamde ethergroepen, waardoor een reeks nieuwe verbindingen ontstond die als nabije verwanten van het oorspronkelijke geneesmiddel functioneren. Wanneer ze deze varianten in het laboratorium tegen H. pylori testten, waren sommige tot wel 60 keer krachtiger dan metronidazol zelf en stopten ze de bacteriële groei bij zeer lage concentraties. Belangrijk is dat deze versterking niet simpelweg voortkwam uit het makkelijker “activeren” van het middel via standaard redoxchemie, wat suggereert dat de gewijzigde moleculen iets kwalitatief anders moeten doen binnen de bacteriële cel.
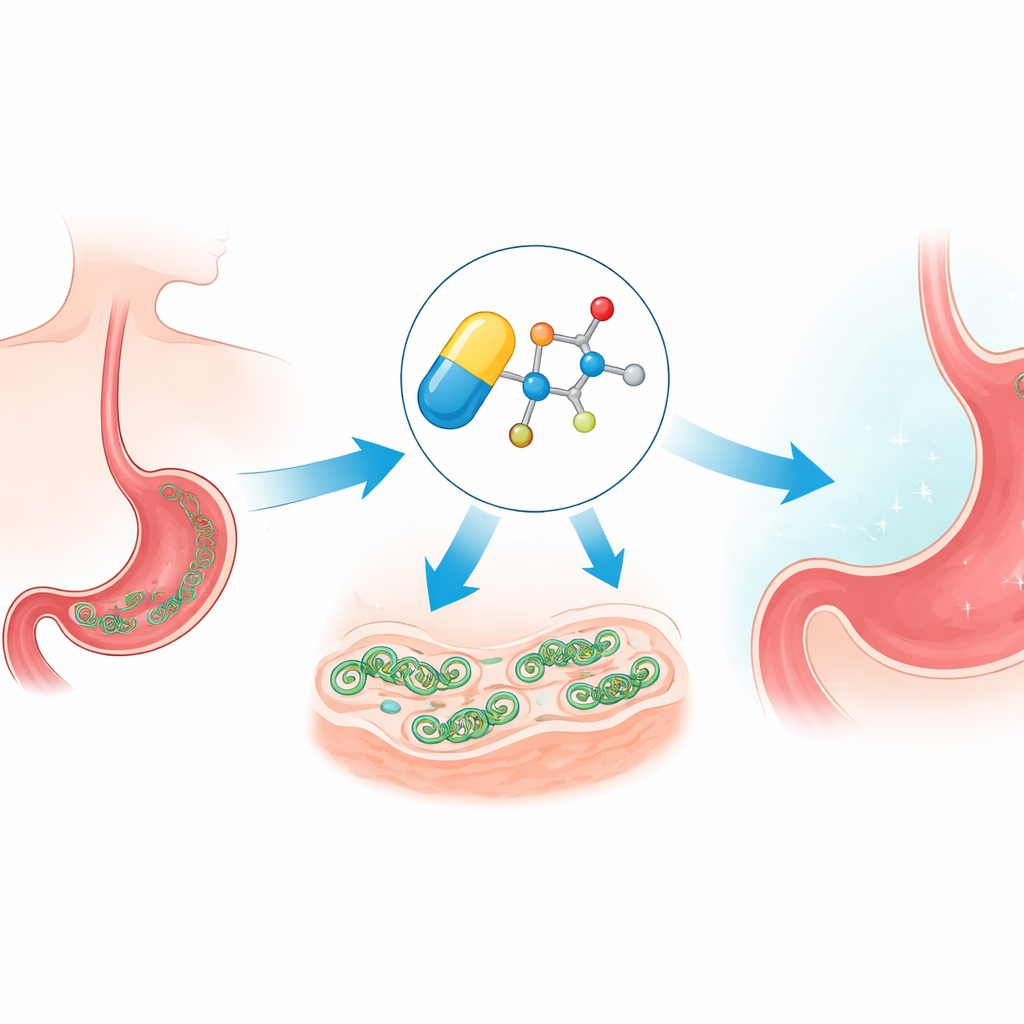
Hoe het middel de cel binnensluipt en overbelast
Metronidazol is een zogenoemde prodrug: zodra het een microbe binnendringt, wordt de nitrogroep chemisch gereduceerd en ontstaan er agressieve radicaalsoorten. Deze reactieve fragmenten vallen vitale moleculen zoals DNA en eiwitten aan, waardoor oxidatieve stress ontstaat. Het team bevestigde dat de nieuwe etherversies deze route nog steeds volgen en stress genereren in H. pylori. Omdat deze reacties echter afhankelijk zijn van zuurstofarme omstandigheden, blijven de verbindingen grotendeels inactief in zuurstofrijke menselijke weefsels, wat helpt verklaren waarom deze geneesmiddelfamilie lange tijd effectief is geweest tegen microben maar relatief veilig voor patiënten.
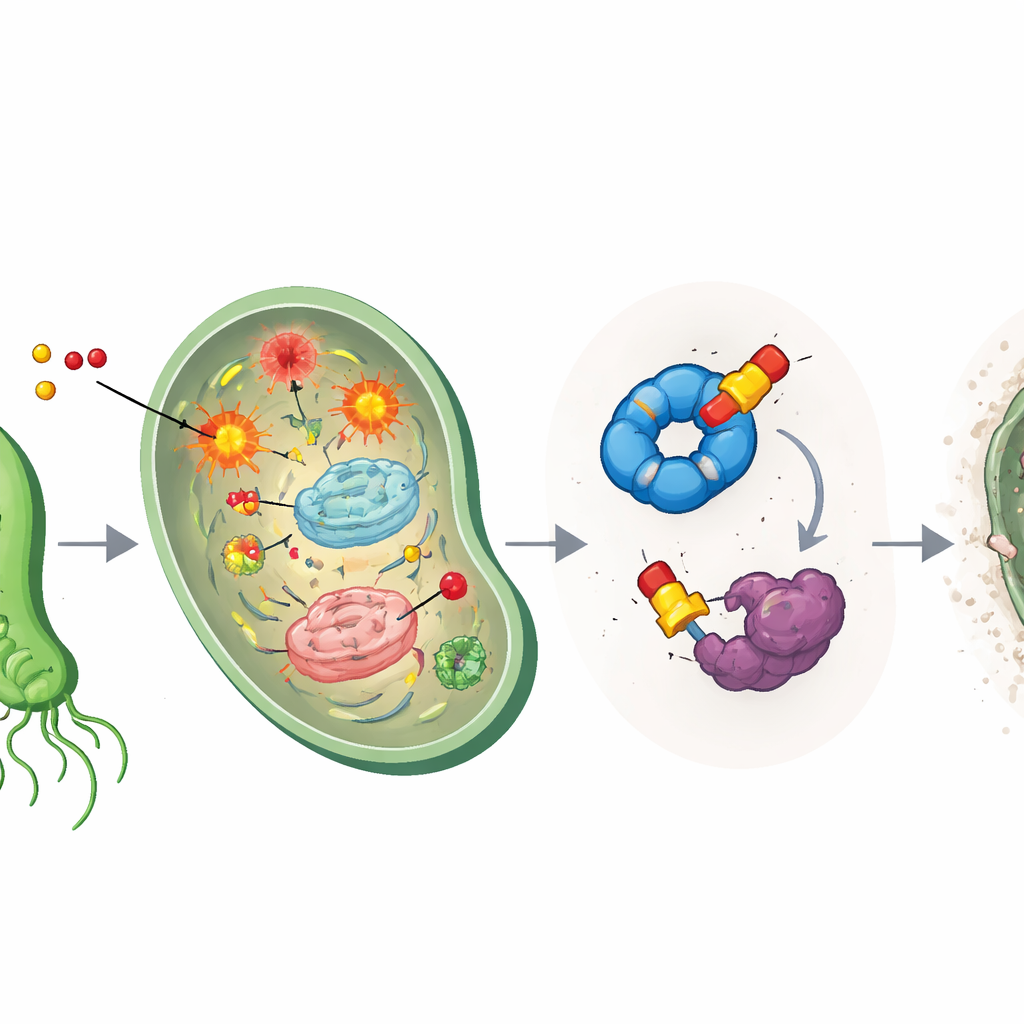
De nooddiensten van de bacterie uitschakelen
Om te achterhalen wat de gewijzigde middelen verder deden, gebruikten de wetenschappers activity-based proteïneprofilering, een chemische vismethode waarbij middelachtige probes zich vasthechten aan hun doelen en vervolgens kunnen worden gevangen en geïdentificeerd. Dit onthulde twee belangrijke eiwitvangers in H. pylori: een vouwhulpje genaamd HpGroEL, dat als een chaperonne beschadigde eiwitten helpt refouwen, en een enzym genaamd HpTpx, dat schadelijke peroxiden neutraliseert en het DNA beschermt tegen oxidatieve schade. De op ether gebaseerde verbindingen binden vooral sterk aan HpTpx, waarbij ze permanente verbindingen aangaan met een kritisch cysteïne in het actieve centrum en zo de capaciteit om peroxiden te ontgiften scherp verminderen. In feite creëren de middelen zowel oxidatieve chaos als het uitschakelen van de brandweer van de cel tegelijk.
Van reageerbuis naar muagmaag
Krachtige antibiotica zijn alleen nuttig als ze zich goed in het lichaam gedragen, dus het team onderzocht toxiciteit en hoe de nieuwe moleculen zich door dierlijke systemen bewegen. In menselijke celkweek toonden de etherderivaten zeer lage toxiciteit, en chemische stabiliteitstests gaven aan dat ze goed in bloedplasma overleven. Farmacokinetische studies in muizen belichtten één opvallende verbinding, MF‑01, die gunstige niveaus in de darm bereikte terwijl ze goede stabiliteit behield. In een H. pylori-infectiemodel dat menselijke behandeling nabootst—met een combinatie van claritromycine en een maagzuurremmer—maakte MF‑01 de bacterie volledig onschadelijk bij ongeveer éénvijftigste van de standaard metronidazoldosis. Bij zulke lage doses was de totale impact op het normale darmmicrobioom milder dan bij conventionele driedubbele therapie, en veel voorkomende gunstige muisdarmbacteriën waren minder gevoelig voor MF‑01 dan voor metronidazol.
Wat dit betekent voor patiënten en toekomstige geneesmiddelen
Samengevat laat het werk zien dat metronidazol en zijn etherverwanten optreden via een krachtige tweeslag: ze veroorzaken oxidatieve stress in H. pylori terwijl ze gelijktijdig belangrijke stressresponsystemen blokkeren die de cel normaal zouden redden. Deze dubbele aanval verklaart de dramatische toename in werkzaamheid en suggereert dat zorgvuldig afgestemde derivaten een verouderde antibioticaklasse kunnen nieuw leven inblazen en verbeteren. Omdat deze nieuwe moleculen voortkomen uit een lang goedgekeurd geneesmiddel, hebben ze een voorsprong op veiligheidsprofilering. Als toekomstige klinische studies de muisresultaten bevestigen, zouden verbindingen zoals MF‑01 kortere, lagere doseringsregimes mogelijk kunnen maken die H. pylori-infecties betrouwbaarder genezen en vriendelijker zijn voor de rest van het darmecosysteem.
Bronvermelding: Fiedler, M.K., Pandler, M.S.I., Gong, R. et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition. Nat Microbiol 11, 1049–1063 (2026). https://doi.org/10.1038/s41564-026-02291-w
Trefwoorden: Helicobacter pylori, metronidazol, antibioticaresistentie, oxitatieve stress, darmmicrobioom