Clear Sky Science · pt
Metronidazol e derivados éter atacam Helicobacter pylori por indução simultânea de estresse e inibição
Por que os germes do estômago e medicamentos antigos ainda importam
Helicobacter pylori é um germe em forma de espiral que coloniza silenciosamente o estômago de quase metade da população mundial. A maioria das pessoas não sente nada, mas a infecção de longa duração pode levar a úlceras e até câncer gástrico. Por décadas, os médicos confiaram em um medicamento mais antigo chamado metronidazol para ajudar a eliminar esse microrganismo, porém a resistência crescente exige doses mais altas e combinações de vários fármacos — esquemas que podem prejudicar os microrganismos benéficos do intestino. Este estudo faz uma pergunta simples com grandes consequências: podemos redesenhar esse medicamento veterano para atingir H. pylori com mais eficácia, em doses menores e com menos danos colaterais?
Um remédio aperfeiçoado com força surpreendente
Os pesquisadores partiram da estrutura química central do metronidazol e anexaram pequenas “alças” chamadas grupos éter, criando uma série de novos compostos que se comportam como parentes próximos do fármaco original. Quando testaram essas variantes contra H. pylori em laboratório, algumas mostraram-se até 60 vezes mais potentes que o metronidazol, interrompendo o crescimento bacteriano em concentrações mínimas. Importante: esse aumento de potência não veio simplesmente de ativar o fármaco mais facilmente por química redox padrão, o que sugere que as moléculas modificadas estão fazendo algo qualitativamente diferente dentro da célula bacteriana.
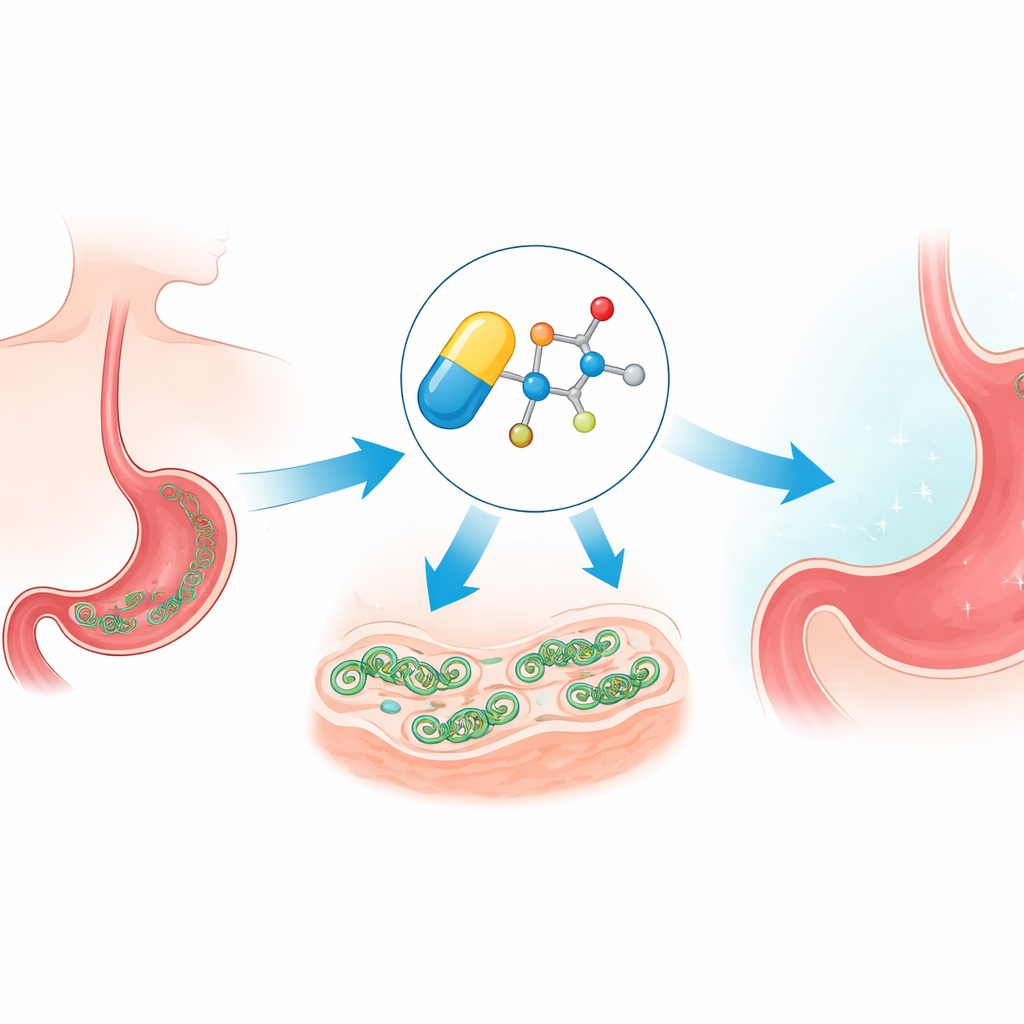
Como o medicamento entra sorrateiramente e sobrecarrega a célula
Metronidazol é um chamado pró-fármaco: uma vez que penetra em um microrganismo, seu grupo nitro é quimicamente reduzido para formar espécies radicais agressivas. Esses fragmentos reativos atacam moléculas vitais, como DNA e proteínas, gerando estresse oxidativo. A equipe confirmou que as novas versões éter ainda seguem esse caminho, gerando estresse dentro de H. pylori. Mas, como essas reações dependem de condições de baixo oxigênio, os compostos permanecem em grande parte inativos em tecidos humanos bem oxigenados, o que ajuda a explicar por que essa família de fármacos tem sido útil contra micróbios e relativamente segura para pacientes.
Atacando as equipes de reparo de emergência do germe
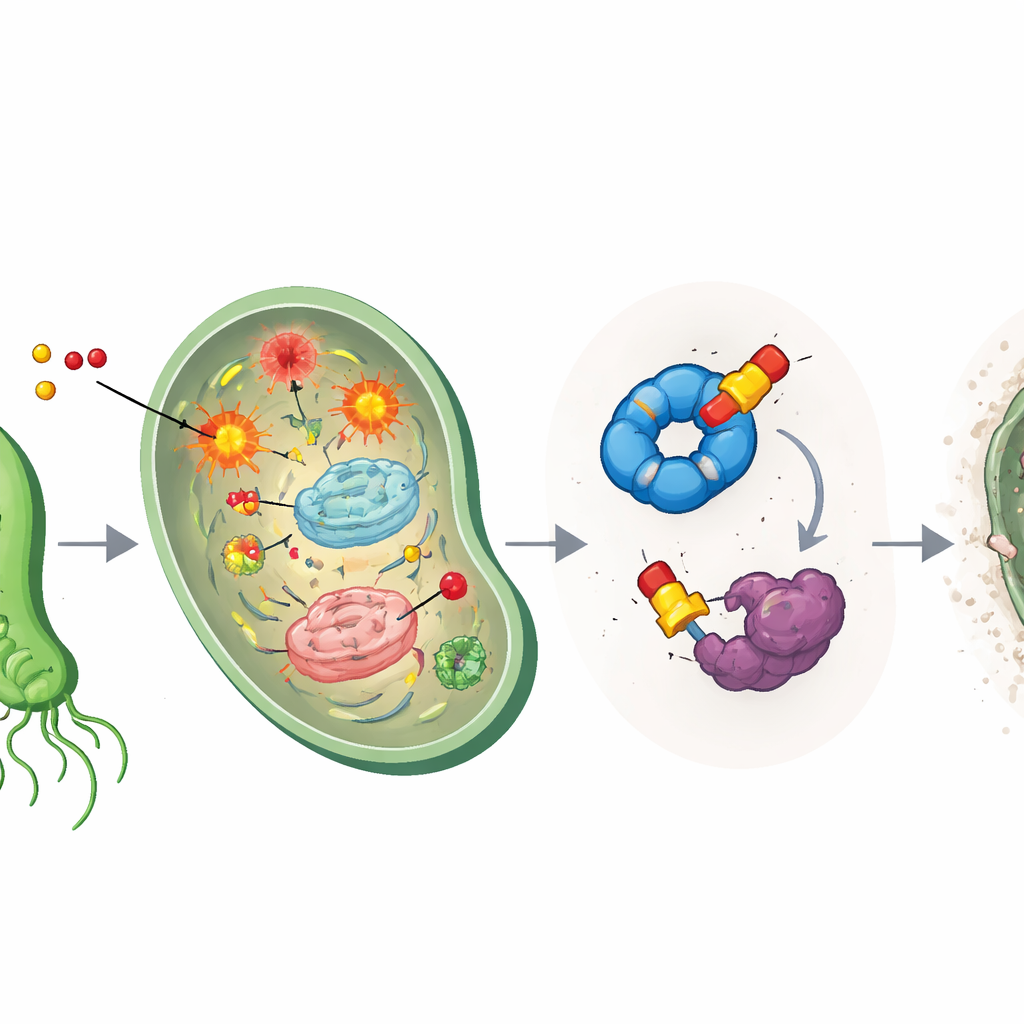
Para descobrir o que mais os fármacos modificados estavam fazendo, os cientistas usaram perfilagem de proteínas baseada em atividade, um método químico de “pesca” em que sondas semelhantes a fármacos se fixam aos alvos e podem ser isoladas e identificadas. Isso revelou dois principais “pegares” proteicos em H. pylori: uma ajudante de dobramento chamada HpGroEL, que atua como chaperona para refoldar proteínas danificadas, e uma enzima chamada HpTpx, que neutraliza peróxidos nocivos e protege o DNA do dano oxidativo. Os compostos à base de éter se ligaram especialmente forte à HpTpx, formando ligações permanentes em uma cisteína crítica no seu sítio ativo e reduzindo drasticamente sua capacidade de desintoxicar peróxidos. Na prática, os fármacos tanto criam um caos oxidativo quanto desabilitam o corpo de bombeiros celular ao mesmo tempo.
Do tubo de ensaio ao estômago de camundongo
Antibióticos potentes são úteis apenas se se comportarem bem no organismo, então a equipe examinou toxicidade e como as novas moléculas se distribuem em sistemas animais. Em culturas de células humanas, os derivados éter mostraram toxicidade muito baixa, e testes de estabilidade química indicaram que eles sobreviveram bem no plasma sanguíneo. Estudos farmacocinéticos em camundongos destacaram um composto de destaque, MF‑01, que alcançou níveis favoráveis no intestino mantendo boa estabilidade. Em um modelo de infecção por H. pylori que imita o tratamento humano — usando uma combinação com claritromicina e um bloqueador de ácido gástrico — MF‑01 eliminou completamente as bactérias em cerca de um cinquenta avos (1/50) da dose padrão de metronidazol. Em doses tão baixas, o impacto geral no microbioma intestinal normal foi mais brando do que com a terapia tripla convencional, e as bactérias intestinais benéficas comuns dos camundongos foram menos sensíveis ao MF‑01 do que ao metronidazol.
O que isso significa para pacientes e futuros medicamentos
Em conjunto, o trabalho mostra que o metronidazol e seus parentes éter atuam por meio de um poderoso golpe duplo: eles desencadeiam estresse oxidativo dentro de H. pylori ao mesmo tempo em que bloqueiam sistemas-chave de resposta ao estresse que normalmente socorreriam a célula. Esse ataque duplo explica o aumento dramático de potência e sugere que derivados cuidadosamente ajustados poderiam reviver e melhorar uma classe de antibióticos envelhecida. Como essas novas moléculas derivam de um fármaco amplamente aprovado, elas já começam com vantagem no perfil de segurança. Se estudos clínicos futuros confirmarem os resultados em camundongos, compostos como o MF‑01 poderiam permitir esquemas mais curtos e com doses menores que curem infecções por H. pylori com mais confiabilidade, sendo mais gentis com o restante do ecossistema intestinal.
Citação: Fiedler, M.K., Pandler, M.S.I., Gong, R. et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition. Nat Microbiol 11, 1049–1063 (2026). https://doi.org/10.1038/s41564-026-02291-w
Palavras-chave: Helicobacter pylori, metronidazol, resistência a antibióticos, estresse oxidativo, microbioma intestinal