Clear Sky Science · es
El metronidazol y derivados éter atacan a Helicobacter pylori mediante inducción simultánea de estrés e inhibición
Por qué siguen importando las bacterias gástricas y los fármacos antiguos
Helicobacter pylori es un germen en forma de espiral que coloniza silenciosamente el estómago de casi la mitad de la población mundial. La mayoría de las personas no siente nada, pero la infección crónica puede provocar úlceras e incluso cáncer de estómago. Durante décadas los médicos han confiado en un fármaco antiguo llamado metronidazol para ayudar a eliminar este microbio, sin embargo el aumento de la resistencia exige dosis más altas y cócteles de varios fármacos—regímenes que pueden alterar los microbios beneficiosos del intestino. Este estudio plantea una pregunta sencilla con grandes consecuencias: ¿podemos rediseñar a este viejo caballo de batalla para que ataque H. pylori con más fuerza, a dosis más bajas y con menos daños colaterales?
Un fármaco mejorado con fuerza sorprendente
Los investigadores partieron de la estructura química base del metronidazol y añadieron pequeñas «asideras» llamadas grupos éter, creando una serie de nuevos compuestos que se comportan como parientes cercanos del fármaco original. Cuando probaron estas variantes contra H. pylori en el laboratorio, algunas resultaron hasta 60 veces más potentes que el metronidazol, deteniendo el crecimiento bacteriano a concentraciones diminutas. Es importante destacar que este aumento no se debió simplemente a que el fármaco se activara más fácilmente mediante la química redox estándar, lo que sugiere que las moléculas modificadas deben estar haciendo algo cualitativamente distinto dentro de la célula bacteriana.
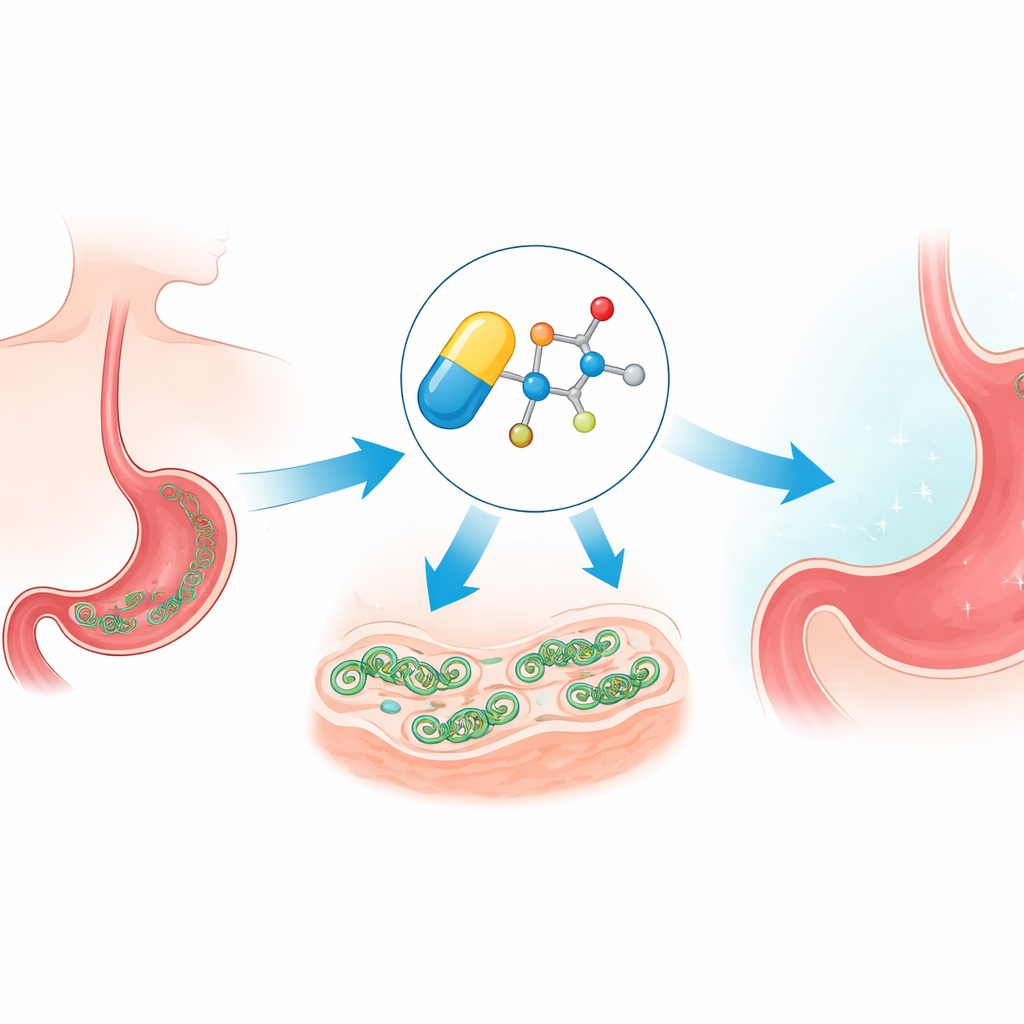
Cómo el fármaco se infiltra y sobrecarga la célula
El metronidazol es lo que se llama un profármaco: una vez que penetra en un microbio, su grupo nitro se reduce químicamente para formar especies radicalarias agresivas. Estos fragmentos reactivos atacan moléculas vitales como el ADN y las proteínas, generando estrés oxidativo. El equipo confirmó que las nuevas versiones éter siguen este camino, generando estrés dentro de H. pylori. Pero dado que estas reacciones dependen de condiciones de bajo oxígeno, los compuestos permanecen mayormente inactivos en tejidos humanos bien oxigenados, lo que ayuda a explicar por qué esta familia de fármacos ha sido útil contra microbios y relativamente segura para los pacientes.
Golpeando a los equipos de rescate de la bacteria
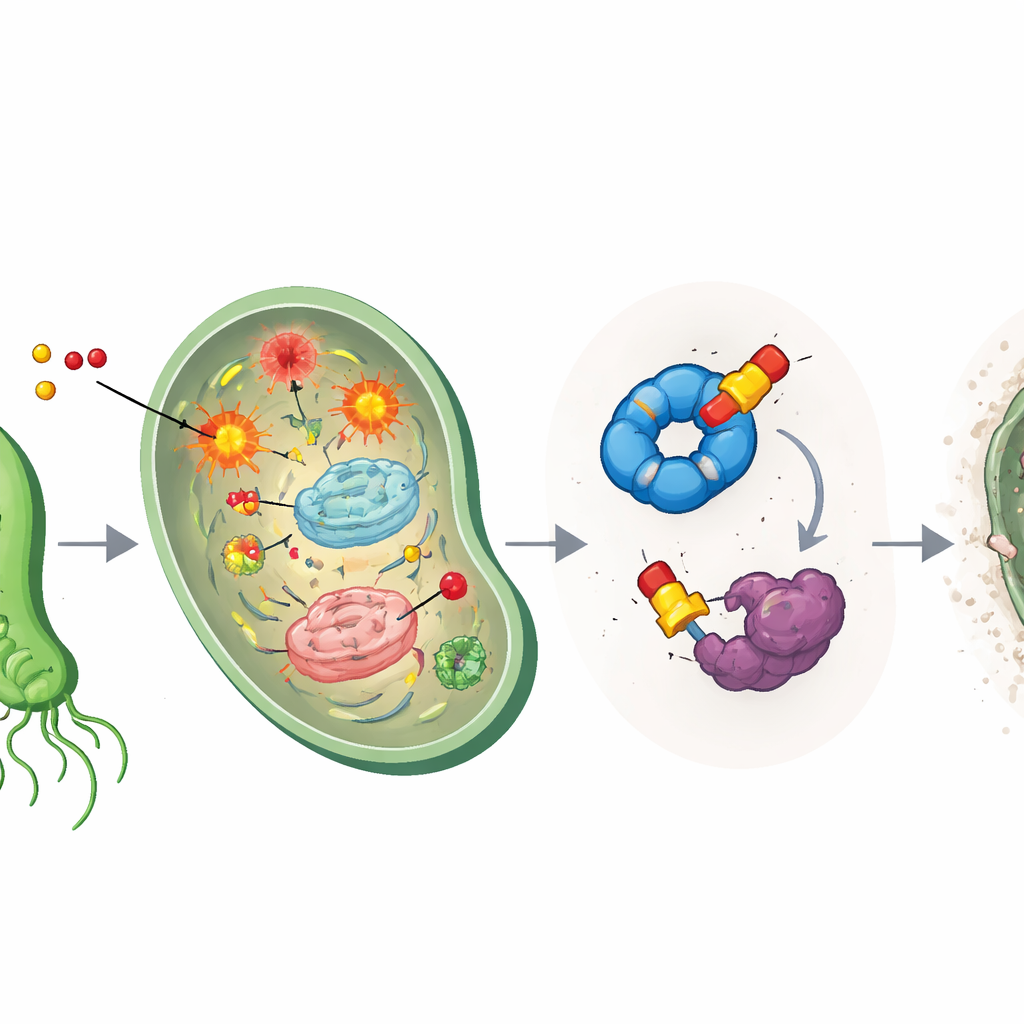
Para averiguar qué más hacían los fármacos modificados, los científicos usaron perfiles de proteínas basados en actividad, un método químico de pesca en el que sondas similares a fármacos se adhieren a sus objetivos y pueden ser extraídas e identificadas. Esto reveló dos principales «capturas» proteicas en H. pylori: un ayudante de plegamiento llamado HpGroEL, que actúa como chaperona para replegar proteínas dañadas, y una enzima llamada HpTpx, que neutraliza peróxidos dañinos y protege el ADN del daño oxidativo. Los compuestos basados en éter se unieron especialmente con fuerza a HpTpx, formando enlaces permanentes en una cisteína crítica del sitio activo y reduciendo drásticamente su capacidad para detoxificar peróxidos. En efecto, los fármacos tanto crean caos oxidativo como inutilizan al cuerpo de bomberos celular al mismo tiempo.
Del tubo de ensayo al estómago del ratón
Los antibióticos potentes solo son útiles si se comportan bien en el organismo, por lo que el equipo examinó la toxicidad y cómo se distribuyen las nuevas moléculas en sistemas animales. En cultivos de células humanas, los derivados éter mostraron muy baja toxicidad, y las pruebas de estabilidad química indicaron que sobreviven bien en el plasma sanguíneo. Los estudios farmacocinéticos en ratones destacaron un compuesto sobresaliente, MF‑01, que alcanzó niveles favorables en el intestino manteniendo buena estabilidad. En un modelo de infección por H. pylori que imita el tratamiento humano—usando una combinación con claritromicina y un bloqueador de ácido gástrico—MF‑01 eliminó por completo la bacteria a aproximadamente una cincuentava parte de la dosis estándar de metronidazol. A dosis tan bajas, el impacto general sobre el microbioma intestinal normal fue más leve que con la terapia triple convencional, y las bacterias intestinales beneficiosas comunes en ratones fueron menos sensibles a MF‑01 que al metronidazol.
Qué significa esto para pacientes y fármacos futuros
En conjunto, el trabajo muestra que el metronidazol y sus derivados éter actúan mediante un poderoso doble golpe: desencadenan estrés oxidativo dentro de H. pylori mientras bloquean simultáneamente sistemas clave de respuesta al estrés que normalmente rescatarían la célula. Este ataque dual explica el aumento dramático de la potencia y sugiere que derivados cuidadosamente ajustados podrían revivir y mejorar una clase de antibióticos envejecida. Dado que estas nuevas moléculas derivan de un fármaco aprobado desde hace tiempo, parten con ventaja en la evaluación de seguridad. Si futuros estudios clínicos confirman los resultados en ratones, compuestos como MF‑01 podrían permitir regímenes más cortos y con dosis más bajas que curen con mayor fiabilidad las infecciones por H. pylori y sean más respetuosos con el resto del ecosistema intestinal.
Cita: Fiedler, M.K., Pandler, M.S.I., Gong, R. et al. Metronidazole and ether derivatives target Helicobacter pylori via simultaneous stress induction and inhibition. Nat Microbiol 11, 1049–1063 (2026). https://doi.org/10.1038/s41564-026-02291-w
Palabras clave: Helicobacter pylori, metronidazol, resistencia a antibióticos, estrés oxidativo, microbioma intestinal