Clear Sky Science · zh
通过噻吩 S,S-氧化物环加成实现 Strychnos 生物碱的集体不对称合成
为什么这些受毒素启发的小分子重要
Strychnos 生物碱是一类以极强活性著称的天然化合物——士的宁就是臭名昭著的例子——并以其复杂纠结的三维构型闻名。这些分子长期以来吸引化学家们的兴趣,因为它们既危险又可能有用,部分化合物在对抗耐药性癌症方面显示出潜力。然而,它们的结构复杂性使得在实验室中构建非常困难。本文揭示了一种新的、简化的策略,能够以受控且高效的方式构建多种 Strychnos 分子,为更安全的研究以及从这些曾经可怕的毒素衍生出潜在新药打开了大门。
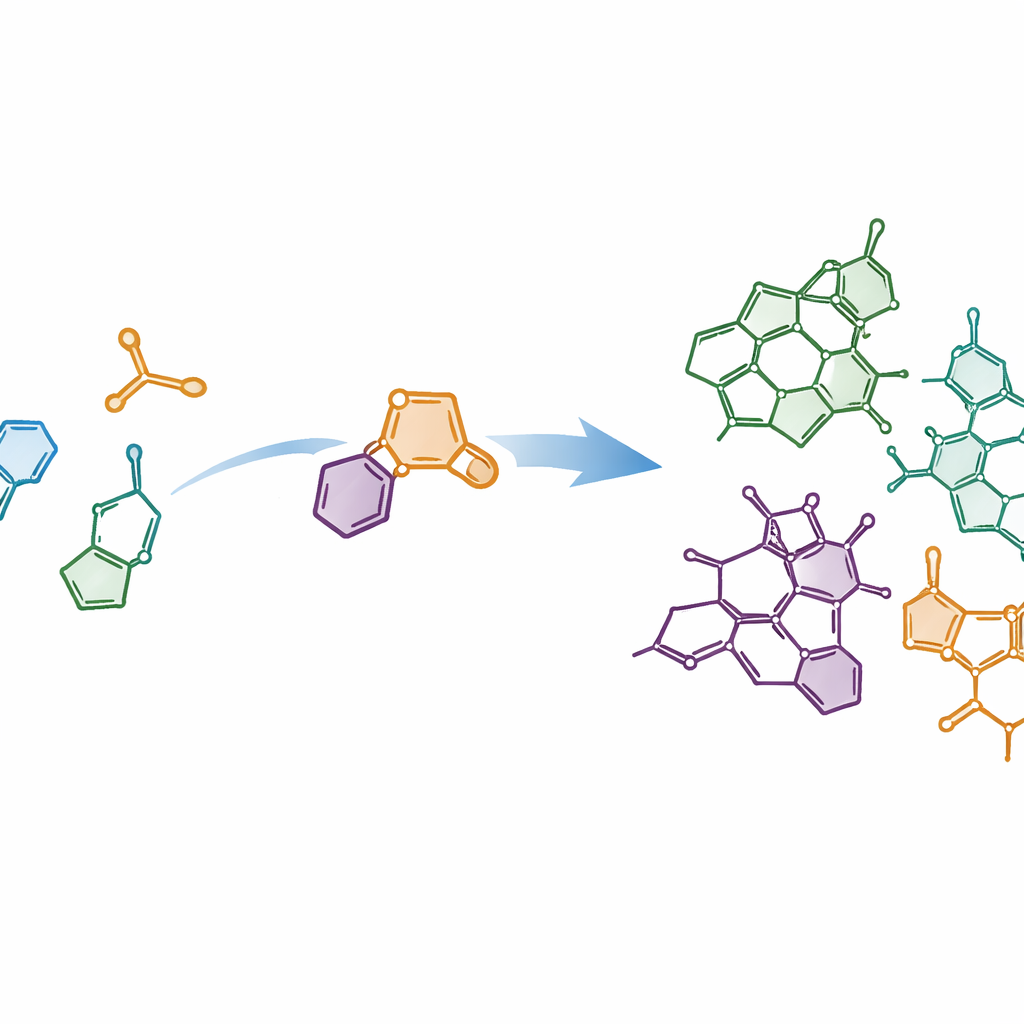
用简单片段构建复杂构型
作者旨在满足现代化学合成的理想:反应步骤短、废物少,并且能够从共同路径产生多种相关分子。他们聚焦于 Strychnos 生物碱共有的致密多环“核心”,并探讨是否能用更简单的构件在少数步骤内把这个框架拼装起来。他们的方案依赖于将一个吲哚片段——生物学中常见的母核——与一种特殊的伙伴噻吩 S,S-二氧化物连接。当两者相遇时,会发生一种强有力的成环事件,称为 Diels–Alder 环加成,随后伴随二氧化硫的清除。这个级联反应把相对平面的起始片段在本质上一举转化为复杂的三维环系。
一种通用的化学捷径
为了将这一理念变为实用工具箱,团队首先开发了高度选择性的环加成反应版本。通过在噻吩 S,S-二氧化物上引入便宜的手性“把手”(樟脑磺酰胺基团),他们能够引导反应几乎只生成一种镜像产物——这是生物活性分子非常重要的特征,因为镜像体往往具有截然不同的生物行为。他们展示了各种带不同取代基的吲哚底物在温和条件下都能顺利反应,作为单一缩合异构体给出三环吲哚啉产物。这些产物不仅是通往 Strychnos 生物碱的中间体,也本身是很有吸引力的医药化学骨架。
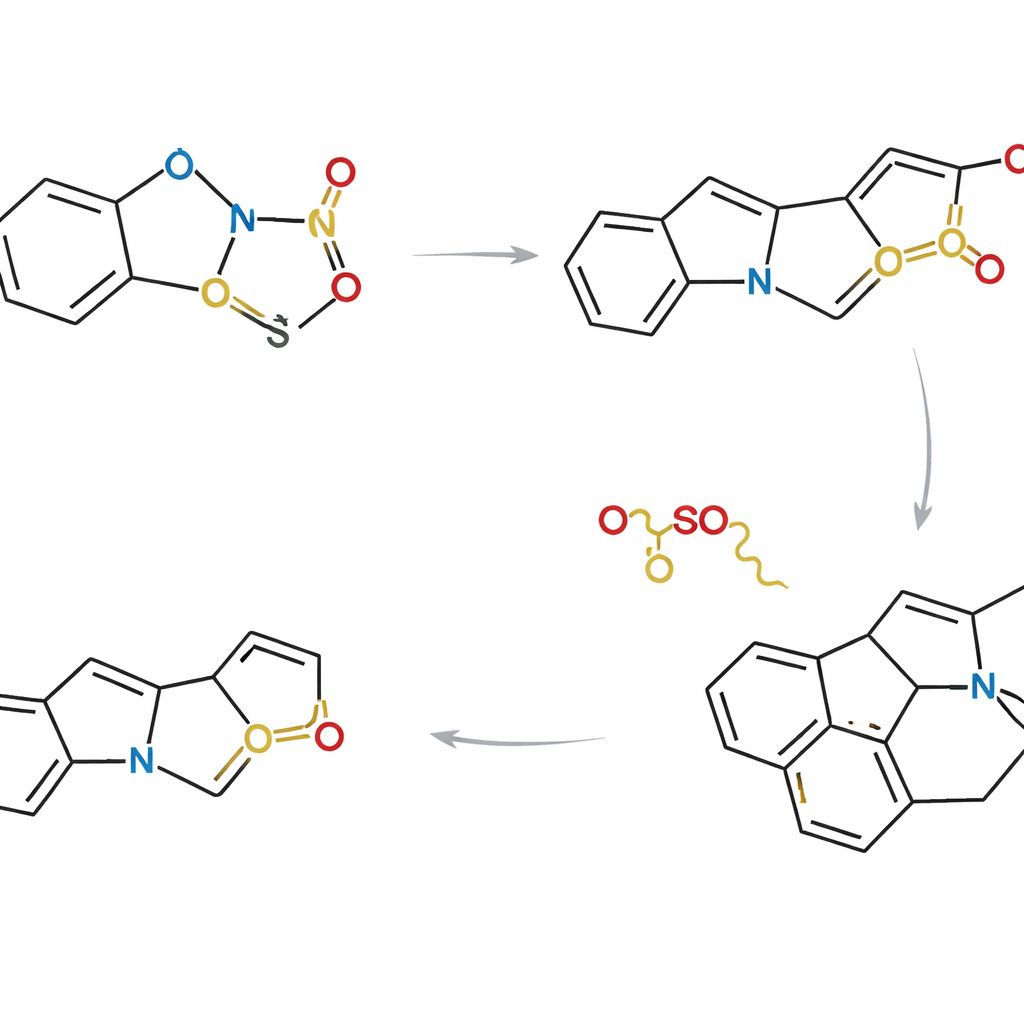
用一套策略收集多种天然产物
在掌握了这种控制能力后,研究人员设计了三条互补路线,区别在于吲哚和噻吩片段何时何地连接。在一种方法中,两片段在环加成前被系在一起,使反应在单个分子内发生。其他方法则先让它们作为独立分子反应,然后再进行内环闭合。通过精心选择取代基和反应顺序,团队能够收敛到一个处于 Strychnos 系谱分支点的共同高级中间体。从这一共享骨架出发,他们完成了八种天然产物的不对称合成,包括 akuammicine、lagumicine、norfluorocurarine、若干 alstolucine 和 echitamidine——通常是迄今报道的最短且最节原子的路线。
攻克百年合成难题
最引人注目的示例之一是首次全合成布鲁辛(brucine),这是一种与士的宁亲缘关系很近的化合物,已知超过200年并被广泛用作手性分离剂,但此前从未被完整地从头合成。布鲁辛的吲哚啉环电子密度异常高且容易降解,这阻碍了以往的合成尝试。通过针对性调整他们基于噻吩的级联反应并谨慎控制反应条件,作者仅用九步线性步骤便从一种简单的商业起始物构筑出了布鲁辛的精细骨架。他们还实现了士的宁本身的十步不对称合成,这是迄今报道的最简洁手性路线。
用机器学习“观看”反应
为了理解为什么这些反应能产生如此精确的结果,团队将高水平量子化学与现代机器学习模拟相结合。这些计算表明,在某些情况下,反应并非以单一平滑方式进行,而是通过不均匀的逐步过程:一对碳—碳键先形成,短暂经过一个浅能量的中间体,然后几乎自发地排出二氧化硫,体系沿能量面下滑。手性樟脑磺酰胺侧链微妙地偏置了这一途径,使得一种三维构型比另一种更容易被到达。这一机理洞见为设计超出 Strychnos 家族的新型噻吩级联反应提供了指导。
从致命毒素到有用工具
总体而言,该研究表明噻吩 S,S-二氧化物可作为强大且可编程的“预装弹簧”单元,用于拼装复杂的分子结构。通过利用它们固有的失去二氧化硫的驱动力,作者设计划链反应,能以高选择性和最少的无谓步骤将简单片段快速转化为 Strychnos 生物碱那样纠结的环系。对非专业读者而言,核心结论是:化学家们正学会将连带臭名的毒素转变为多功能的发现平台,借助巧妙的反应设计和计算洞察,比以往更高效地探索复杂的化学空间。
引用: Park, K.H.‘., Park, J., Frank, N. et al. Collective asymmetric synthesis of the Strychnos alkaloids via thiophene S,S-dioxide cycloadditions. Nat. Chem. 18, 782–789 (2026). https://doi.org/10.1038/s41557-025-02041-1
关键词: Strychnos 生物碱, 不对称合成, 环加成级联反应, 噻吩 S,S-二氧化物, 天然产物化学