Clear Sky Science · pl
Kolektywna asymetryczna synteza alkaloidów Strychnos przez cykloadycje tiofenów S,S‑tlenków
Dlaczego małe molekuły inspirowane truciznami mają znaczenie
Alkaloidy Strychnos to rodzina związków naturalnych znana ze swojej ogromnej mocy — najsłynniejszym przykładem jest strychnina — oraz z misternych, trójwymiarowych kształtów. Te molekuły od dawna fascynują chemików, ponieważ są jednocześnie niebezpieczne i potencjalnie użyteczne; niektóre wykazują obiecujące działanie wobec nowotworów opornych na leczenie. Ich architektoniczna złożoność sprawia jednak, że bardzo trudno je zbudować w laboratorium. W artykule przedstawiono nową, uproszczoną metodę konstruowania wielu różnych cząsteczek Strychnos w sposób kontrolowany i wydajny, co otwiera drogę do bezpieczniejszych badań i możliwych nowych leków pochodzących od tych niegdyś budzących grozę trucizn.
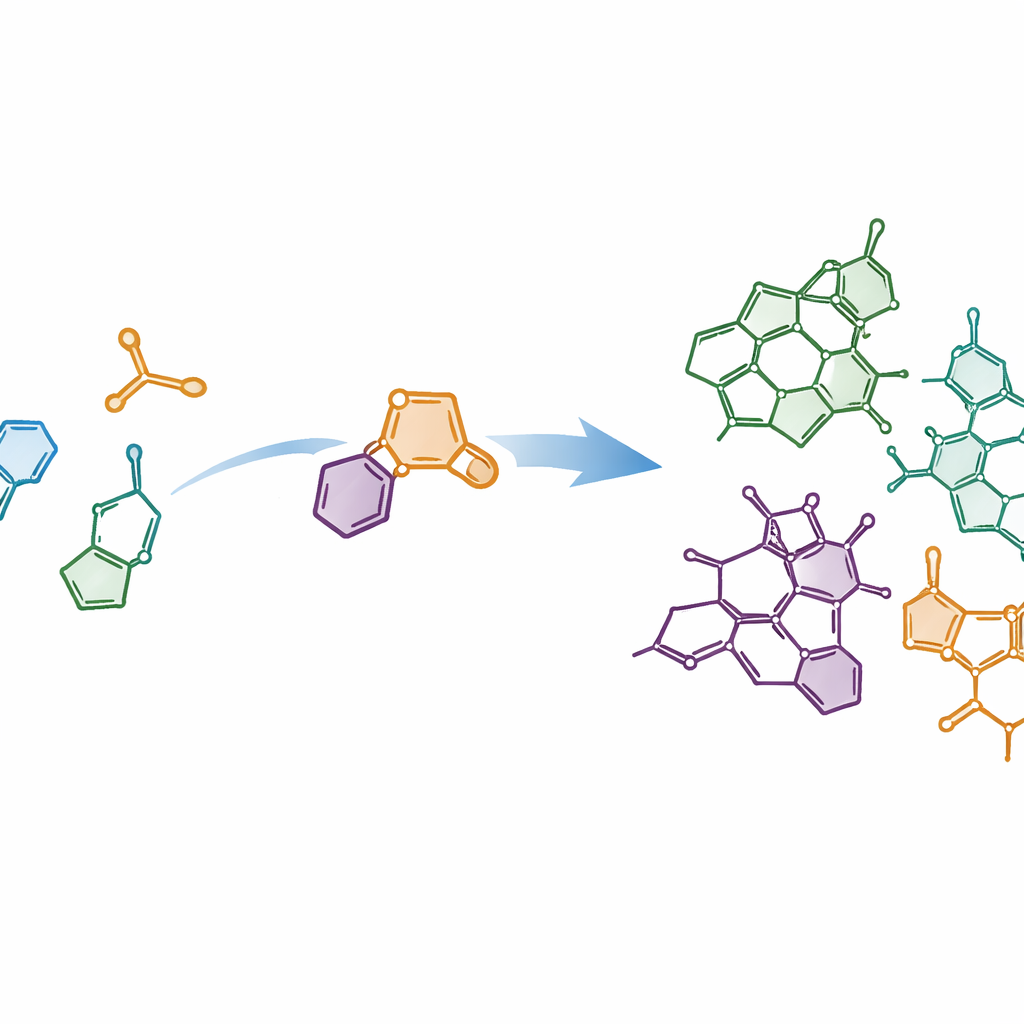
Budowanie złożonych kształtów z prostych elementów
Autorzy postawili sobie za cel spełnienie współczesnych ideałów syntezy chemicznej: reakcji krótkich, oszczędnych pod względem odpadów i pozwalających uzyskać wiele spokrewnionych związków z jednego wspólnego szlaku. Skoncentrowali się na gęsto upakowanym, wieloringowym „rdzeniu” wspólnym dla alkaloidów Strychnos i zastanawiali się, czy tę ramę da się złożyć z prostszych elementów w zaledwie kilku etapach. Plan opierał się na połączeniu fragmentu indolowego — powszechnego szkielety w biologii — z wyspecjalizowanym partnerem zwanym tiofenem S,S‑tlenkiem. Gdy te dwa elementy się spotkają, przechodzą potężne tworzenie pierścienia zwane cykloadycją Dielsa–Aldera, a następnie następuje czysta utrata dwutlenku siarki. Ta kaskada przekształca stosunkowo płaskie cząsteczki wyjściowe w skomplikowane, trójwymiarowe układy pierścieniowe w zasadzie jednym ruchem.
Wszechstronny chemiczny skrót
Aby zamienić ten pomysł w praktyczne narzędzie, zespół najpierw opracował wysoce selektywne wersje tych reakcji cykloadycji. Poprzez przyłączenie taniej, chiralnej „rączki” (grupy kamforosultamu) do tiofenu S,S‑tlenku mogli skierować reakcję tak, by powstawał niemal wyłącznie jeden produkt będący lustrzanym odbiciem — kluczowa cecha dla molekuł bioaktywnych, które często zachowują się zupełnie inaczej niż ich lustrzane bliźniaki. Pokazali, że szeroki zakres partnerów indolowych, niosących różne podstawienia, reaguje gładko w łagodnych warunkach, dając produkty trójpierścieniowe typu indoliny jako pojedyncze diastereomery. Produkty te nie są tylko etapami pośrednimi w kierunku alkaloidów Strychnos, lecz same w sobie stanowią atrakcyjne szkielety dla chemii medycznej.
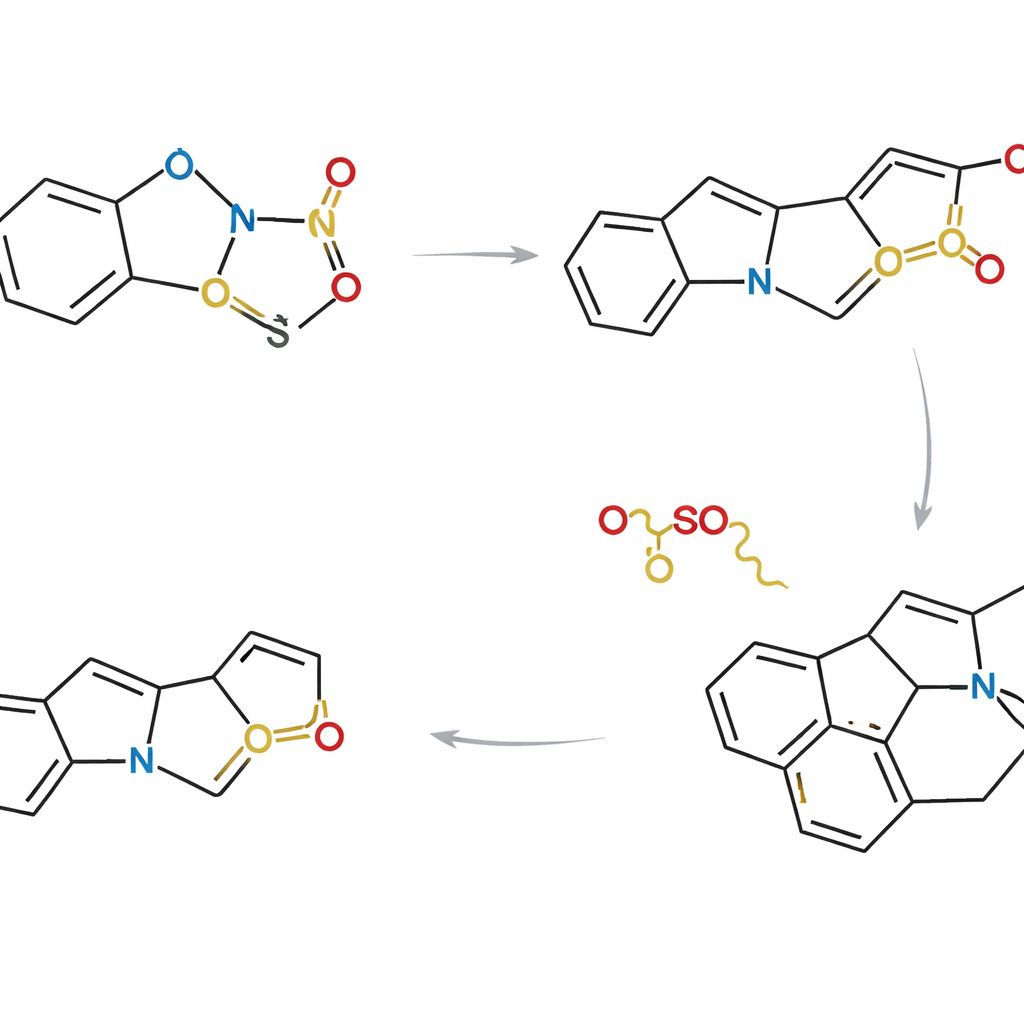
Zbieranie wielu produktów naturalnych w jednej strategii
Uzbrojeni w taką kontrolę, badacze zaprojektowali trzy komplementarne drogi różniące się tym, jak i kiedy fragmenty indolowe i tiofenowe są łączone. W jednym podejściu dwa fragmenty są zespolone przed cykloadycją, więc reakcja zachodzi wewnątrz jednej cząsteczki. W innych najpierw reagują jako odrębne molekuły, a następnie poddawane są wewnętrznemu zamknięciu pierścienia. Poprzez ostrożny dobór podstawień i sekwencji reakcji zespół mógł zbiec do wspólnego zaawansowanego intermediatу, który leży w punkcie rozgałęzienia drzewa rodowego alkaloidów Strychnos. Z tego wspólnego szkieletu zrealizowali asymetryczne syntezy ośmiu produktów naturalnych, w tym akuamycyny, lagumicyny, norfluorokurariny, kilku alstolucyn i echitamidyny — często w najkrótszych i najbardziej atomowo wydajnych szlakach opisanych do tej pory.
Rozwiązanie wieku‑starego wyzwania syntetycznego
Jednym z najbardziej uderzających pokazów jest pierwsza całkowita synteza brucyny, bliskiego chemicznego kuzyna strychniny, znanego od ponad 200 lat i szeroko stosowanego jako czynnik rozdzielający enancjomery, lecz nigdy wcześniej w pełni zsyntetyzowanego od podstaw. Pierścień indolinowy brucyny jest wyjątkowo bogaty elektronowo i podatny na degradację, co zniechęcało wcześniejsze próby. Poprzez dostosowanie kaskady opartej na tiofenie i staranne panowanie nad warunkami reakcji autorom udało się ukształtować delikatny szkielet brucyny w zaledwie dziewięciu krokach liniowych, zaczynając od prostego, komercyjnie dostępnego materiału wyjściowego. Osiągnęli także dziesięciokrokową syntezę asymetryczną samej strychniny, będącą jak dotąd najbardziej zwięzłą chiralną drogą opisaną w literaturze.
Obserwowanie reakcji za pomocą uczenia maszynowego
Aby zrozumieć, dlaczego ich reakcje dają tak precyzyjne wyniki, zespół połączył wysokopoziomową chemię kwantową z nowoczesnymi symulacjami uczenia maszynowego. Obliczenia te wykazały, że w niektórych przypadkach reakcja nie przebiega jednym płynnym ruchem, lecz przez nierówny, stopniowy taniec: najpierw tworzy się jedno wiązanie węglowo‑węglowe, krótko odwiedzany jest płytki intermediat, a następnie dwutlenek siarki jest wydalany niemal spontanicznie, gdy system zsuwa się po krajobrazie energetycznym. Chiralny łańcuch boczny kamforosultamu subtelnie faworyzuje tę ścieżkę, czyniąc jedna trójwymiarową aranżację znacznie łatwiejszą do osiągnięcia niż drugą. Ten wgląd mechanistyczny daje wskazówki do projektowania nowych kaskad opartych na tiofenach poza rodziną Strychnos.
Od śmiertelnych trucizn do użytecznych narzędzi
Podsumowując, badanie pokazuje, że tiofeny S,S‑tlenki mogą działać jako potężne, programowalne „sprężynujące” elementy do składania zawiłych architektur molekularnych. Wykorzystując ich wrodzoną skłonność do utraty dwutlenku siarki, autorzy opracowali reakcje kaskadowe, które szybko przekształcają proste fragmenty w poplątane systemy pierścieniowe alkaloidów Strychnos z wysoką selektywnością i minimalną liczbą zbędnych etapów. Dla osób niebędących specjalistami płynąca stąd konkluzja jest taka, że chemicy uczą się przekształcać nawet słynne trucizny w wszechstronne platformy odkrywcze, wykorzystując sprytne projektowanie reakcji i obliczeniowy wgląd, by badać złożoną przestrzeń chemiczną wydajniej niż kiedykolwiek wcześniej.
Cytowanie: Park, K.H.‘., Park, J., Frank, N. et al. Collective asymmetric synthesis of the Strychnos alkaloids via thiophene S,S-dioxide cycloadditions. Nat. Chem. 18, 782–789 (2026). https://doi.org/10.1038/s41557-025-02041-1
Słowa kluczowe: Alkaloidy Strychnos, synteza asymetryczna, kaskady cykloadycji, tiofeny S,S‑tlenki, chemia związków naturalnych