Clear Sky Science · de
Kollektive asymmetrische Synthese der Strychnos‑Alkaloide über Cycloadditionen von Thiophen‑S,S‑dioxiden
Warum winzige, von Giften inspirierte Moleküle wichtig sind
Die Strychnos‑Alkaloide sind eine Familie natürlicher Verbindungen, bekannt für ihre extreme Wirksamkeit — Strychnin ist das berüchtigte Beispiel — und für ihre verschachtelten, dreidimensionalen Formen. Diese Moleküle faszinieren Chemiker seit langem, weil sie zugleich gefährlich und potenziell nützlich sind; einige zeigen vielversprechende Aktivität gegen medikamentenresistente Krebsarten. Ihre architektonische Komplexität macht sie jedoch im Labor nur schwer zugänglich. Diese Arbeit stellt einen neuen, gestrafften Weg vor, um viele verschiedene Strychnos‑Moleküle kontrolliert und effizient herzustellen, was Türen öffnet für sicherere Untersuchungen und mögliche neue Arzneimittel, die aus diesen einst gefürchteten Giften abgeleitet sind.
Komplexe Formen aus einfachen Bausteinen aufbauen
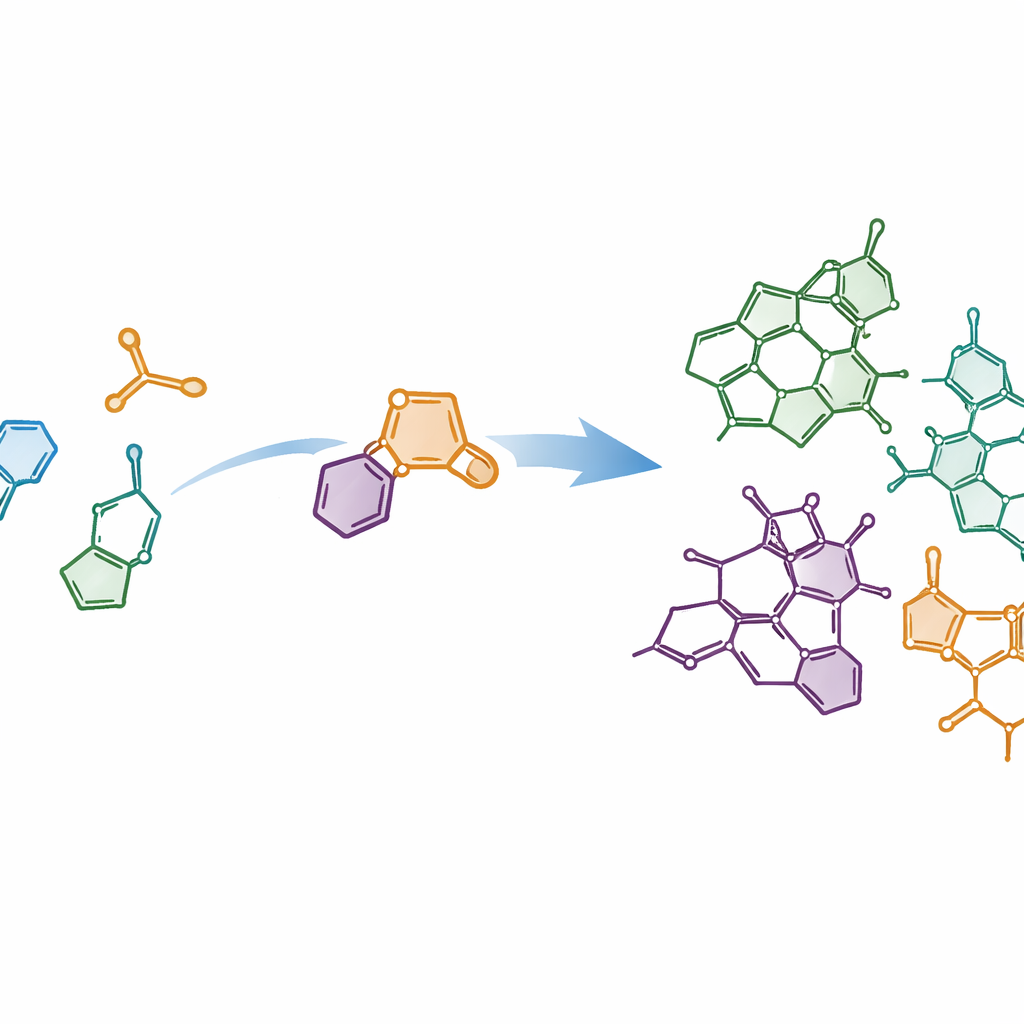
Die Autoren verfolgten zeitgemäße Ideale chemischer Synthese: Reaktionen, die kurz, abfallarm und in der Lage sind, mehrere verwandte Moleküle aus einem gemeinsamen Weg zu liefern. Sie konzentrierten sich auf das dichte, ringreiche „Kernstück“, das allen Strychnos‑Alkaloiden gemein ist, und fragten, ob dieses Gerüst aus einfacheren Bausteinen in nur wenigen Schritten zusammengesetzt werden kann. Ihr Plan beruhte darauf, ein Indolfragment — ein in der Biologie häufiges Grundgerüst — mit einem speziellen Partner zu verbinden: einem Thiophen‑S,S‑dioxid. Treffen diese beiden aufeinander, durchlaufen sie ein kraftvolles Ringbildungsverhalten, eine Diels–Alder‑Cycloaddition, gefolgt vom sauberen Verlust von Schwefeldioxidgas. Diese Kaskade verwandelt relativ flache Ausgangsstücke in komplexe, dreidimensionale Ringsysteme im Wesentlichen in einem Schritt.
Eine vielseitige chemische Abkürzung
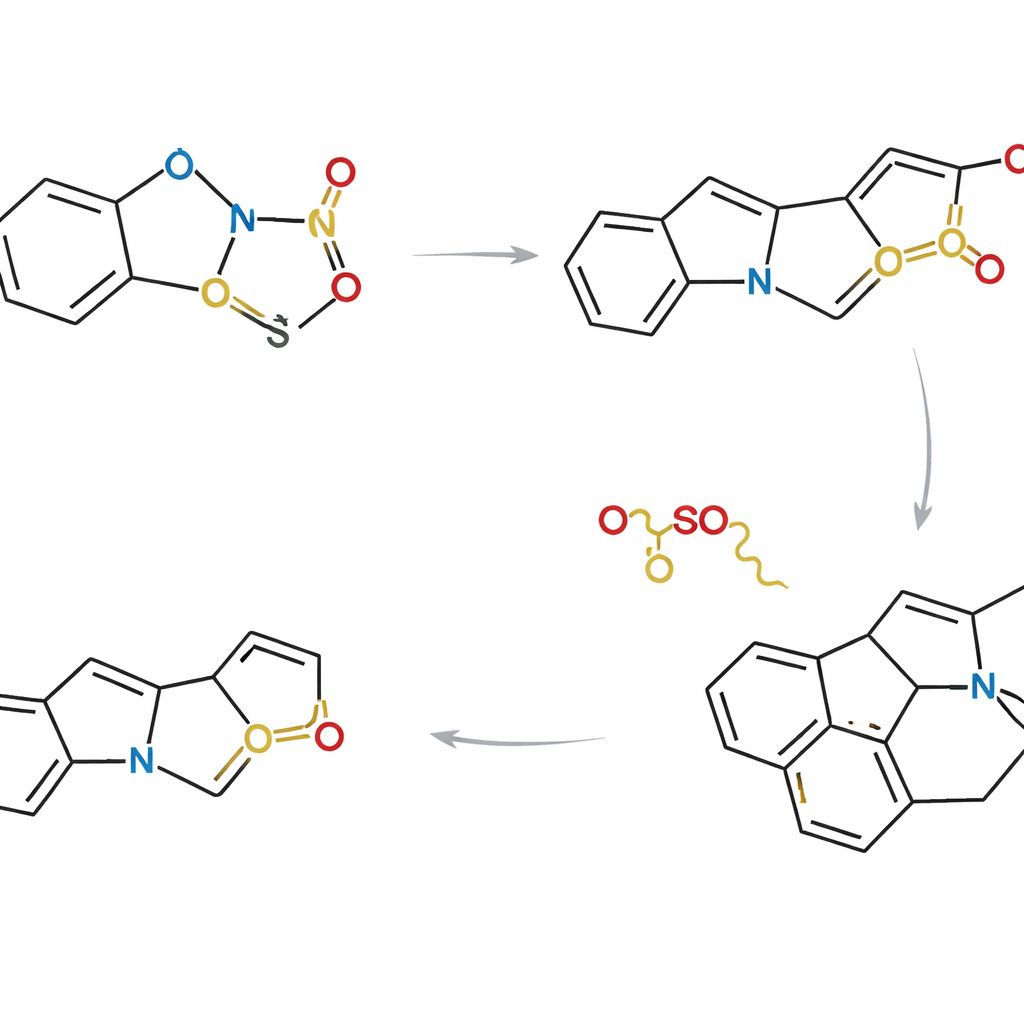
Um diese Idee in ein praktisches Werkzeug zu überführen, entwickelte das Team zunächst hochselektive Varianten dieser Cycloadditionsreaktionen. Durch das Anbringen eines günstigen, chiralen „Griffs“ (einer Camphorsultamgruppe) am Thiophen‑S,S‑dioxid konnten sie die Reaktion so lenken, dass nahezu ausschließlich ein Spiegelbildprodukt entsteht — ein entscheidendes Merkmal für bioaktive Moleküle, die sich oft sehr unterschiedlich von ihren Spiegelbildisomeren verhalten. Sie zeigten, dass eine breite Palette von Indolpartnern mit unterschiedlichen Substituenten unter milden Bedingungen glatt reagieren und trizyklische Indolinprodukte als einzelne Diastereomere liefern. Diese Produkte sind nicht nur Zwischenstufen zu Strychnos‑Alkaloiden, sondern auch attraktive Gerüste für die Wirkstoffforschung an sich.
Viele Naturstoffe mit einer Strategie sammeln
Mit dieser Kontrolle entwarfen die Forscher drei komplementäre Routen, die sich darin unterscheiden, wie und wann die Indol‑ und Thiophen‑Partner verbunden werden. In einem Ansatz sind die beiden Fragmente vor der Cycloaddition miteinander gekoppelt, sodass die Reaktion innerhalb eines einzelnen Moleküls stattfindet. In anderen reagieren sie zunächst als getrennte Moleküle und schließen dann intern zu Ringen. Durch die sorgfältige Auswahl von Substituenten und Reaktionssequenzen konnte das Team auf ein gemeinsames fortgeschrittenes Zwischenprodukt zulaufen, das am Verzweigungspunkt des Strychnos‑Familienbaums steht. Von diesem gemeinsamen Gerüst aus vollendeten sie asymmetrische Synthesen von acht Naturstoffen, darunter Akuammicin, Lagumicin, Norfluorocurarin, mehrere Alstolucine und Echitamidin — oft auf den kürzesten und am atomökonomischsten gemeldeten Routen bis heute.
Eine hundertjährige Syntheseherausforderung knacken
Eines der eindrucksvollsten Ergebnisse ist die erste Totalsynthese von Brucin, einem nahen chemischen Verwandten des Strychnins, der seit mehr als 200 Jahren bekannt und weit verbreitet als chirales Auflösungsmittel verwendet wird, aber noch nie vollständig von Grund auf aufgebaut worden war. Brucins Indolinring ist ungewöhnlich elektronreich und degradiert leicht, was frühere Versuche entmutigt hatte. Durch die Anpassung ihrer thiophenbasierten Kaskade und die sorgfältige Steuerung der Reaktionsbedingungen konnten die Autoren Brucins empfindliches Gerüst in nur neun linearen Schritten aus einem einfachen, kommerziell erhältlichen Ausgangsstoff formen. Außerdem gelang ihnen eine zehnstufige asymmetrische Synthese von Strychnin selbst — die bisher prägnanteste chirale Route.
Reaktionen mit maschinellem Lernen beobachten
Um zu verstehen, warum ihre Reaktionen so präzise Ergebnisse liefern, kombinierten die Forscher hochrangige Quantenchemie mit modernen maschinellen Lernsimulationen. Diese Berechnungen zeigten, dass die Reaktion in einigen Fällen nicht in einer gleichmäßigen Bewegung abläuft, sondern durch einen ungleichmäßigen, schrittweisen Tanz: Zuerst bildet sich eine Kohlenstoff‑Kohlenstoff‑Bindung, ein seichtes Zwischenprodukt wird kurz besucht und dann wird Schwefeldioxid nahezu spontan freigesetzt, während das System das Energielandscape hinabgleitet. Die chirale Camphorsultam‑Seitenkette neigt diesen Pfad subtil, sodass eine dreidimensionale Anordnung deutlich leichter erreichbar ist als die andere. Diese mechanistischen Einsichten liefern Richtlinien für die Gestaltung neuer thiophenbasierter Kaskaden über die Strychnos‑Familie hinaus.
Von tödlichen Toxinen zu nützlichen Werkzeugen
Insgesamt zeigt die Studie, dass Thiophen‑S,S‑dioxide als leistungsstarke, programmierbare „federbelastete“ Bausteine dienen können, um komplexe molekulare Architekturen zusammenzuschnappen. Indem sie deren eingebauten Drang, Schwefeldioxid zu verlieren, nutzten, entwickelten die Autoren Kaskadenreaktionen, die einfache Fragmente schnell und mit hoher Selektivität sowie minimalen Verlustschritten in die verschlungenen Ringsysteme der Strychnos‑Alkaloide umwandeln. Für Nicht‑Spezialisten ist die Botschaft, dass Chemiker lernen, selbst berüchtigte Gifte in vielseitige Plattformen für Entdeckungen zu verwandeln — mithilfe cleverer Reaktionsgestaltung und rechnerischer Einsicht, um komplexeren chemischen Raum effizienter als je zuvor zu erkunden.
Zitation: Park, K.H.‘., Park, J., Frank, N. et al. Collective asymmetric synthesis of the Strychnos alkaloids via thiophene S,S-dioxide cycloadditions. Nat. Chem. 18, 782–789 (2026). https://doi.org/10.1038/s41557-025-02041-1
Schlüsselwörter: Strychnos‑Alkaloide, asymmetrische Synthese, Cycloadditionskaskaden, Thiophen‑S,S‑dioxide, Naturstoffchemie