Clear Sky Science · sv
Kollektiv asymmetrisk syntes av Strychnos‑alkaloider via cykloadditioner med tiofendioxid (S,S)
Varför små, giftinspirerade molekyler är viktiga
Strychnos‑alkaloiderna är en familj naturliga föreningar kända för sin extrema potens — stryknin är det ökända exemplet — och för sina intrikata, tredimensionella former. Dessa molekyler har länge fascinerat kemister eftersom de både är farliga och potentiellt användbara; några visar lovande egenskaper mot läkemedelsresistenta cancerformer. Deras arkitektoniska komplexitet gör dem dock mycket svåra att bygga i laboratorium. Denna artikel presenterar en ny, förenklad metod för att konstruera många olika Strychnos‑molekyler på ett kontrollerat och effektivt sätt, vilket öppnar dörrar för säkrare studier och möjliga nya läkemedel härledda från dessa tidigare fruktade gifter.
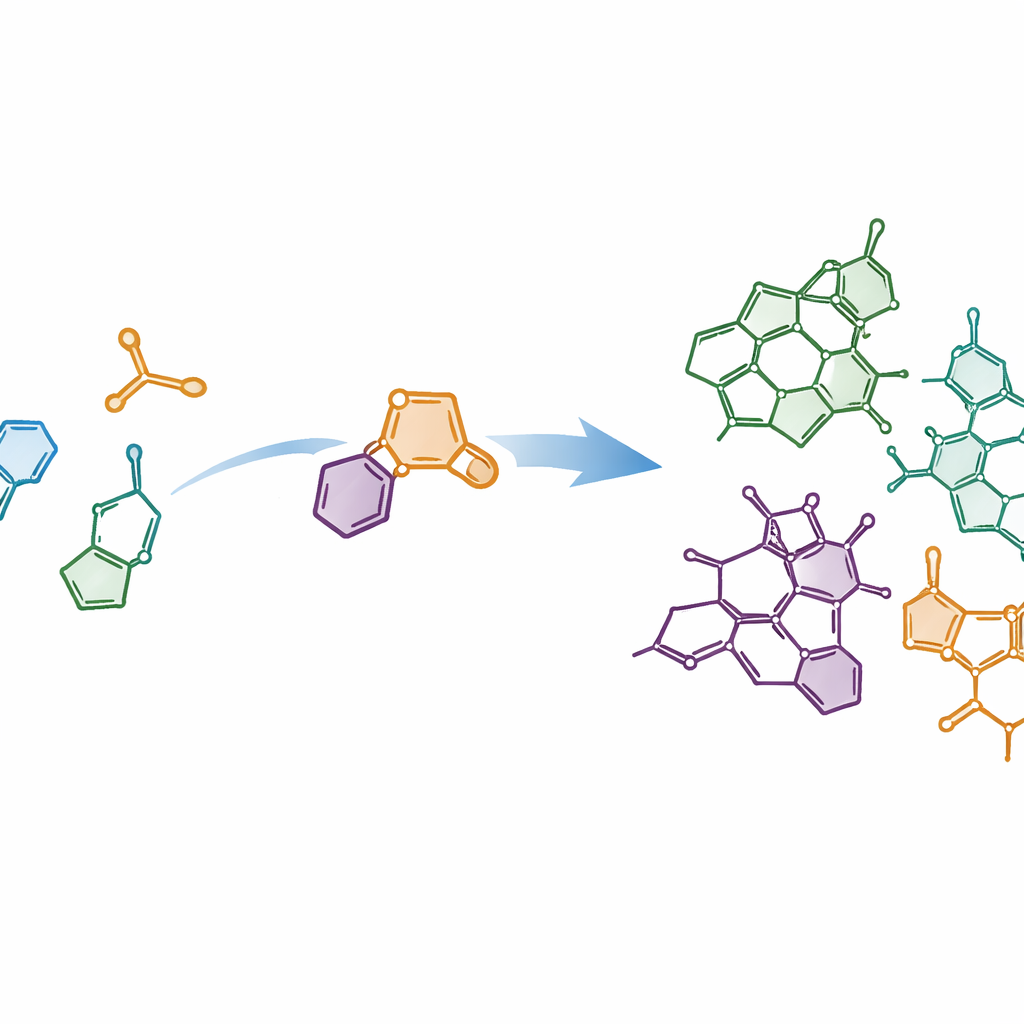
Bygga komplexa former från enkla delar
Författarna strävade efter moderna ideal inom kemisk syntes: reaktioner som är korta, sparsamma med avfall och som kan producera flera besläktade molekyler från en gemensam väg. De koncentrerade sig på den tätt ringpackade ”kärnan” som delas av Strychnos‑alkaloiderna och undersökte om detta ramverk kunde sättas ihop från enklare byggstenar på bara några steg. Deras plan byggde på att förena ett indolfragment — en vanlig biologisk stomme — med en speciell partner kallad tiofen S,S‑dioxid. När dessa två möts genomgår de en kraftfull ringbildande händelse kallad Diels–Alder‑cykloaddition, följd av en ren förlust av svaveldioxidgas. Denna kaskad omvandlar relativt platta utgångsdelar till komplexa, tredimensionella ringsystem i praktiskt taget ett enda slag.
En mångsidig kemisk genväg
För att förvandla idén till en praktisk verktygslåda utvecklade teamet först mycket selektiva versioner av dessa cykloadditioner. Genom att fästa ett billigt, kiralt ”handtag” (en kamforsultam‑grupp) på tiofen S,S‑dioxiden kunde de styra reaktionen så att nästan uteslutande en spegelbildsprodukt bildades — en avgörande egenskap för bioaktiva molekyler, som ofta uppför sig mycket olika från sina spegelvända tvillingar. De visade att en mängd olika indolpartner, med många olika substituenter, reagerar smidigt under milda förhållanden för att ge tricykliska indolinprodukter som enstaka diastereomerer. Dessa produkter är inte bara mellanprodukter till Strychnos‑alkaloider utan utgör också attraktiva ramar för läkemedelskemisk utveckling i sig.
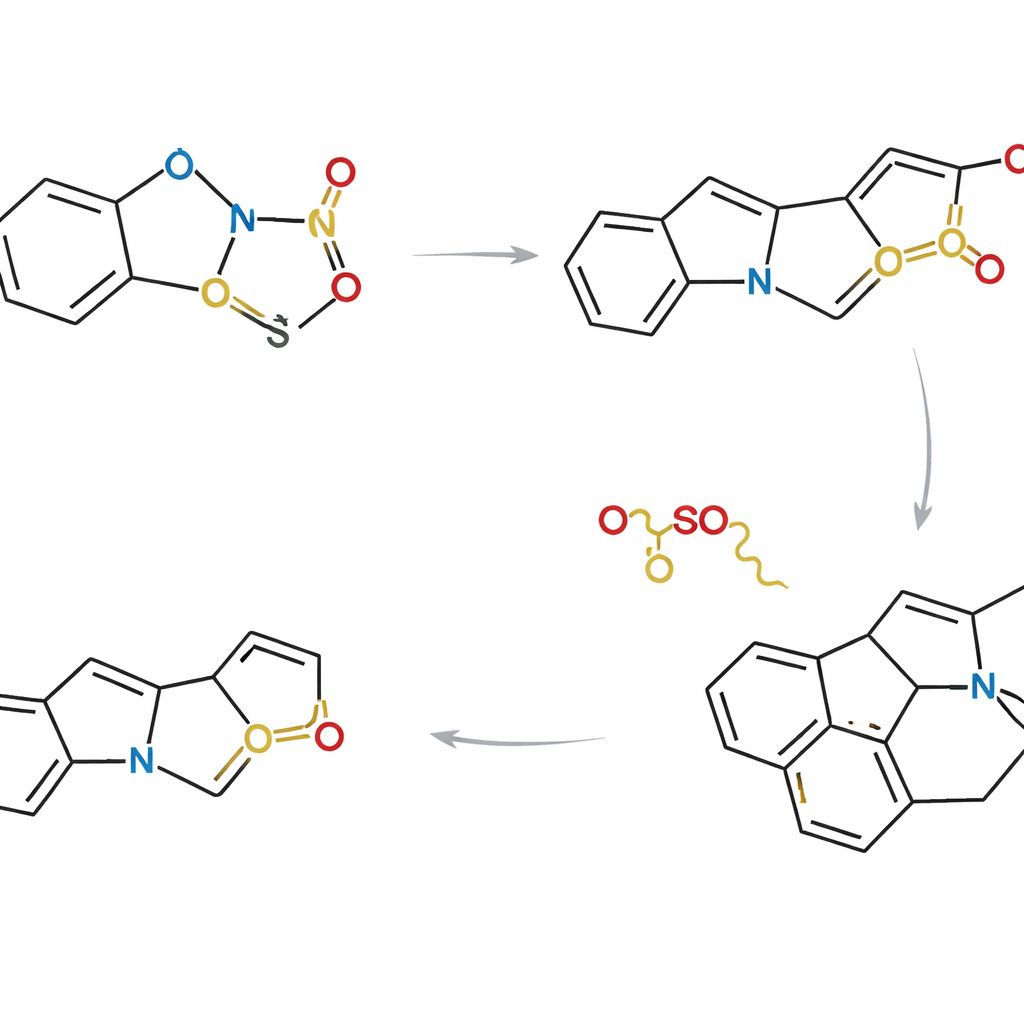
Samla många naturprodukter i en strategi
Med denna kontroll utformade forskarna tre kompletterande rutter som skiljer sig åt i hur och när indol‑ och tiofenpartnerna kopplas ihop. I en strategi är de två fragmenten förbundna innan cykloaddition, så reaktionen sker inom en och samma molekyl. I andra varianter reagerar de först som separata molekyler och genomgår sedan intern ringstängning. Genom noggranna val av substituenter och reaktionssekvenser kunde teamet konvergera mot ett gemensamt avancerat mellanled som sitter vid förgreningspunkten i Strychnos‑släktträdet. Från detta delade skal kunde de slutföra asymmetriska synteser av åtta naturprodukter, inklusive akuammicin, lagumicin, norfluorokurarine, flera alstoluciner och echitamidin — ofta i de kortaste och mest atom‑effektiva rutterna rapporterade hittills.
Knäcka en hundraårig syntetisk utmaning
Ett av de mest anmärkningsvärda exemplen är den första totala syntesen av brucine, en nära kemisk kusin till stryknin som varit känd i mer än 200 år och som använts flitigt som ett kiralt resolvansmedel, men som aldrig tidigare byggts helt från grunden. Brucines indolinsring är ovanligt elektronrik och benägen att brytas ned, vilket har avskräckt tidigare försök. Genom att skräddarsy sin tiofenbaserade kaskad och noggrant hantera reaktionsförhållanden lyckades författarna forma brucines ömtåliga ramverk på endast nio linjära steg från ett enkelt kommersiellt tillgängligt startmaterial. De uppnådde också en tiostegs asymmetrisk syntes av själva stryknin, den mest koncisa kirala rutten som rapporterats hittills.
Observera reaktioner med maskininlärning
För att förstå varför deras reaktioner ger så precisa utfall kombinerade teamet kvantkemi på hög nivå med moderna maskininlärningssimuleringar. Dessa beräkningar visade att reaktionen i vissa fall inte fortlöper i ett enda jämnt rörelsemönster utan genom en ojämn, stegvis dans: en kol‑kol‑bindning bildas först, ett grunt intermediär besöks kortvarigt, och sedan avges svaveldioxid nästan spontant när systemet glider nedför energilandskapet. Den kirala kamforsultam‑sidokedjan snedvrider subtilt denna väg, vilket gör en tredimensionell arrangemangsform mycket lättare att nå än den andra. Denna mekanistiska insikt ger riktlinjer för att designa nya tiofen‑baserade kaskader bortom Strychnos‑familjen.
Från dödliga toxiner till användbara verktyg
Sammanfattningsvis visar studien att tiofen S,S‑dioxider kan fungera som kraftfulla, programmerbara ”fjäder‑laddade” enheter för att slå ihop intrikata molekylära arkitekturer. Genom att utnyttja deras inneboende benägenhet att förlora svaveldioxid konstruerade författarna kaskadreationer som snabbt omvandlar enkla fragment till Strychnos‑alkaloidernas intrasslade ringsystem med hög selektivitet och minimalt antal onödiga steg. För icke‑specialister är slutsatsen att kemister lär sig förvandla även ökända gifter till mångsidiga plattformar för upptäckt genom smart reaktionsdesign och beräkningsmässig insikt, vilket gör det möjligt att utforska komplext kemiskt rum mer effektivt än någonsin tidigare.
Citering: Park, K.H.‘., Park, J., Frank, N. et al. Collective asymmetric synthesis of the Strychnos alkaloids via thiophene S,S-dioxide cycloadditions. Nat. Chem. 18, 782–789 (2026). https://doi.org/10.1038/s41557-025-02041-1
Nyckelord: Strychnos‑alkaloider, asymmetrisk syntes, cykloaddition‑kaskader, tiofendioxid (S,S), naturproduktkemi