Clear Sky Science · ru
Коллективный асимметричный синтез алкалоидов Strychnos посредством циклоприсоединений тиофен‑S,S‑диоксидов
Почему важны маленькие молекулы, вдохновлённые ядами
Алкалоиды Strychnos представляют собой семейство природных соединений, известных своей исключительной активностью — стрихнин служит печально известным примером — и сложными трёхмерными архитектурами. Эти молекулы давно привлекают химиков: они одновременно опасны и потенциально полезны, некоторые показывают активность против лекарственно‑устойчивых форм рака. Однако их пространственная сложность делает синтез в лаборатории чрезвычайно трудным. В этой статье описан новый, упрощённый способ управляемого и эффективного построения множества различных молекул Strychnos, что открывает возможности для более безопасного изучения и создания потенциальных новых лекарств, происходящих от этих некогда грозных ядов.
Построение сложных форм из простых фрагментов
Авторы стремились соответствовать современным идеалам химического синтеза: короткие реакции с минимальными отходами, дающие возможность получать несколько родственных молекул по общей траектории. Они сосредоточились на плотном, насыщенном кольцевом «ядре», общей черте алкалоидов Strychnos, и задали вопрос, можно ли собрать эту структуру из более простых блоков всего в несколько шагов. План опирался на соединение фрагмента индола — распространённого биологического каркаса — со специальным партнёром, тиофеном S,S‑диоксидом. При встрече эти два фрагмента претерпевают мощное образование кольца — циклоприсоединение Дильса–Альдера, за которым следует чистая потеря диоксида серы. Этот каскад превращает относительно плоские исходные куски в сложные трёхмерные кольцевые системы по сути за один приём.
Универсальный химический укор
Чтобы воплотить идею в практический набор приёмов, команда сначала разработала высокоселективные варианты этих циклоприсоединений. Присоединив дешёвую хиральную «ручку» (группу камфорсультам), они могли направлять реакцию так, чтобы образовывался почти исключительно один зеркально‑симметричный продукт — важное свойство для биоактивных соединений, которые часто ведут себя по‑разному у зеркальных изомеров. Показано, что широкий спектр индольных партнёров с разными заместителями реагирует мягко и даёт трициклические индолиновые продукты как единые диастереомеры. Эти продукты не только служат ступенями к алкалоидам Strychnos, но и сами по себе представляют интересные каркасы для медицины.
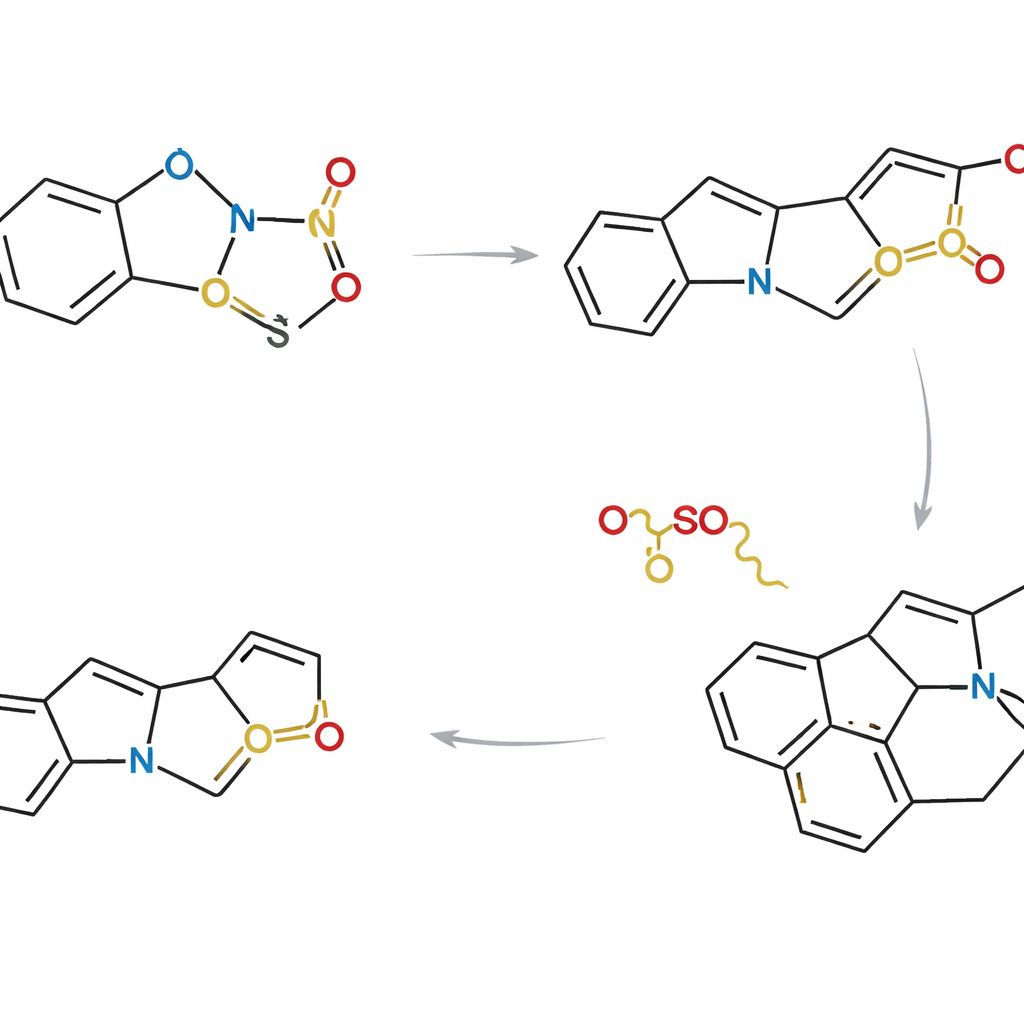
Сбор многих природных продуктов в одной стратегии
Обладая таким контролем, исследователи разработали три взаимодополняющих маршрута, различающихся способом и моментом соединения индольного и тиофенового партнёров. В одном подходе два фрагмента соединяют тетивой до циклоприсоединения, так что реакция происходит внутри одной молекулы. В других они сначала реагируют как отдельные молекулы, а затем проходят внутримолекулярное замыкание. Тщательно подбирая заместители и последовательности реакций, команда смогла сойтись к общему продвинутому интермедиату, занимающему точку разветвления в «семейном древе» Strychnos. От этого общего каркаса они завершили асимметричный синтез восьми природных продуктов, включая акуаммицин, лагумицин, норфлوروкурарин, несколько алстолуцинов и эхитамидин — часто в самых коротких и наиболее атомоэффективных маршрутах, сообщённых на сегодняшний день.
Решение столетней синтетической задачи
Одним из наиболее впечатляющих достижений стал первый полный синтез брацина (brucine) — близкого химического родственника стрихнина, известного более 200 лет и широко использовавшегося как хиральный средство для разделения, но никогда ранее полностью не собранного «с нуля». Индолиновое кольцо брацина необычно электронобогато и склонно к разложению, что препятствовало предыдущим попыткам. Настроив свой тиофеновый каскад и тщательно контролируя условия реакций, авторы смогли сформировать хрупкий каркас брацина всего за девять линейных шагов от простого коммерчески доступного исходного материала. Им также удалось выполнить десятишаговый асимметричный синтез самого стрихнина — наиболее лаконичный хиральный маршрут, о котором сообщалось до настоящего времени.
Наблюдение реакций с помощью машинного обучения
Чтобы понять, почему реакции дают столь точные результаты, команда совместила расчёты высокого уровня квантовой химии с современными моделями машинного обучения. Эти вычисления показали, что в некоторых случаях реакция протекает не одномоментно, а поэтапно: сначала формируется одна углеродно‑углеродная связь, кратковременно посещается неглубокий интермедиат, а затем диоксид серы почти спонтанно отталкивается при скатывании системы по энергетическому ландшафту. Хиральная боковая цепь камфорсультама тонко смещает этот путь, делая достижимой одну трёхмерную конфигурацию гораздо легче, чем другую. Это механистическое понимание даёт ориентиры для проектирования новых тиофеновых каскадов за пределами семейства Strychnos.
От смертоносных токсинов к полезным инструментам
В целом исследование демонстрирует, что тиофен‑S,S‑диоксиды могут выступать как мощные, программируемые «заряженные пружины» для быстрого складывания запутанных молекулярных архитектур. Используя их предрасположенность к потере диоксида серы, авторы спроектировали каскадные реакции, которые быстро превращают простые фрагменты в сложные кольцевые системы алкалоидов Strychnos с высокой селективностью и минимальным числом лишних этапов. Для неспециалистов главный вывод таков: химики учатся превращать даже печально известные яды в универсальные платформы для открытий, применяя изящный дизайн реакций и вычислительную интуицию для эффективного исследования сложного химического пространства.»}
Цитирование: Park, K.H.‘., Park, J., Frank, N. et al. Collective asymmetric synthesis of the Strychnos alkaloids via thiophene S,S-dioxide cycloadditions. Nat. Chem. 18, 782–789 (2026). https://doi.org/10.1038/s41557-025-02041-1
Ключевые слова: Алкалоиды Strychnos, асимметричный синтез, каскады циклоприсоединений, тиофен S,S‑диоксиды, химия природных соединений