Clear Sky Science · fr
Synthèse asymétrique collective des alcaloïdes Strychnos par cycloadditions des thiophènes S,S‑dioxyde
Pourquoi de petites molécules inspirées de poisons comptent
Les alcaloïdes Strychnos forment une famille de composés naturels célèbres pour leur puissance extrême — la strychnine en est l’exemple notoire — et pour leurs architectures enchevêtrées et tridimensionnelles. Ces molécules fascinent depuis longtemps les chimistes parce qu’elles sont à la fois dangereuses et potentiellement utiles, certaines montrant un intérêt contre des cancers résistants aux médicaments. Leur complexité architecturale les rend toutefois très difficiles à construire en laboratoire. Cet article dévoile une nouvelle voie simplifiée pour assembler de nombreuses molécules Strychnos de façon contrôlée et efficace, ouvrant la porte à des études plus sûres et à de possibles nouveaux médicaments dérivés de ces poisons autrefois redoutés.
Construire des formes complexes à partir de pièces simples
Les auteurs se sont fixés les idéaux modernes de la synthèse chimique : des réactions courtes, économes en déchets et capables de produire plusieurs molécules apparentées depuis une voie commune. Ils se sont concentrés sur le « cœur » dense et compact en anneaux partagé par les alcaloïdes Strychnos et ont cherché à savoir si ce cadre pouvait être assemblé à partir de blocs de construction plus simples en seulement quelques étapes. Leur plan reposait sur la jonction d’un fragment indole — un motif courant en biologie — avec un partenaire spécial appelé thiophène S,S‑dioxyde. Quand ces deux composants se rencontrent, ils subissent un puissant événement de formation d’anneau appelé cycloaddition de Diels–Alder, suivi de la perte nette de dioxyde de soufre. Cette cascade transforme des pièces de départ relativement plates en systèmes d’anneaux tridimensionnels complexes en une seule opération, pour ainsi dire.
Un raccourci chimique polyvalent
Pour transformer cette idée en boîte à outils pratique, l’équipe a d’abord développé des versions hautement sélectives de ces cycloadditions. En attachant une « poignée » chirale bon marché (un groupe camphorsultame) au thiophène S,S‑dioxyde, ils ont pu orienter la réaction pour former presque exclusivement un seul produit image‑miroir — une caractéristique cruciale pour les molécules bioactives, qui se comportent souvent très différemment selon leur énantiomère. Ils ont montré qu’un large éventail de partenaires indole, portant divers substituants, réagissent de façon fluide sous des conditions douces pour donner des produits indoline tricycliques comme diastéréoisomères uniques. Ces produits sont non seulement des marches vers les alcaloïdes Strychnos, mais représentent aussi des cadres attractifs pour la chimie médicinale en eux‑mêmes.
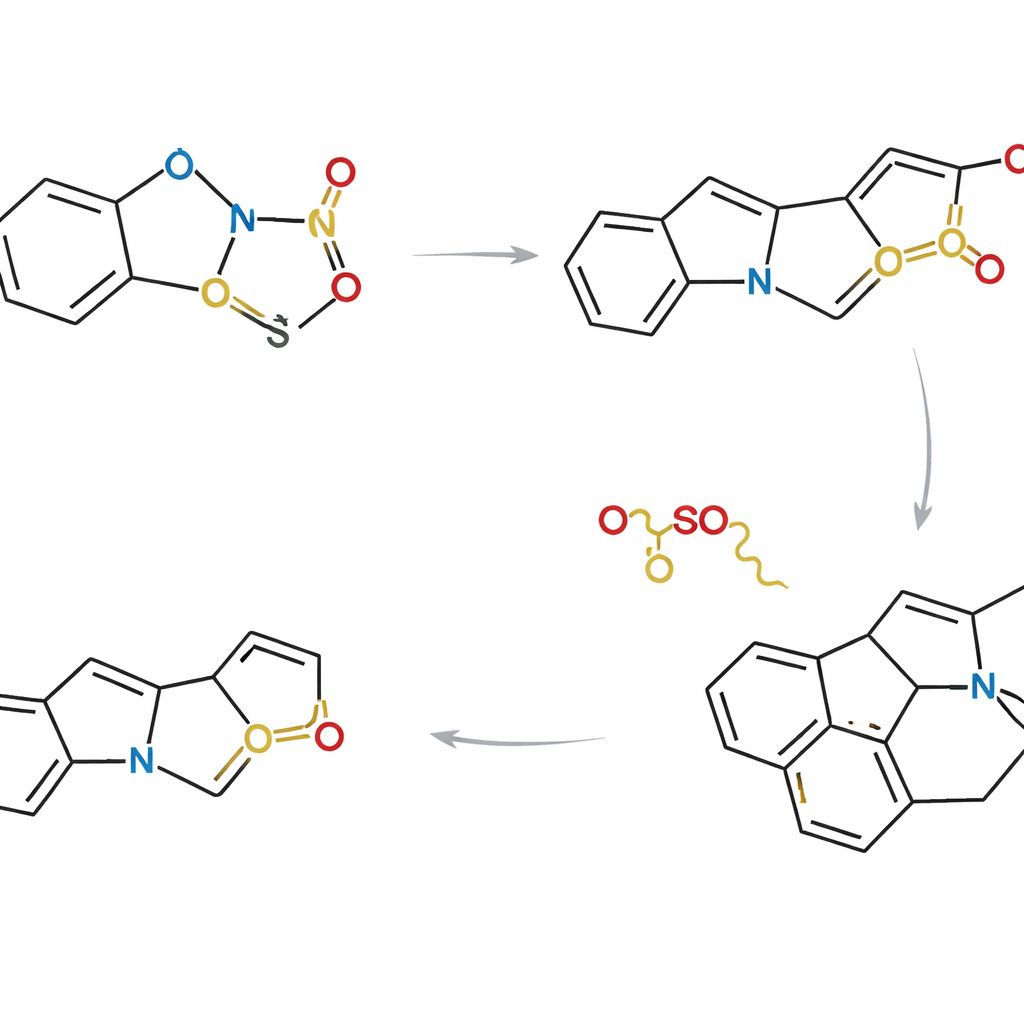
Réunir de nombreux produits naturels dans une même stratégie
Fort de ce contrôle, les chercheurs ont conçu trois voies complémentaires qui diffèrent par la manière et le moment où les partenaires indole et thiophène sont liés. Dans une approche, les deux fragments sont reliés entre eux avant la cycloaddition, de sorte que la réaction se déroule à l’intérieur d’une seule molécule. Dans d’autres, ils réagissent d’abord comme molécules distinctes puis subissent une fermeture interne d’anneau. En choisissant soigneusement substituants et séquences de réaction, l’équipe a pu converger vers un intermédiaire avancé commun qui se situe au point de ramification de l’arbre généalogique des Strychnos. À partir de ce squelette partagé, ils ont réalisé des synthèses asymétriques de huit produits naturels, dont l’akuammicine, la lagumicine, la norfluorocurarine, plusieurs alstolucines et l’échitamidine — souvent via les routes les plus courtes et les plus efficaces en atomes rapportées à ce jour.
Résoudre un défi synthétique vieux d’un siècle
Une des démonstrations les plus marquantes est la première synthèse totale de la brucine, proche cousine chimique de la strychnine connue depuis plus de 200 ans et largement utilisée comme agent de résolution chiral, mais jamais entièrement construite de novo. L’anneau indoline de la brucine est exceptionnellement riche en électrons et sujet à la dégradation, ce qui a découragé les tentatives antérieures. En adaptant leur cascade à base de thiophène et en contrôlant finement les conditions réactionnelles, les auteurs ont pu forger l’architecture délicate de la brucine en seulement neuf étapes linéaires à partir d’un matériau de départ simple et disponible dans le commerce. Ils ont également réalisé une synthèse asymétrique de la strychnine en dix étapes, la voie chirale la plus concise publiée jusqu’à présent.
Surveiller les réactions avec l’apprentissage automatique
Pour comprendre pourquoi leurs réactions donnent des résultats si précis, l’équipe a combiné la chimie quantique de haut niveau avec des simulations modernes d’apprentissage automatique. Ces calculs ont révélé que, dans certains cas, la réaction ne progresse pas en un seul mouvement fluide mais par une danse inégale et par étapes : une liaison carbone–carbone se forme d’abord, un intermédiaire peu profond est brièvement parcouru, puis le dioxyde de soufre est expulsé presque spontanément lorsque le système descend la colline énergétique. La chaîne latérale camphorsultame chirale biaise subtilement cette trajectoire, rendant une organisation tridimensionnelle beaucoup plus accessible que l’autre. Cette compréhension mécanistique fournit des lignes directrices pour concevoir de nouvelles cascades à base de thiophène au‑delà de la famille des Strychnos.
De toxines mortelles à des outils utiles
Globalement, l’étude montre que les thiophènes S,S‑dioxyde peuvent agir comme des éléments « à ressort » puissants et programmables pour assembler des architectures moléculaires complexes. En exploitant leur tendance intrinsèque à perdre du dioxyde de soufre, les auteurs ont conçu des cascades qui convertissent rapidement des fragments simples en systèmes d’anneaux enchevêtrés des alcaloïdes Strychnos avec une grande sélectivité et un minimum d’étapes inutiles. Pour les non‑spécialistes, la leçon est que les chimistes apprennent à transformer même des poisons notoires en plates‑formes polyvalentes pour la découverte, en utilisant une conception astucieuse des réactions et des outils computationnels pour explorer l’espace chimique complexe plus efficacement que jamais.
Citation: Park, K.H.‘., Park, J., Frank, N. et al. Collective asymmetric synthesis of the Strychnos alkaloids via thiophene S,S-dioxide cycloadditions. Nat. Chem. 18, 782–789 (2026). https://doi.org/10.1038/s41557-025-02041-1
Mots-clés: Alcaloïdes Strychnos, Synthèse asymétrique, Cascades de cycloaddition, Thiophènes S,S‑dioxyde, Chimie des produits naturels