Clear Sky Science · es
Síntesis asimétrica colectiva de los alcaloides de Strychnos mediante cicloadiciones de tiofeno S,S-dioxido
Por qué importan las pequeñas moléculas inspiradas en venenos
Los alcaloides de Strychnos son una familia de compuestos naturales famosos por su potencia extrema —la estricnina es el ejemplo notorio— y por sus formas enredadas y tridimensionales. Estas moléculas han fascinado durante largo tiempo a los químicos porque son a la vez peligrosas y potencialmente útiles; algunas muestran promesas contra cánceres resistentes a fármacos. Sin embargo, su complejidad arquitectónica las hace muy difíciles de construir en el laboratorio. Este trabajo presenta una nueva vía simplificada para construir muchos compuestos de Strychnos de forma controlada y eficiente, abriendo la puerta a estudios más seguros y a posibles nuevos medicamentos derivados de estos venenos antaño temidos.
Construir formas complejas a partir de piezas simples
Los autores buscaron cumplir los ideales modernos de la síntesis química: reacciones cortas, con poco residuo y capaces de producir múltiples moléculas relacionadas a partir de una vía común. Se centraron en el denso «núcleo» lleno de anillos compartido por los alcaloides de Strychnos y se preguntaron si ese marco podía ensamblarse a partir de bloques más simples en solo unos pocos pasos. Su plan consistió en unir un fragmento de indol —un andamiaje habitual en biología— con un socio especial llamado tiofeno S,S-dioxido. Cuando ambos se encuentran, sufren un potente evento formador de anillos llamado cicloadición de Diels–Alder, seguido por la pérdida limpia de dióxido de azufre. Esta cascada convierte piezas de partida relativamente planas en sistemas de anillos complejos y tridimensionales, prácticamente de un solo golpe.
Un atajo químico versátil
Para convertir esta idea en una caja de herramientas práctica, el equipo desarrolló primero versiones altamente selectivas de estas reacciones de cicloadición. Al unir un «asa» quiral barato (un grupo camforsultama) al tiofeno S,S-dioxido pudieron dirigir la reacción para formar casi exclusivamente un enantiómero —una característica crucial para moléculas bioactivas, que a menudo se comportan de modo muy distinto frente a sus imágenes especulares. Demostraron que una amplia variedad de socios indólicos, con distintos sustituyentes, reaccionan con suavidad bajo condiciones leves para dar productos indolinas tríciclicas como diastereómeros únicos. Estos productos no solo son peldaños hacia los alcaloides de Strychnos, sino que también constituyen marcos atractivos para la química medicinal por derecho propio.
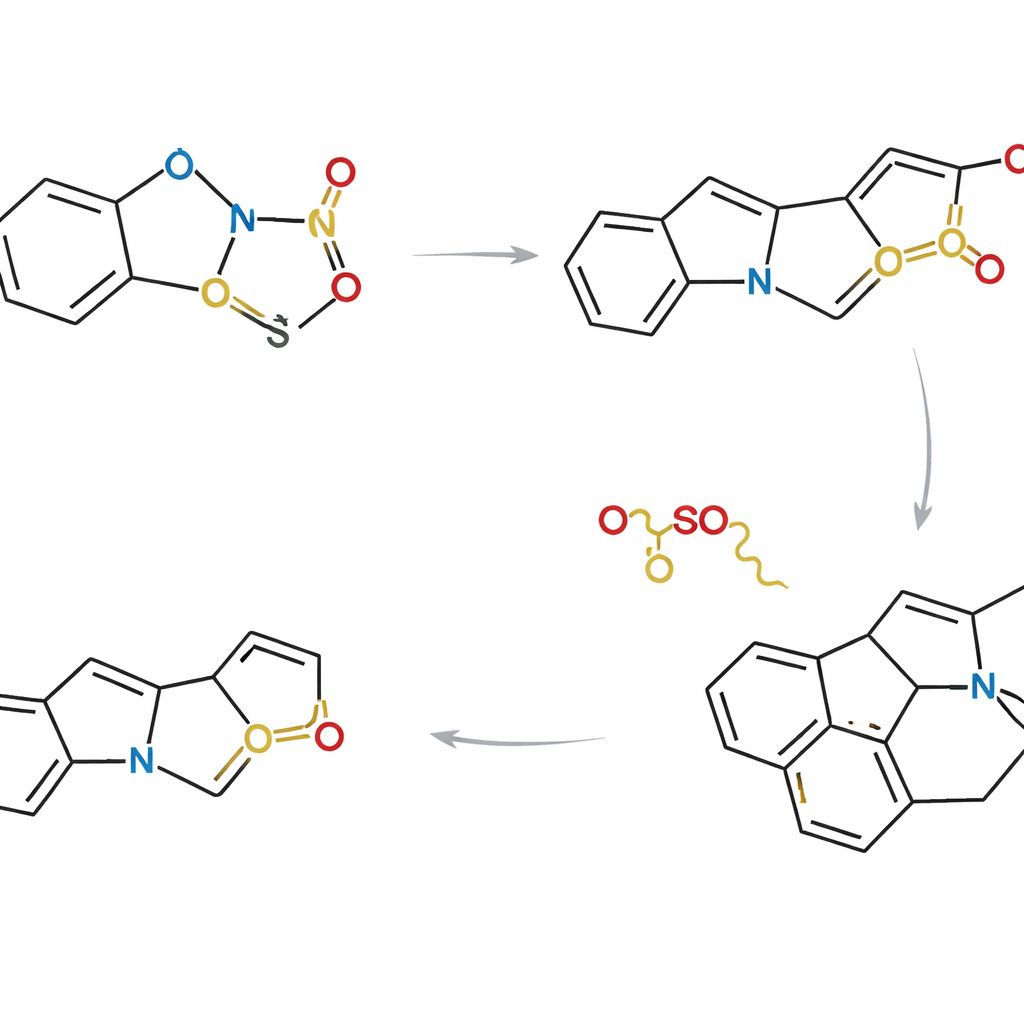
Reunir muchos productos naturales en una sola estrategia
Con este control, los investigadores diseñaron tres rutas complementarias que difieren en cómo y cuándo se enlazan los socios indólico y tiofénico. En un enfoque, los dos fragmentos se conectan antes de la cicloadición, de modo que la reacción ocurre dentro de una sola molécula. En otros, primero reaccionan como moléculas separadas y después sufren un cierre de anillo interno. Mediante la elección cuidadosa de sustituyentes y secuencias de reacción, el equipo consiguió converger hacia un intermedio avanzado común que se ubica en el punto de ramificación del árbol familiar de los Strychnos. A partir de este andamiaje compartido, completaron síntesis asimétricas de ocho productos naturales, incluidos akuammicina, lagumicina, norfluorocurarina, varias alstolucinas y echitamidina —con frecuencia en las rutas más concisas y eficientes en átomos reportadas hasta la fecha.
Resolver un desafío sintético de un siglo
Una de las demostraciones más llamativas es la primera síntesis total de brucina, una pariente química cercana de la estricnina que se conoce desde hace más de 200 años y se ha usado ampliamente como agente de resolución quiral, pero que nunca se había construido completamente desde cero. El anillo de indolina de la brucina es inusualmente rico en electrones y propenso a degradarse, lo que desalentó intentos previos. Al adaptar su cascada basada en tiofeno y manejar cuidadosamente las condiciones de reacción, los autores lograron forjar el delicado andamiaje de la brucina en solo nueve pasos lineales a partir de un material de partida comercial sencillo. También consiguieron una síntesis asimétrica de la estricnina en diez pasos, la ruta quiral más concisa reportada hasta ahora.
Vigilar las reacciones con aprendizaje automático
Para entender por qué sus reacciones producen resultados tan precisos, el equipo combinó química cuántica de alto nivel con simulaciones modernas de aprendizaje automático. Estos cálculos revelaron que, en algunos casos, la reacción no progresa en un movimiento homogéneo sino a través de una danza desigual y por etapas: primero se forma un enlace carbono‑carbono, se visita brevemente un intermedio poco profundo y luego el dióxido de azufre se expulsa casi de forma espontánea mientras el sistema desciende por el paisaje energético. La cadena lateral quiral de camforsultama sesga sutilmente esta vía, haciendo que una disposición tridimensional sea mucho más fácil de alcanzar que la otra. Esta visión mecanística ofrece pautas para diseñar nuevas cascadas basadas en tiofeno más allá de la familia Strychnos.
De toxinas mortales a herramientas útiles
En conjunto, el estudio muestra que los tiofenos S,S-dioxido pueden actuar como piezas «cargadas» potentes y programables para ensamblar arquitecturas moleculares intrincadas. Aprovechando su impulso incorporado para perder dióxido de azufre, los autores diseñaron reacciones en cascada que convierten rápidamente fragmentos simples en los enmarañados sistemas anulares de los alcaloides de Strychnos con alta selectividad y pasos mínimos desperdiciados. Para los no especialistas, la conclusión es que los químicos están aprendiendo a convertir incluso venenos notorios en plataformas versátiles para el descubrimiento, usando un diseño ingenioso de reacciones e insights computacionales para explorar el espacio químico complejo de forma más eficiente que nunca.
Cita: Park, K.H.‘., Park, J., Frank, N. et al. Collective asymmetric synthesis of the Strychnos alkaloids via thiophene S,S-dioxide cycloadditions. Nat. Chem. 18, 782–789 (2026). https://doi.org/10.1038/s41557-025-02041-1
Palabras clave: Alcaloides de Strychnos, síntesis asimétrica, cascadas de cicloadición, tiofenos S,S-dioxido, química de productos naturales