Clear Sky Science · it
Sintesi asimmetrica collettiva degli alcaloidi Strychnos mediante cicladditioni di tiofene S,S-diossido
Perché contano le piccole molecole ispirate ai veleni
Gli alcaloidi Strychnos sono una famiglia di composti naturali noti per la loro potenza estrema—lo strichnina è l'esempio celebre—e per le loro forme tortuose e tridimensionali. Queste molecole hanno da tempo affascinato i chimici perché sono al contempo pericolose e potenzialmente utili; alcune mostrano promettenti attività contro tumori resistenti alle terapie. Tuttavia, la loro complessa architettura le rende molto difficili da costruire in laboratorio. Questo articolo presenta una nuova via semplificata per costruire in modo controllato ed efficiente molti diversi membri della famiglia Strychnos, aprendo la strada a studi più sicuri e a possibili nuovi farmaci derivati da questi veleni un tempo temuti.
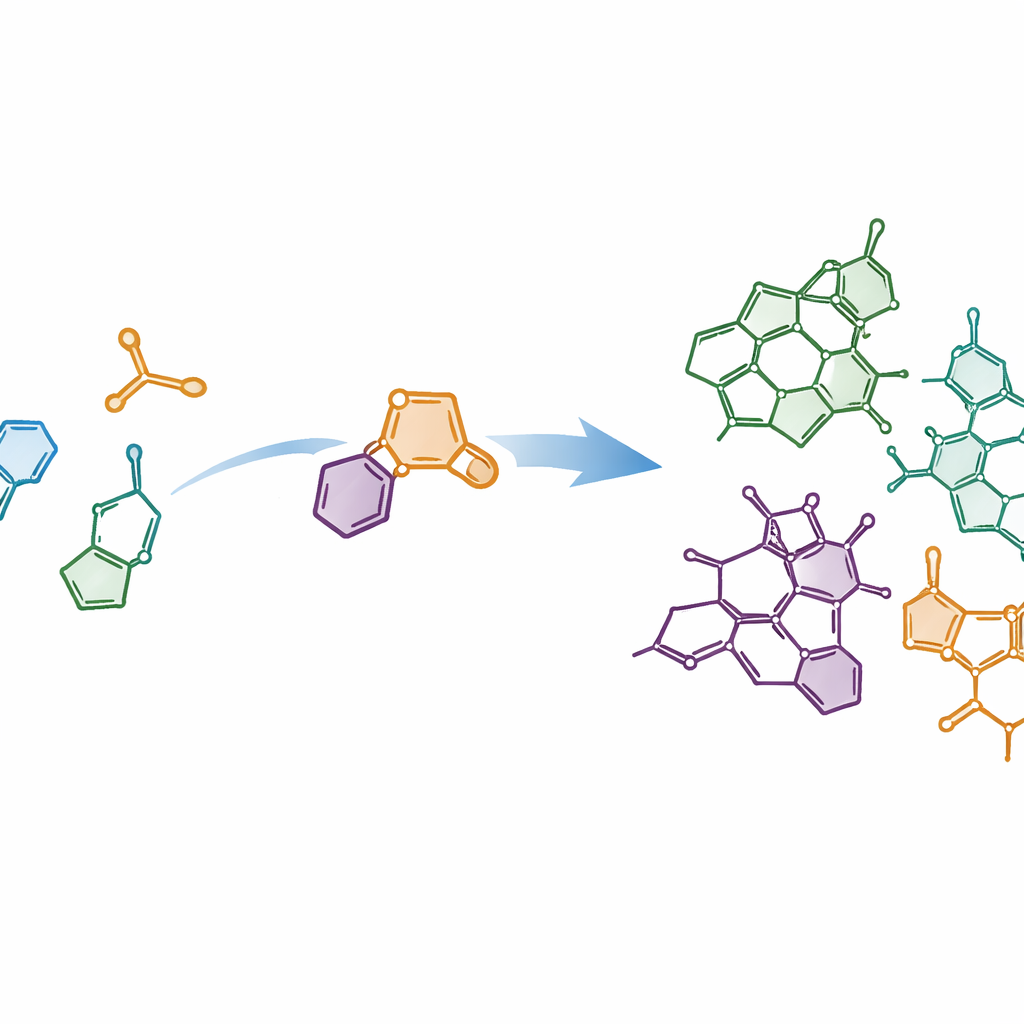
Costruire strutture complesse a partire da pezzi semplici
Gli autori hanno cercato di soddisfare gli ideali contemporanei della sintesi chimica: reazioni brevi, a basso impatto di scarto e in grado di produrre molte molecole correlate a partire da una via comune. Si sono concentrati sul nucleo denso e ricco di anelli condiviso dagli alcaloidi Strychnos e si sono chiesti se questo scheletro potesse essere assemblato da blocchi più semplici in appena pochi passaggi. Il loro piano prevedeva l’unione di un frammento indolico—uno scaffold comune in biologia—a un partner speciale chiamato tiofene S,S-diossido. Quando questi due reagiscono fra loro, subiscono un potente evento di formazione di anelli chiamato cicladdizione Diels–Alder, seguito dalla pulita perdita di diossido di zolfo. Questa cascata trasforma pezzi relativamente piatti di partenza in complessi sistemi anulari tridimensionali in sostanza in un solo colpo.
Una scorciatoia chimica versatile
Per trasformare questa idea in una cassetta degli attrezzi pratica, il gruppo ha prima sviluppato versioni altamente selettive di queste cicladdizioni. Attaccando al tiofene S,S-diossido una “maniglia” chirale economica (un gruppo camforsultame), sono riusciti a indirizzare la reazione a formare quasi esclusivamente un solo prodotto immagine-speculare—una caratteristica cruciale per molecole bioattive, che spesso si comportano in modo molto diverso rispetto al loro enantiomero. Hanno dimostrato che un'ampia gamma di partner indolici, portatori di diversi sostituenti, reagisce in modo regolare in condizioni miti per dare prodotti indolinici triclci come singoli diastereomeri. Questi prodotti non sono solo tappe verso gli alcaloidi Strychnos, ma costituiscono anche scheletri interessanti per la chimica medicinale di per sé.
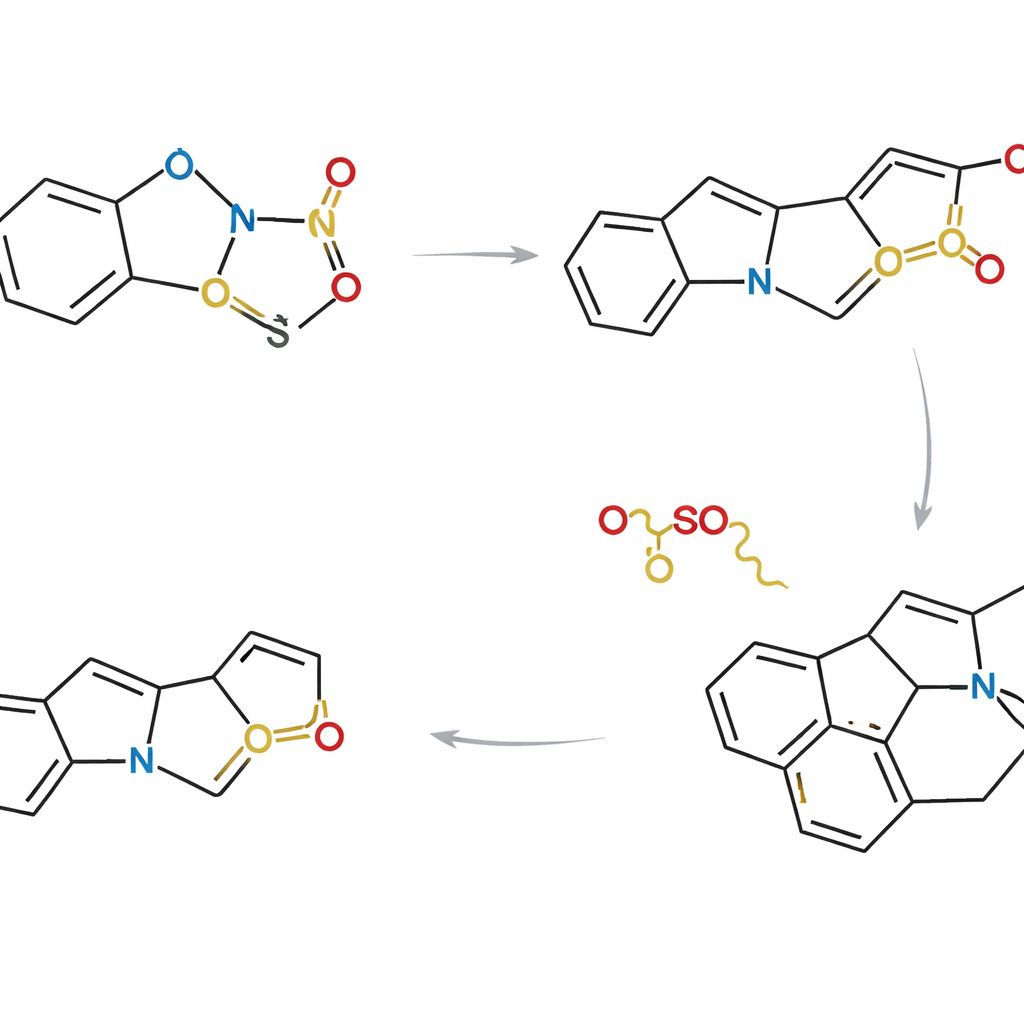
Raccogliere molti prodotti naturali con una sola strategia
Dotati di questo controllo, i ricercatori hanno progettato tre rotte complementari che differiscono nel modo e nel momento in cui i partner indolo e tiofene vengono collegati. In un approccio, i due frammenti sono legati insieme prima della cicladdizione, così la reazione avviene all’interno di una singola molecola. In altri, reagiscono prima come molecole separate e poi subiscono la chiusura anulare interna. Scegliendo con cura i sostituenti e le sequenze di reazione, il gruppo è riuscito a convergere su un intermedio avanzato comune che si trova al punto di diramazione dell’albero genealogico degli Strychnos. Da questo scaffold condiviso hanno completato sintesi asimmetriche di otto prodotti naturali, tra cui akuammicina, lagumicina, norfluorocurarina, diverse alstolucine ed echitamidina—spesso con le rotte più brevi e più efficienti in termini di atomi riportate fino ad oggi.
Risolvendouna sfida sintetica vecchia di un secolo
Una delle dimostrazioni più impressionanti è la prima sintesi totale della brucina, una stretta cugina chimica della strichnina nota da oltre 200 anni e ampiamente impiegata come agente di risoluzione chirale, eppure mai costruita completamente da zero. L’anello indolinico della brucina è particolarmente ricco di elettroni e soggetto a degradazione, caratteristica che ha scoraggiato tentativi precedenti. Adattando la loro cascata basata su tiofene e gestendo con cura le condizioni di reazione, gli autori sono riusciti a forgiare il delicato impianto della brucina in sole nove tappe lineari a partire da un materiale di partenza commerciale semplice. Hanno anche realizzato una sintesi asimmetrica della strichnina in dieci passaggi, la via chirale più concisa riportata finora.
Osservare le reazioni con il machine learning
Per comprendere perché le loro reazioni diano esiti così precisi, il gruppo ha combinato chimica quantistica di alto livello con moderne simulazioni di machine learning. Questi calcoli hanno rivelato che, in alcuni casi, la reazione non procede in un unico movimento uniforme ma attraverso una danza irregolare e a tappe: prima si forma un legame carbonio–carbonio, si visita brevemente un intermedio poco profondo e poi il diossido di zolfo viene espulso quasi spontaneamente mentre il sistema scende nel paesaggio energetico. La catena laterale chirale camforsultame sbilancia sottilmente questo percorso, rendendo molto più facile raggiungere una disposizione tridimensionale rispetto all’altra. Questa comprensione meccanicistica fornisce linee guida per progettare nuove cascate basate su tiofene al di là della famiglia Strychnos.
Da tossine mortali a strumenti utili
Nel complesso, lo studio dimostra che i tiofeni S,S-diossidi possono agire come potenti e programmabili pezzi “caricati a molla” per assemblare architetture molecolari intricate. Sfruttando la loro tendenza intrinseca a perdere diossido di zolfo, gli autori hanno messo a punto reazioni a cascata che convertono rapidamente semplici frammenti nei complessi sistemi anulari degli alcaloidi Strychnos con alta selettività e passi minimi sprecati. Per il lettore non specialista, il messaggio è che i chimici stanno imparando a trasformare persino veleni tristemente famosi in piattaforme versatili per la scoperta, usando un design reazionale ingegnoso e l’intuito computazionale per esplorare lo spazio chimico complesso in modo più efficiente che mai prima d’ora.
Citazione: Park, K.H.‘., Park, J., Frank, N. et al. Collective asymmetric synthesis of the Strychnos alkaloids via thiophene S,S-dioxide cycloadditions. Nat. Chem. 18, 782–789 (2026). https://doi.org/10.1038/s41557-025-02041-1
Parole chiave: Alcaloidi Strychnos, sintesi asimmetrica, cascate di cicladdizione, tiofeni S,S-diossidi, chimica dei prodotti naturali