Clear Sky Science · nl
Collectieve asymmetrische synthese van Strychnos-alkaloïden via cycloaddities van thiophene S,S-dioxiden
Waarom door vergif geïnspireerde kleine moleculen ertoe doen
De Strychnos-alkaloïden vormen een familie natuurlijke verbindingen die beroemd zijn vanwege hun extreme potentie — strychnine is het beruchte voorbeeld — en vanwege hun ingewikkelde, driedimensionale vormen. Deze moleculen hebben chemici al lang gefascineerd omdat ze tegelijk gevaarlijk en potentieel nuttig zijn; sommige tonen belofte tegen medicijnresistente kankers. Hun architectonische complexiteit maakt ze echter zeer moeilijk in het laboratorium op te bouwen. Dit artikel onthult een nieuwe, gestroomlijnde manier om veel verschillende Strychnos-moleculen gecontroleerd en efficiënt te construeren, wat de deur opent naar veiliger onderzoek en mogelijk nieuwe geneesmiddelen afgeleid van deze ooit gevreesde vergiften.
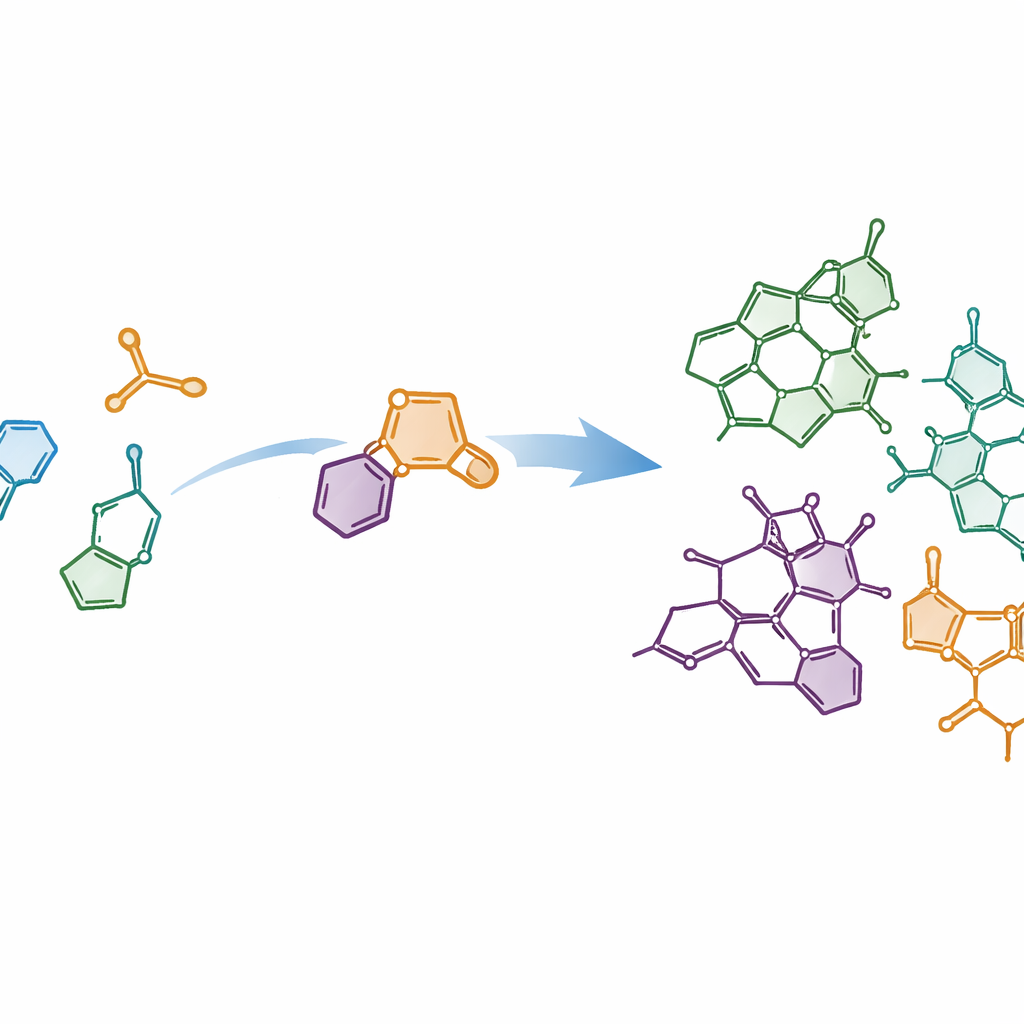
Complexe vormen opbouwen uit eenvoudige onderdelen
De auteurs streefden naar de moderne ideaalbeelden van chemische synthese: reacties die kort zijn, weinig afval genereren en meerdere verwante moleculen uit een gemeenschappelijk pad kunnen produceren. Ze richtten zich op de dichte, ring-rijke "kern" die Strychnos-alkaloïden gemeen hebben en vroegen zich af of dit kader in slechts enkele stappen uit eenvoudigere bouwstenen in elkaar gezet kon worden. Hun plan berustte op het verbinden van een indoolfragment — een veelvoorkomend skelet in de biologie — met een speciaal partnermolecuul dat een thiophene S,S-dioxide heet. Wanneer deze twee samenkomen, ondergaan ze een krachtige ringvormende gebeurtenis die een Diels–Alder-cycloadditie wordt genoemd, gevolgd door het schone verlies van zwaveldioxidegas. Deze cascade zet relatief vlakke uitgangsstoffen in wezen in één beweging om in complexe, driedimensionale ringsystemen.
Een veelzijdige chemische snelkoppeling
Om dit idee in een praktisch gereedschapskist te veranderen, ontwikkelde het team eerst zeer selectieve versies van deze cycloadditie-reacties. Door een goedkope, chirale "greep" (een camphorsultamgroep) aan de thiophene S,S-dioxide te koppelen, konden ze de reactie sturen zodat er vrijwel uitsluitend één spiegelbeeldproduct werd gevormd — een cruciale eigenschap voor bioactieve moleculen, die vaak heel anders reageren dan hun spiegelbeelden. Ze toonden aan dat een breed scala aan indoolpartners, met veel verschillende substituenten, onder milde omstandigheden soepel reageert en tricyclische indolineproducten oplevert als enkele diastereomeren. Deze producten zijn niet alleen opstapjes naar Strychnos-alkaloïden, maar vormen op zichzelf ook aantrekkelijke raamwerken voor de medicinale chemie.
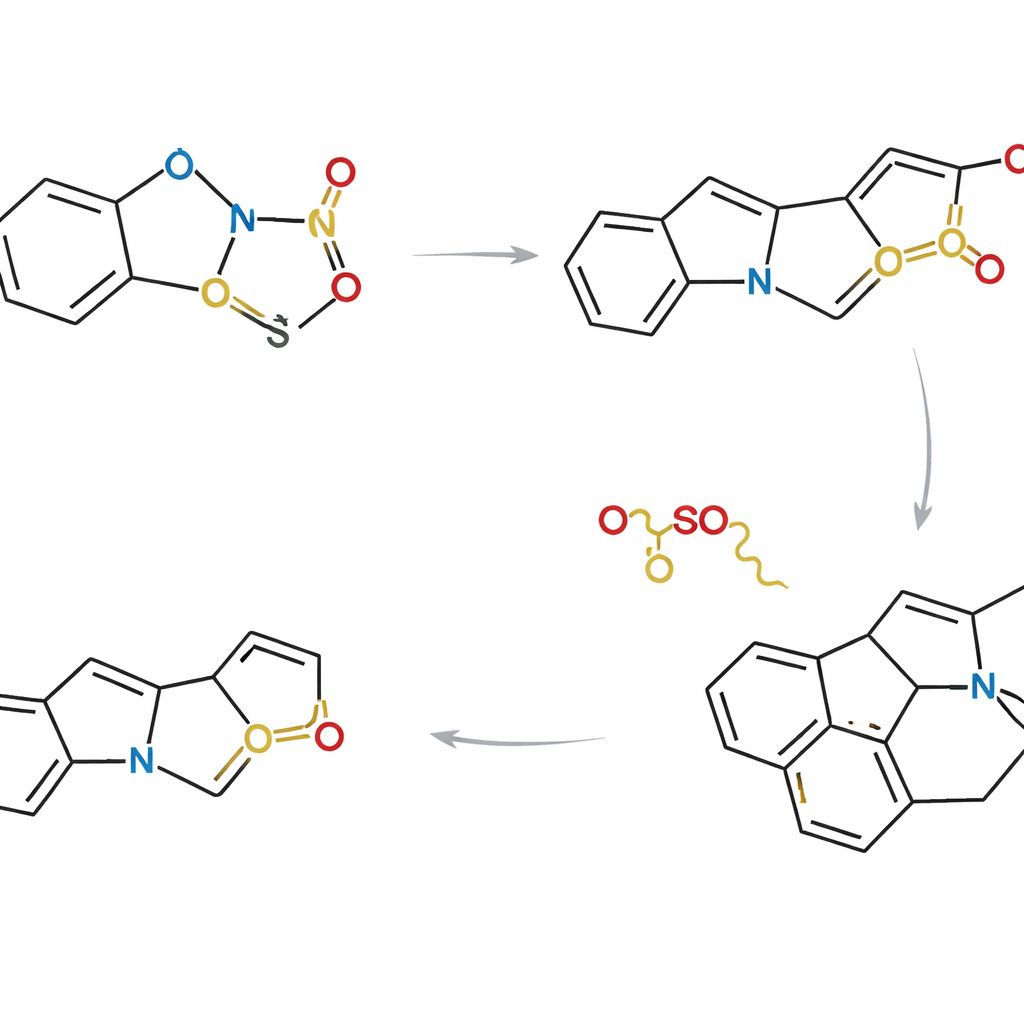
Veel natuurlijke producten verzamelen in één strategie
Gewapend met deze controle ontwierpen de onderzoekers drie complementaire routes die verschillen in hoe en wanneer de indool- en thiophene-partners worden verbonden. In de ene benadering worden de twee fragmenten aan elkaar getetherd voordat de cycloadditie plaatsvindt, zodat de reactie binnen één molecule gebeurt. In andere benaderingen reageren ze eerst als afzonderlijke moleculen en ondergaan daarna interne ringsluiting. Door zorgvuldig substituenten en reactiesequenties te kiezen, kon het team convergeren naar een gemeenschappelijk gevorderd intermediair dat op het kruispunt van de Strychnos-stamboom zit. Vanuit dit gedeelde skelet voltooiden ze asymmetrische syntheses van acht natuurlijke producten, waaronder akuammicine, lagumicine, norfluorocurarine, meerdere alstolucines en echitamidine — vaak via de kortste en meest atom-efficiënte routes die tot nu toe zijn gerapporteerd.
Een eeuwoude synthetische uitdaging kraken
Een van de meest opvallende demonstraties is de eerste totale synthese van brucine, een nauw verwant chemisch familielid van strychnine dat al meer dan 200 jaar bekend is en veel gebruikt werd als chiraal resolveermiddel, maar dat nog nooit volledig vanaf het begin was opgebouwd. De indoline-ring van brucine is buitengewoon elektronrijk en gevoelig voor afbraak, wat eerdere pogingen belette. Door hun thiophene-gebaseerde cascade aan te passen en de reactiestromen nauwkeurig te beheersen, konden de auteurs het fragiele raamwerk van brucine smeden in slechts negen lineaire stappen vanaf een eenvoudig commercieel beschikbaar uitgangsmateriaal. Ze behaalden ook een tienstappen asymmetrische synthese van strychnine zelf, de meest beknopte chirale route die tot nu toe is gerapporteerd.
Reacties volgen met machine learning
Om te begrijpen waarom hun reacties zulke precieze uitkomsten geven, combineerde het team hoogwaardige kwantumchemie met moderne machine-learning-simulaties. Deze berekeningen lieten zien dat de reactie in sommige gevallen niet in één vloeiende beweging verloopt, maar door een ongelijkmatige, stapsgewijze dans: eerst vormt zich één koolstof–koolstof-binding, wordt een ondiep intermediair kort bezocht, en vervolgens wordt zwaveldioxide bijna spontaan uitgestoten terwijl het systeem naar beneden glijdt op het energielandschap. De chirale camphorsultam-zijketen bevoordeelt subtiel dit pad, waardoor één driedimensionale rangschikking veel gemakkelijker te bereiken is dan de andere. Dit mechanistische inzicht biedt richtlijnen voor het ontwerpen van nieuwe thiophene-gebaseerde cascades buiten de Strychnos-familie.
Van dodelijke toxines naar bruikbare hulpmiddelen
Al met al laat de studie zien dat thiophene S,S-dioxiden kunnen fungeren als krachtige, programmeerbare "veerbeladen" onderdelen om ingewikkelde moleculaire architecturen in elkaar te klikken. Door hun ingebouwde drang om zwaveldioxide te verliezen te benutten, ontwierpen de auteurs cascade-reacties die eenvoudig fragmenten snel en met hoge selectiviteit en minimale verspilde stappen omzetten in de verwarde ringsystemen van Strychnos-alkaloïden. Voor niet-specialisten is de conclusie dat chemici leren zelfs beruchte vergiften te veranderen in veelzijdige platforms voor ontdekking, waarbij slim reactiedesign en computationele inzichten worden ingezet om complex chemisch gebied efficiënter te verkennen dan ooit tevoren.
Bronvermelding: Park, K.H.‘., Park, J., Frank, N. et al. Collective asymmetric synthesis of the Strychnos alkaloids via thiophene S,S-dioxide cycloadditions. Nat. Chem. 18, 782–789 (2026). https://doi.org/10.1038/s41557-025-02041-1
Trefwoorden: Strychnos-alkaloïden, asymmetrische synthese, cycloadditie-cascades, thiophene S,S-dioxiden, natuurlijke productchemie