Clear Sky Science · pt
Síntese assimétrica coletiva dos alcaloides Strychnos via cicloadições de tiofeno S,S-dióxido
Por que moléculas minúsculas inspiradas em venenos importam
Os alcaloides Strychnos são uma família de compostos naturais célebres por sua potência extrema — a estricnina é o exemplo notório — e por suas formas intrincadas e tridimensionais. Essas moléculas têm fascinado químicas por serem ao mesmo tempo perigosas e potencialmente úteis, com algumas mostrando promessa contra cânceres resistentes a medicamentos. Ainda assim, sua complexidade arquitetural as torna muito difíceis de construir em laboratório. Este artigo revela uma nova forma simplificada de construir diversas moléculas Strychnos de maneira controlada e eficiente, abrindo caminhos para estudos mais seguros e possíveis novos fármacos derivados desses venenos outrora temidos.
Construindo formas complexas a partir de peças simples
Os autores buscaram cumprir os ideais modernos da síntese química: reações curtas, com pouco desperdício e capazes de produzir múltiplas moléculas relacionadas a partir de uma via comum. Eles concentraram-se no núcleo denso e repleto de anéis compartilhado pelos alcaloides Strychnos e perguntaram se essa estrutura poderia ser montada a partir de blocos mais simples em apenas algumas etapas. O plano baseou‑se na união de um fragmento indólico — um arcabouço comum na biologia — a um parceiro especial chamado tiofeno S,S‑dióxido. Quando esses dois se encontram, sofrem um potente evento de formação de anel chamado cicloadição de Diels–Alder, seguido pela perda limpa de dióxido de enxofre. Essa cascata converte peças iniciais relativamente planas em sistemas anelares complexos e tridimensionais essencialmente em um único passo.
Um atalho químico versátil
Para transformar essa ideia em uma caixa de ferramentas prática, a equipe primeiro desenvolveu versões altamente seletivas dessas reações de cicloadição. Ao anexar um “pegador” quiral barato (um grupo camforsultama) ao tiofeno S,S‑dióxido, puderam direcionar a reação para formar quase exclusivamente um produto imagem‑especular — uma característica crucial para moléculas bioativas, que frequentemente se comportam de maneira muito diferente de seus enantiômeros. Demonstraram que uma ampla variedade de parceiros indólicos, com muitos substituintes diferentes, reagem suavemente sob condições brandas para dar produtos indolina tricíclicos como diastereômeros únicos. Esses produtos não são apenas degraus rumo aos alcaloides Strychnos, mas também estruturas atraentes para a química medicinal por si mesmas.
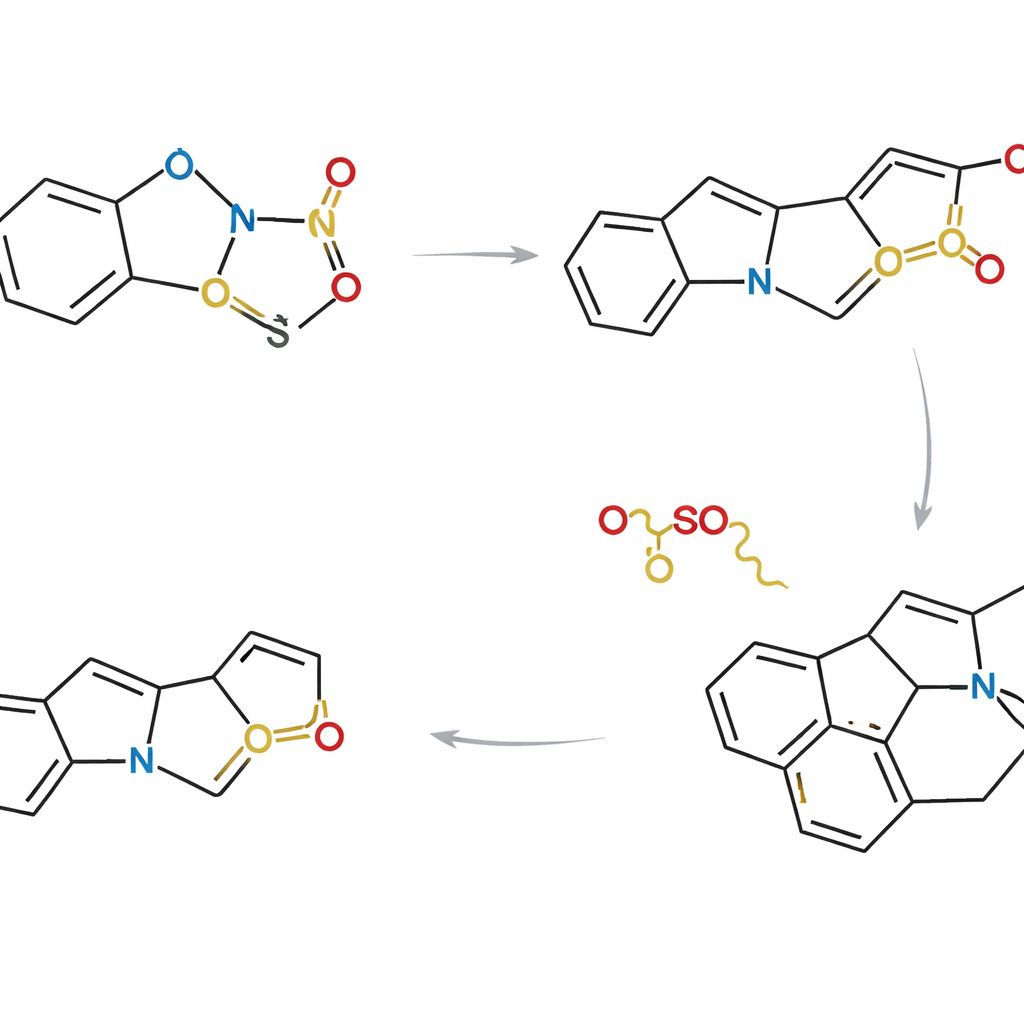
Reunindo muitos produtos naturais em uma única estratégia
Com esse controle em mãos, os pesquisadores desenharam três rotas complementares que diferem em como e quando os parceiros indólico e tiofeno são ligados. Em uma abordagem, os dois fragmentos são conectados antes da cicloadição, de modo que a reação ocorre dentro de uma única molécula. Em outras, eles reagem primeiro como moléculas separadas e então sofrem fechamento interno de anel. Ao escolher cuidadosamente substituintes e sequências reacionais, a equipe conseguiu convergir para um intermediário avançado comum que fica no ponto de ramificação da família Strychnos. A partir desse arcabouço compartilhado, completaram sínteses assimétricas de oito produtos naturais, incluindo akuammicina, lagumicina, norfluorocurarina, várias alstolucinas e echitamidina — frequentemente nas rotas mais curtas e com maior eficiência atômica relatadas até hoje.
Resolvido um desafio sintético centenário
Uma das demonstrações mais impressionantes é a primeira síntese total da brucina, uma prima química próxima da estricnina conhecida há mais de 200 anos e amplamente usada como agente de resolução quiral, mas que nunca havia sido construída completamente a partir do zero. O anel de indolina da brucina é incomumente rico em elétrons e propenso à degradação, o que desencorajou tentativas anteriores. Ao ajustar sua cascata baseada em tiofeno e gerenciar cuidadosamente as condições reacionais, os autores conseguiram forjar o delicado arcabouço da brucina em apenas nove etapas lineares a partir de um material de partida comercial simples. Também alcançaram uma síntese assimétrica da estricnina em dez etapas, a rota quiral mais concisa relatada até o momento.
Observando reações com aprendizado de máquina
Para entender por que suas reações dão resultados tão precisos, a equipe combinou química quântica de alto nível com simulações modernas de aprendizado de máquina. Esses cálculos revelaram que, em alguns casos, a reação não progride em um movimento suave, mas por meio de uma dança desigual e em etapas: uma ligação carbono–carbono se forma primeiro, um intermediário raso é brevemente acessado e então o dióxido de enxofre é expelido quase de forma espontânea enquanto o sistema desliza pela paisagem energética. A cadeia lateral quiral de camforsultama inclina sutilmente esse caminho, tornando uma disposição tridimensional muito mais fácil de alcançar do que a outra. Essa visão mecanística fornece diretrizes para projetar novas cascatas baseadas em tiofeno além da família Strychnos.
De toxinas mortais a ferramentas úteis
No conjunto, o estudo mostra que tiofenos S,S‑dióxidos podem agir como peças poderosas e programáveis, “carregadas” para montar arquiteturas moleculares intrincadas. Ao explorar seu impulso intrínseco de perder dióxido de enxofre, os autores engenharam reações em cascata que convertem rapidamente fragmentos simples nos sistemas anelares emaranhados dos alcaloides Strychnos com alta seletividade e passos mínimos desperdiçados. Para não especialistas, a conclusão é que os químicos estão aprendendo a transformar até venenos notórios em plataformas versáteis para descoberta, usando desenho reacional inteligente e insight computacional para explorar o espaço químico complexo de forma mais eficiente do que nunca.
Citação: Park, K.H.‘., Park, J., Frank, N. et al. Collective asymmetric synthesis of the Strychnos alkaloids via thiophene S,S-dioxide cycloadditions. Nat. Chem. 18, 782–789 (2026). https://doi.org/10.1038/s41557-025-02041-1
Palavras-chave: Alcaloides Strychnos, Síntese assimétrica, Cascatas de cicloadição, Tiofenos S,S-dióxidos, Química de produtos naturais