Clear Sky Science · zh
工程化外膜囊泡增强实体瘤CAR-T细胞疗法
重启机体的抗癌战士
近年来许多最显著的癌症缓解来自CAR-T细胞疗法,患者自身的免疫细胞被重新编程去追杀癌细胞。然而对于乳腺癌和肝癌等实体瘤,这种方法常常受阻:肿瘤的保护性“邻里”和不断变化的分子“身份标签”使恶性细胞能够躲藏或反击。本研究提出了一种巧妙的辅助系统,基于来自细菌的微小囊泡,既能打开肿瘤的防御,又能在肿瘤细胞上标记明确的靶点,从而帮助CAR-T细胞更有效地识别并摧毁它们。
为何“超充能”的T细胞在实体瘤中受挫
CAR-T细胞通过识别癌细胞表面的特定标志物来发挥作用。血液肿瘤通常始终表达这些标志物,但实体瘤表现不均:有些细胞带有靶点,另一些则没有,存活下来的细胞甚至可以停止表达该靶点。与此同时,实体瘤被一种充满抑制性细胞和信号的敌对环境包围,会关闭T细胞的活性。其中一个关键刹车是肿瘤细胞表面的PD-L1与T细胞上的PD-1之间的分子握手,这告诉免疫系统退下。当CAR-T细胞开始攻击时,它们释放的炎性分子反而可能促使PD-L1水平进一步上升,进而削弱自身的效力。
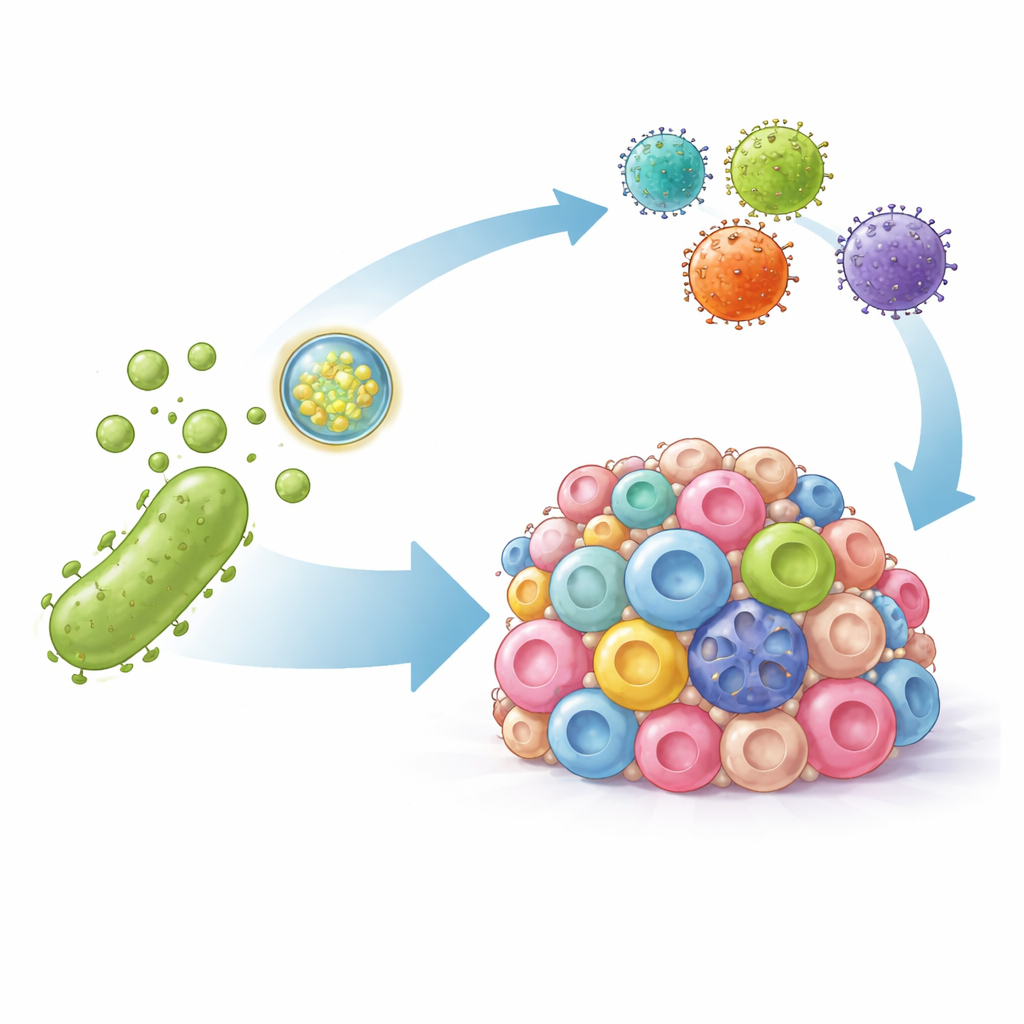
把细菌囊泡变成精准递送载体
研究人员转而利用细菌外膜囊泡——细菌自然释放的纳米级小泡,能够激发免疫反应。他们对这些囊泡进行了两方面的工程改造。首先,在囊泡表面装饰了可紧密结合PD-L1的抗体片段,使囊泡能定向进入肿瘤细胞并物理阻断这一免疫抑制信号。其次,他们将编码人工HER2标志物的DNA装入囊泡。一旦这些DNA被递送入肿瘤细胞,便能使细胞暂时在表面展示HER2,从而将原本难以察觉的癌细胞标记为可被CAR-T细胞识别的目标。
改写肿瘤周围环境
在乳腺癌小鼠模型中,改造后的囊泡在肿瘤中高效累积并重塑局部免疫格局。接受囊泡处理的肿瘤中抑制性细胞类型减少,例如调节性T细胞、某些巨噬细胞和髓源性抑制细胞,而具有攻击性的防御细胞如杀伤性T细胞和自然杀伤细胞增多。这些T细胞产生更多穿孔素和颗粒酶——可在癌细胞上打孔的分子——以及更多炎性信使分子,例如干扰素-γ和肿瘤坏死因子。通过阻断PD-L1并激活固有免疫,囊泡将一个冷漠、保护性的肿瘤“邻里”转变为欢迎并维持免疫进攻的环境。
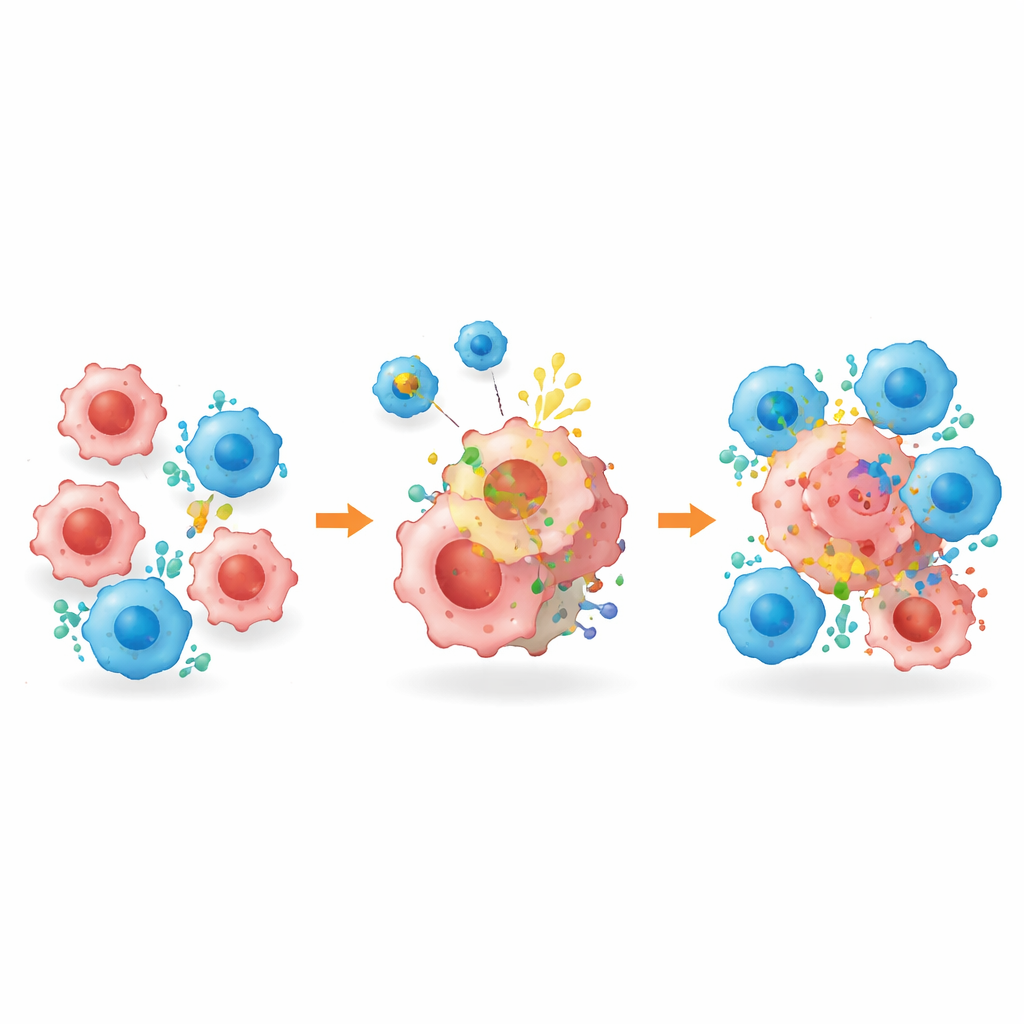
为隐匿的肿瘤细胞贴上消除标签
除了重塑肿瘤环境外,该平台(命名为BROAD-CAR)还直接解决了靶点缺失的问题。在包含HER2阳性和HER2阴性细胞的混合肿瘤中,传统的针对HER2的CAR-T疗法最初缩小了肿瘤,但留下了失去靶点的细胞,导致肿瘤再生长。然而与BROAD-CAR联合使用时,肿瘤几乎被完全清除:囊泡使HER2在先前为阴性的细胞上出现,使CAR-T细胞能够识别并杀死它们。同样策略也在原本不表达HER2的肝肿瘤中奏效。重要的是,详细分析显示HER2的装饰仅限于肿瘤组织,在健康器官或免疫细胞中未检测到表达,且治疗并未在小鼠中引起明显器官损伤或体重下降。
对复发与转移的持久保护
益处超出了初次肿瘤控制。在乳腺癌模型中,BROAD-CAR与CAR-T联合治疗不仅缩小了原发肿瘤,还大幅减少了肺转移。完全治愈的小鼠在随后再次挑战癌细胞时表现出抗性——无论这些细胞是否表达HER2——这表明初期的强烈免疫攻击诱发了更广泛且持久的肿瘤免疫记忆。这提示该平台可能不仅增强单一工程化T细胞产品,还能帮助更广泛的免疫系统更彻底地识别肿瘤。
这对未来癌症治疗意味着什么
总体而言,研究表明细菌囊泡可以被改造为安全、可调的辅助工具,使CAR-T疗法在对抗棘手的实体瘤时效果大幅提升。通过同时解除免疫刹车并在肿瘤细胞上临时标记清晰的靶点,BROAD-CAR系统使工程化T细胞能够在小鼠中清除多样甚至无靶点的癌症,同时避免伤及健康组织。如果在人类中也能得到类似结果,这一方法可能将CAR-T治疗扩大到更多实体瘤患者,并降低因抗原丧失导致复发的可能,为帮助免疫系统完成其任务提供一种有力的新途径。
引用: Li, X., Li, X., Shi, J. et al. Engineered outer membrane vesicles enhance solid tumour CAR-T cell therapy. Nat. Biomed. Eng 10, 660–675 (2026). https://doi.org/10.1038/s41551-025-01575-6
关键词: CAR-T细胞疗法, 实体瘤, 肿瘤微环境, 细菌外膜囊泡, 癌症免疫疗法