Clear Sky Science · sv
Konstruerade yttre membranvesiklar förbättrar CAR-T-cellterapi mot solida tumörer
Starta om kroppens cancerbekämpare
Många av de mest dramatiska cancerremissionerna på senare år har kommit från CAR-T-cellterapi, där en patients egna immunceller omprogrammeras för att jaga cancer. För solida tumörer som bröst- och levercancer stannar dock ofta denna strategi av: tumörens skyddande miljö och skiftande molekylära “ID‑taggar” gör att maligna celler kan gömma sig eller slå tillbaka. Denna studie presenterar ett smart hjälpsystem baserat på små bubblor från bakterier som både kan öppna upp tumörens försvar och måla tydliga mål på tumörceller, så att CAR-T‑celler kan hitta och förgöra dem mer effektivt.
Varför superladdade T‑celler har svårt i solida tumörer
CAR-T‑celler känner igen cancerceller genom att fästa vid specifika markörer på deras yta. Blodcancer visar vanligtvis dessa markörer konsekvent, men solida tumörer är fläckiga: vissa celler bär målet, andra inte, och överlevande celler kan helt enkelt sluta visa det. Samtidigt omges solida tumörer av en fientlig miljö full av celler och signaler som slår ner T‑celler. En viktig broms är ett molekylärt handslag mellan PD‑L1 på tumörceller och PD‑1 på T‑celler, vilket säger åt immunsystemet att avstå. När CAR-T‑celler börjar attackera släpper de ut inflammatoriska molekyler som paradoxalt nog kan driva upp PD‑L1‑nivåerna ytterligare och därigenom dämpa deras egen effekt.
Förvandla bakteriella bubblor till precisa budbärare
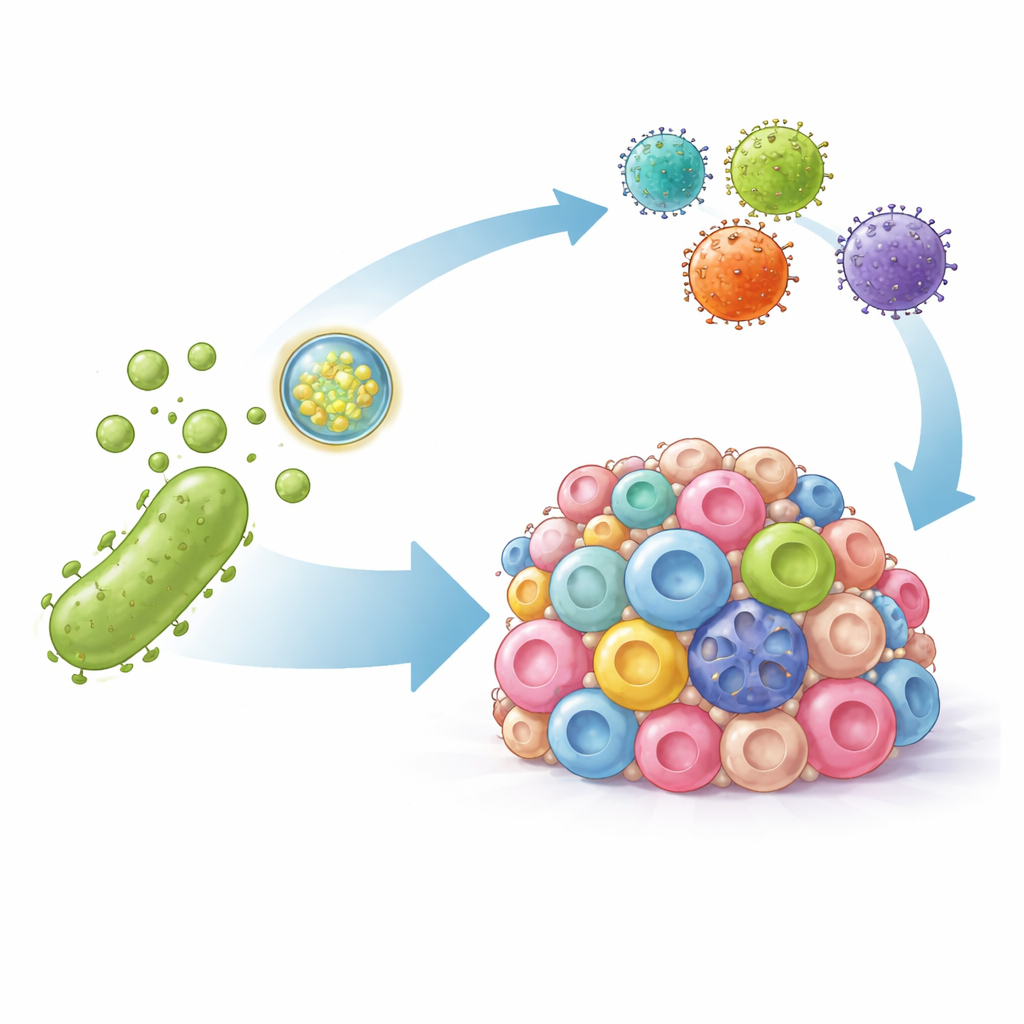
Forskarna vände sig till bakterieyttremembranvesiklar—naturligt förekommande nanoskala bubblor som bakterier släpper och som kan väcka immunsvar. De konstruerade dessa vesiklar på två sätt. För det första dekorerade de ytan med en del av en antikropp som fäster starkt vid PD‑L1, så att vesiklarna söker sig till tumörceller och fysiskt blockerar denna immundämpande signal. För det andra packade de vesiklarna med DNA‑instruktioner som kodar en artificiell version av HER2‑markören, ett välkänt mål för CAR‑T‑celler. När detta DNA levererats in i tumörceller får det dem att tillfälligt visa HER2 på ytan, vilket i praktiken märker även tidigare osynliga cancerceller för angrepp.
Omskrivning av tumörens närmiljö
I musmodeller av bröstcancer ackumulerades de modifierade vesiklarna effektivt i tumörer och omformade den lokala immunmiljön. Tumörer som behandlats med dessa vesiklar visade färre suppressiva celltyper, såsom regulatoriska T‑celler, vissa makrofager och myeloida suppressorceller, och fler aggressiva försvarare som cytotoxiska T‑celler och NK‑celler. Dessa T‑celler producerade mer perforin och granzyme—molekyler som gör hål på cancerceller—och fler inflammatoriska budbärare såsom interferon‑gamma och tumörnekrosfaktor. Genom att blockera PD‑L1 samtidigt som medfödda immunförsvaret aktiverades, förvandlade vesiklarna en kall, skyddande tumörmiljö till en som välkomnar och upprätthåller en immunattack.
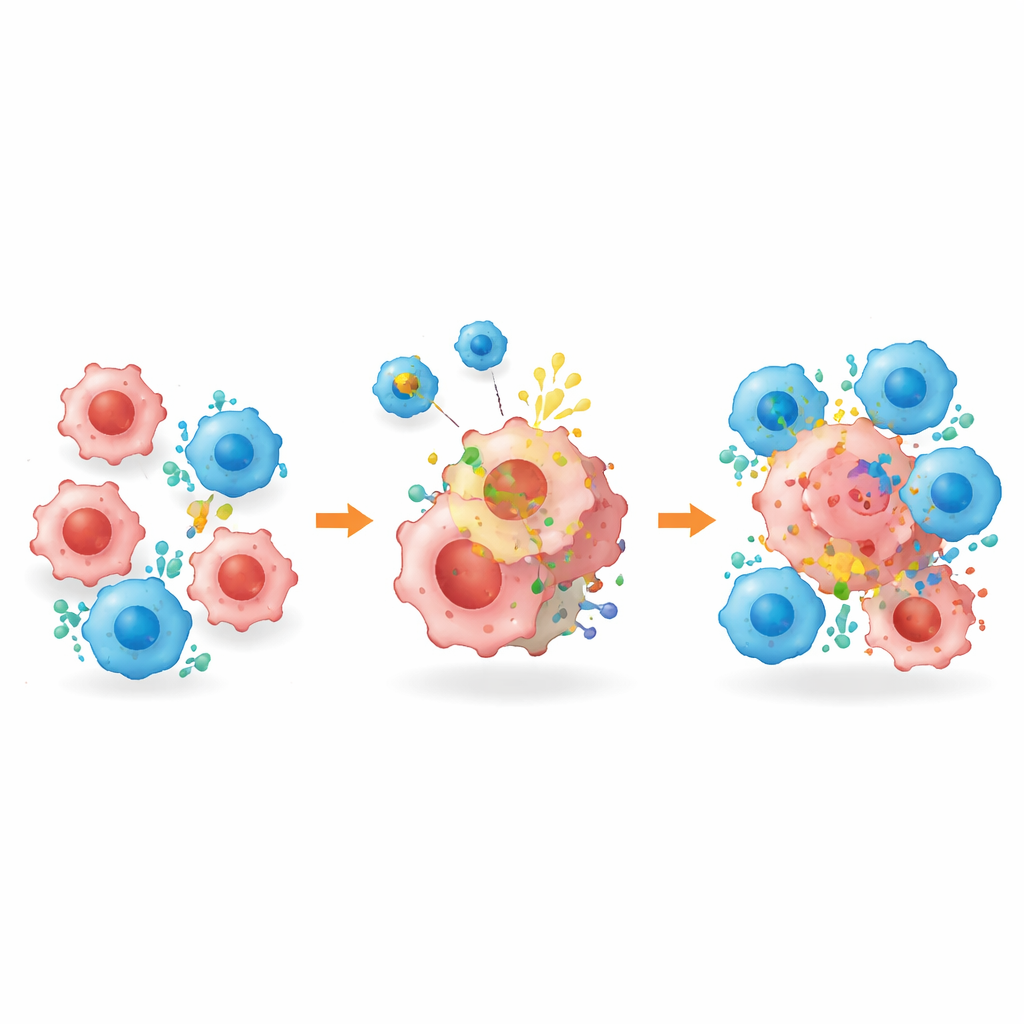
Märkning av dolda tumörceller för eliminering
Utöver att omforma tumörmiljön tog plattformen—kallad BROAD‑CAR—direkt itu med problemet med saknade mål. I blandade tumörer som innehöll både HER2‑positiva och HER2‑negativa celler krympte konventionell HER2‑inriktad CAR‑T‑terapi inledningsvis tumörerna men lämnade kvar celler som förlorat målet, vilket ledde till återväxt. När den kombinerades med BROAD‑CAR utplånades dock tumörerna nästan helt: vesiklarna gjorde att HER2 dök upp på tidigare negativa celler, vilket gjorde att CAR‑T‑celler kunde känna igen och döda dem. Samma strategi fungerade i levertumörer som ursprungligen saknade HER2. Viktigt var att detaljerade analyser visade att HER2‑dekorationen förblev begränsad till tumörvävnad, utan påvisbar uttryck i friska organ eller immunceller, och behandlingen orsakade inga uppenbara organskador eller viktminskning hos mössen.
Varaktigt skydd mot återkomst och spridning
Fördelarna sträckte sig bortom den initiala tumören. I bröstcancermodeller krympte den kombinerade BROAD‑CAR‑ och CAR‑T‑behandlingen inte bara primära tumörer utan minskade också kraftigt lungmetastaser. Möss som blev helt botade motstod senare återutmaning med cancerceller, oavsett om dessa celler uttryckte HER2 eller inte, vilket antyder att den intensiva inledande striden utlöste ett bredare, långtidsbeständigt immunologiskt minne mot tumören. Detta tyder på att plattformen kan göra mer än att stärka en enskild konstruerad T‑cellsprodukt—den kan också hjälpa det bredare immunsystemet att lära sig känna igen cancern mer fullständigt.
Vad detta kan innebära för framtidens cancervård
Sammanfattningsvis visar studien att bakteriella vesiklar kan omvandlas till säkra, anpassningsbara hjälpare som får CAR‑T‑terapi att fungera mycket bättre mot svårövervinnerliga solida tumörer. Genom både att lyfta immundämpningar och måla tydliga, tillfälliga mål på tumörceller lät BROAD‑CAR‑systemet konstruerade T‑celler rensa ut olika och till och med mållösa cancerformer hos möss, samtidigt som friska vävnader undveks. Om liknande resultat uppnås hos människor kan detta tillvägagångssätt utöka CAR‑T‑behandling till betydligt fler patienter med solida tumörer och göra återfall på grund av antigenförlust mindre sannolika—vilket erbjuder ett kraftfullt nytt sätt att hjälpa immunsystemet att slutföra det det påbörjar.
Citering: Li, X., Li, X., Shi, J. et al. Engineered outer membrane vesicles enhance solid tumour CAR-T cell therapy. Nat. Biomed. Eng 10, 660–675 (2026). https://doi.org/10.1038/s41551-025-01575-6
Nyckelord: CAR-T-cellterapi, solida tumörer, tumörmikromiljö, bakteriella yttre membranvesiklar, cancerimmunterapi