Clear Sky Science · tr
Genetiği Değiştirilmiş dış zar vezikülleri katı tümör CAR-T hücre tedavisini güçlendiriyor
Vücudun Kanser Savaşçılarını Yeniden Başlatmak
Son yıllardaki en çarpıcı kanser gerilemelerinin çoğu, hastanın kendi bağışıklık hücrelerinin kanseri avlamaya yeniden programlandığı CAR-T hücre tedavisinden geldi. Ancak meme ve karaciğer kanserleri gibi katı tümörlerde bu yaklaşım genellikle tıkanıyor: tümörün koruyucu çevresi ve değişken moleküler “kimlik etiketleri” kötü huylu hücrelerin saklanmasına veya karşı koymasına izin veriyor. Bu çalışma, bakterilerden kaynaklanan küçük kabarcıklara dayanan zekice bir yardımcı sistem sunuyor; bu sistem hem tümörün savunmasını açıyor hem de tümör hücrelerine net hedefler boyayarak CAR-T hücrelerinin onları daha etkili biçimde bulup yok etmesini sağlıyor.
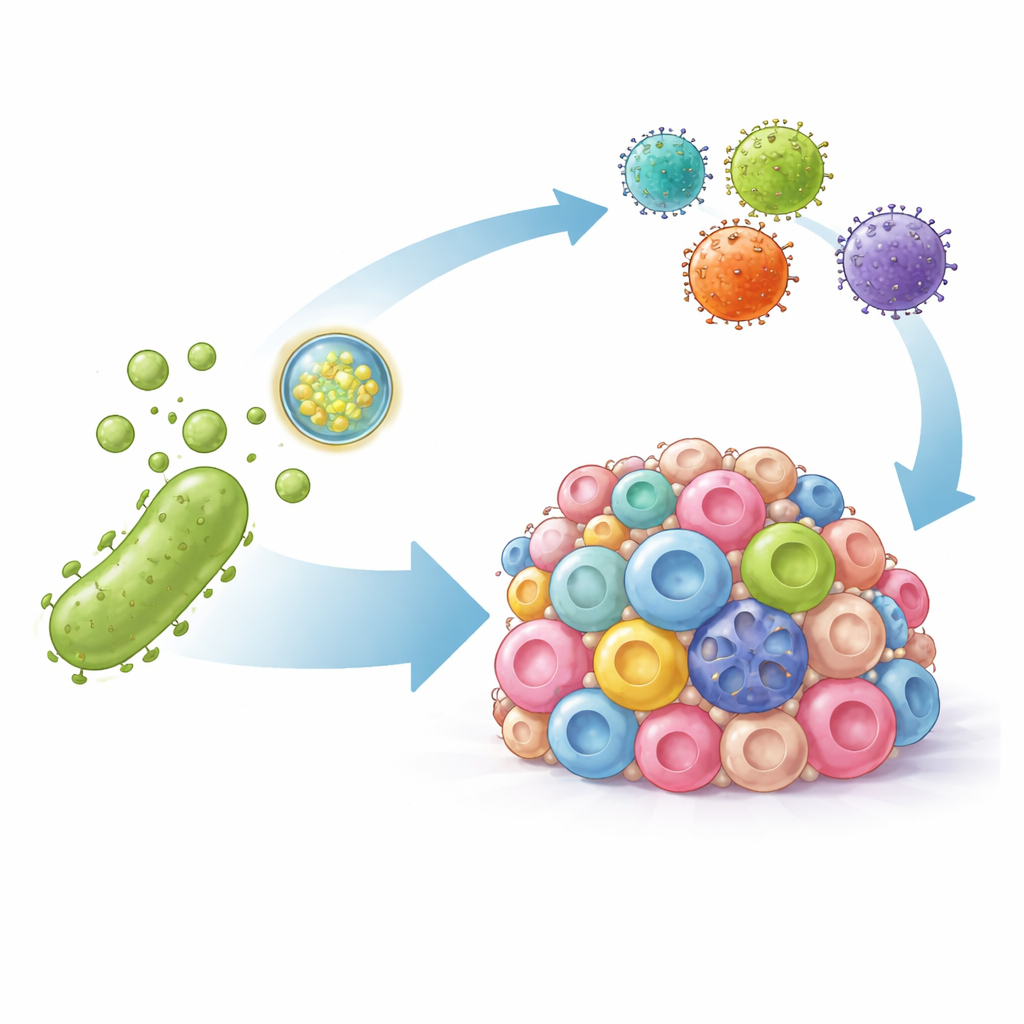
Gelişmiş T Hücrelerinin Katı Tümörlerde Neden Zorlandığı
CAR-T hücreleri, kanser hücrelerini yüzeylerindeki belirli işaretçilere tutunarak tanır. Kan dolaşımı kaynaklı kanserler genellikle bu işaretçileri tutarlı şekilde gösterirken, katı tümörler yamalıdır: bazı hücrelerde hedef bulunur, bazılarında bulunmaz ve hayatta kalan hücreler basitçe onu göstermeyi bırakabilir. Aynı zamanda katı tümörler, T hücrelerini kapatan hücreler ve sinyallerle dolu düşmanca bir ortamla çevrilidir. Önemli bir fren, tümör hücrelerindeki PD-L1 ile T hücrelerindeki PD-1 arasındaki moleküler tokalaşmadır; bu, bağışıklık sistemine geri çekilmesini söyler. CAR-T hücreleri saldırmaya başladıkça, paradoksal olarak PD-L1 düzeylerini daha da yükseltebilen inflamatuar moleküller salgılarlar ve bu da kendi etkilerini daha da köreltir.
Bakteriyel Kabarcıkları Hassas Kurye Haline Getirmek
Araştırmacılar, bağışıklık yanıtlarını uyandırabilen bakteriler tarafından doğal olarak salgılanan nanoskaladaki dış zar veziküllerine yöneldiler. Bu vezikülleri iki biçimde mühendisliklediler. Öncelikle yüzeylerini PD-L1’e sıkıca yapışan bir antikor parçasıyla süslediler; böylece veziküller tümör hücrelerine yöneliyor ve bu bağışıklık baskılayıcı sinyali fiziksel olarak engelliyor. İkinci olarak, vezikülleri yapay bir HER2 işaretçisini kodlayan DNA talimatlarıyla doldurdular. Bu DNA tümör hücrelerine teslim edildiğinde, hücrelerin geçici olarak yüzeylerinde HER2 göstermesini sağlıyor; böylece daha önce görünmez olan kanser hücreleri bile saldırı için etiketlenmiş oluyor.
Tümör Çevresini Yeniden Yazmak
Meme kanseri fare modellerinde, modifiye veziküller tümörlerde etkin şekilde birikti ve yerel bağışıklık manzarasını yeniden şekillendirdi. Bu veziküllerle tedavi edilen tümörlerde düzenleyici T hücreleri, belirli makrofaj alt tipleri ve miyeloid kaynaklı baskılayıcı hücreler gibi baskılayıcı hücre tipleri daha az; katil T hücreleri ve doğal öldürücü hücreler gibi daha saldırgan savunucular ise daha fazlaydı. Bu T hücreleri, kanser hücrelerinde delikler açan perforin ve granzim gibi molekülleri ve interferon-gama ile tümör nekroz faktörü gibi daha fazla inflamatuar haberciyi üretti. PD-L1’i bloke ederken aynı anda doğuştan gelen bağışıklığı da aktive ederek, veziküller soğuk, koruyucu bir tümör çevresini bağışıklık saldırısını karşılayan ve sürdüren bir ortama dönüştürdü.
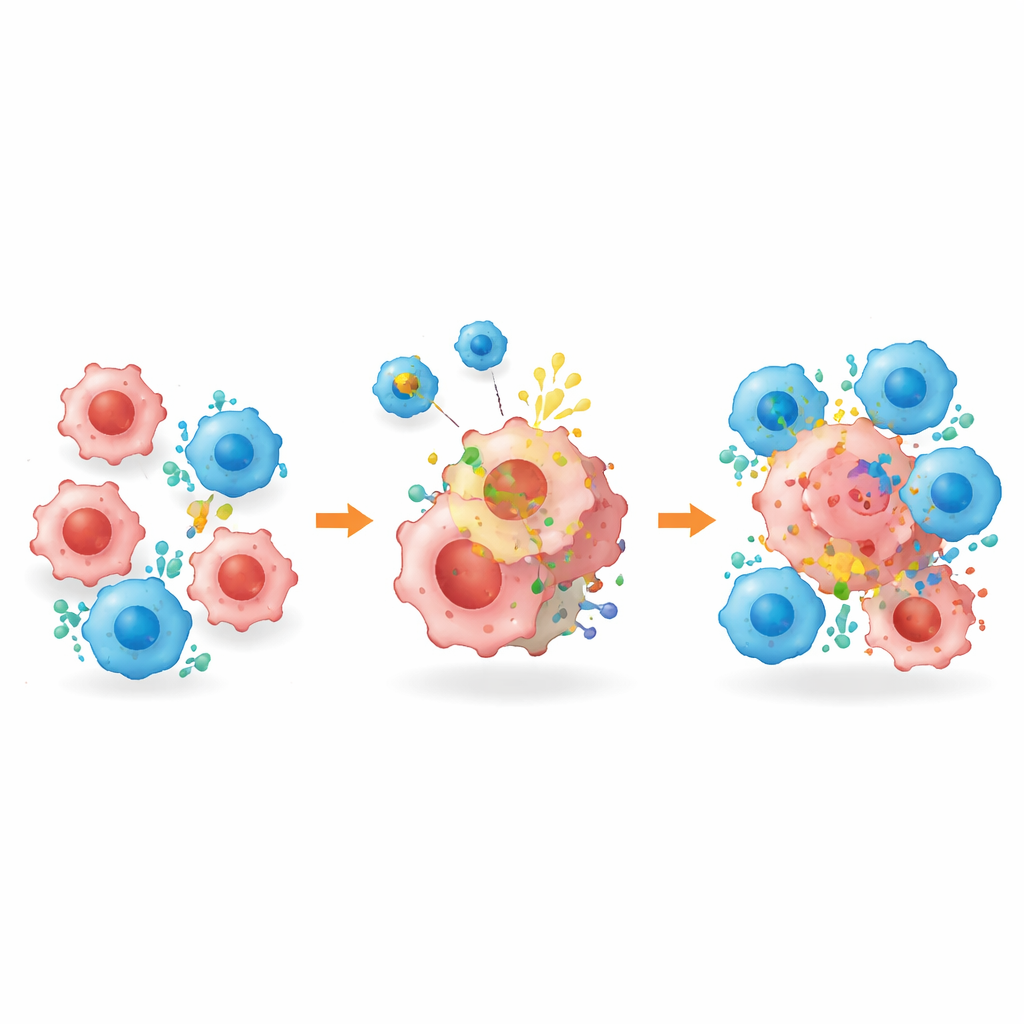
Saklı Tümör Hücrelerini Yok Etmeye Etiketlemek
Tümör ortamını yeniden şekillendirmenin ötesinde, BROAD-CAR adı verilen platform doğrudan eksik hedef sorununu ele aldı. Hem HER2-pozitif hem de HER2-negatif hücreler içeren karışık tümörlerde, geleneksel HER2 yönelimli CAR-T tedavisi başlangıçta tümörleri küçülttü ama hedefi kaybetmiş hücreleri geride bırakarak yeniden büyümeye yol açtı. Ancak BROAD-CAR ile kombine edildiğinde, tümörler neredeyse yok oldu: veziküller daha önce negatif olan hücrelerin yüzeyinde HER2’nin görünmesini sağladı, böylece CAR-T hücreleri onları tanıyıp öldürebildi. Aynı strateji başlangıçta hiç HER2’si olmayan karaciğer tümörlerinde de işe yaradı. Önemli olarak, ayrıntılı analizler HER2 süslemesinin sağlıklı organlarda veya bağışıklık hücrelerinde tespit edilebilir bir şekilde ortaya çıkmadığını; tedavinin farelerde belirgin organ hasarına ya da kilo kaybına neden olmadığını gösterdi.
Tekrarlama ve Yayılmaya Karşı Kalıcı Koruma
Faydalar başlangıçtaki tümörü aşarak devam etti. Meme kanseri modellerinde, BROAD-CAR ile birlikte uygulanan CAR-T tedavisi yalnızca primer tümörleri küçültmekle kalmadı, aynı zamanda akciğer metastazlarını da keskin şekilde azalttı. Tamamen iyileşen fareler, daha sonra kanser hücreleriyle yeniden meydan okumaya karşı direnç gösterdi; bu hücreler HER2 ifade etsin ya da etmesin, bu da yoğun başlangıç muharebesinin tümöre karşı daha geniş, uzun ömürlü bir bağışıklık belleği tetiklemiş olabileceğini düşündürüyor. Bu, platformun yalnızca tek bir mühendislikli T hücre ürününü güçlendirmekle kalmayıp, aynı zamanda daha geniş bağışıklık sisteminin kanseri daha kapsamlı biçimde tanımasına da yardımcı olabileceği fikrine işaret ediyor.
Geleceğin Kanser Bakımı İçin Ne Anlatıyor
Genel olarak çalışma, bakteriyel veziküllerin CAR-T tedavisini inatçı katı tümörlere karşı çok daha etkili kılacak güvenli, uyarlanabilir yardımcılar haline getirilebileceğini gösteriyor. Hem bağışıklık frenlerini kaldırarak hem de tümör hücreleri üzerinde geçici, net hedefler boyayarak BROAD-CAR sistemi, mühendislikli T hücrelerin farelerde çeşitli ve hatta hedefsiz kanserleri temizlemesine izin verdi; sağlıklı dokulardan kaçındı. Benzer sonuçlar insanlarda da elde edilirse, bu yaklaşım CAR-T tedavisini katı tümörü olan çok daha fazla hastaya genişletebilir ve antijen kaybına bağlı nüksleri daha az olası hale getirerek bağışıklık sisteminin başladığını bitirmesine güçlü yeni bir yol sunabilir.
Atıf: Li, X., Li, X., Shi, J. et al. Engineered outer membrane vesicles enhance solid tumour CAR-T cell therapy. Nat. Biomed. Eng 10, 660–675 (2026). https://doi.org/10.1038/s41551-025-01575-6
Anahtar kelimeler: CAR-T hücre tedavisi, katı tümörler, tümör mikroçevresi, bakteriyel dış zar vezikülleri, kanser immünoterapisi