Clear Sky Science · it
Vescicole di membrana esterna ingegnerizzate potenziano la terapia CAR-T contro i tumori solidi
Riavviare i combattenti contro il cancro del corpo
Molte delle remissioni più spettacolari degli ultimi anni derivano dalla terapia CAR-T, in cui le cellule immunitarie del paziente vengono riprogrammate per cercare e attaccare il cancro. Tuttavia, per i tumori solidi come quelli al seno e al fegato, questo approccio spesso si inceppa: il quartiere protettivo del tumore e le etichette molecolari “di riconoscimento” variabili consentono alle cellule maligne di nascondersi o contrattaccare. Questo studio presenta un sistema ausiliario ingegnoso basato su piccole bolle di origine batterica che può sia aprire le difese del tumore sia dipingere bersagli chiari sulle cellule tumorali, in modo che le CAR-T possano trovarle e distruggerle più efficacemente.
Perché le cellule T potenziate faticano nei tumori solidi
Le CAR-T riconoscono le cellule tumorali agganciandosi a marcatori specifici presenti sulla loro superficie. Nei tumori del sangue questi marcatori sono di solito stabili, ma nei tumori solidi la situazione è irregolare: alcune cellule portano il bersaglio, altre no, e le cellule sopravvissute possono semplicemente smettere di esprimerlo. Allo stesso tempo, i tumori solidi sono circondati da un ambiente ostile pieno di cellule e segnali che spengono le cellule T. Un freno chiave è la stretta molecolare tra PD-L1 sulle cellule tumorali e PD-1 sulle cellule T, che ordina al sistema immunitario di fermarsi. Quando le CAR-T cominciano ad attaccare rilasciano molecole infiammatorie che paradossalmente possono innalzare ulteriormente i livelli di PD-L1, attenuando così il loro stesso impatto.
Trasformare le bolle batteriche in corrieri di precisione
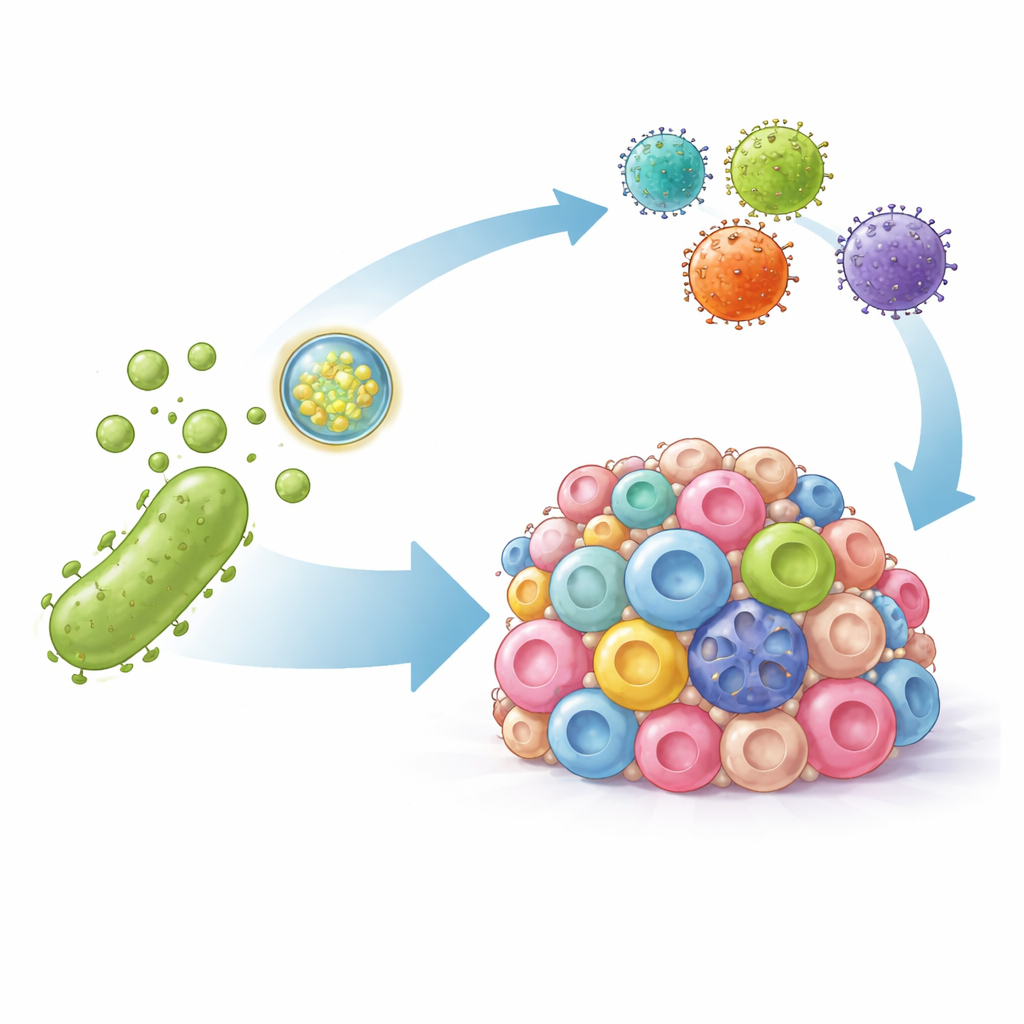
I ricercatori si sono orientati verso le vescicole di membrana esterna batteriche — bolle nanoscalari che i batteri rilasciano naturalmente e che possono risvegliare risposte immunitarie. Hanno ingegnerizzato queste vescicole in due modi. Primo, hanno decorato la loro superficie con un frammento di anticorpo che si lega saldamente a PD-L1, così le vescicole si dirigono verso le cellule tumorali e bloccano fisicamente questo segnale immunosoppressivo. Secondo, hanno caricato le vescicole con istruzioni di DNA che codificano una versione artificiale del marcatore HER2, un bersaglio ben noto per le CAR-T. Una volta consegnato nelle cellule tumorali, questo DNA induce temporaneamente l’espressione di HER2 sulla superficie cellulare, etichettando efficacemente anche le cellule precedentemente invisibili per l’attacco.
Riscrivere il quartiere tumorale
Nei modelli murini di tumore al seno, le vescicole modificate si accumulavano in modo efficiente nei tumori e rimodellavano il panorama immunitario locale. I tumori trattati con queste vescicole mostravano meno tipi cellulari soppressivi, come le cellule T regolatorie, alcuni macrofagi e le cellule soppressorie di derivazione mieloide, e più difensori aggressivi come le cellule T citotossiche e le cellule natural killer. Queste cellule T producevano più perforina e granzima — molecole che perforano le cellule tumorali — e più messaggeri infiammatori come l’interferone-gamma e il fattore di necrosi tumorale. Bloccando PD-L1 e attivando al contempo l’immunità innata, le vescicole hanno trasformato un microambiente tumorale freddo e protettivo in uno che favorisce e sostiene un assalto immunitario.
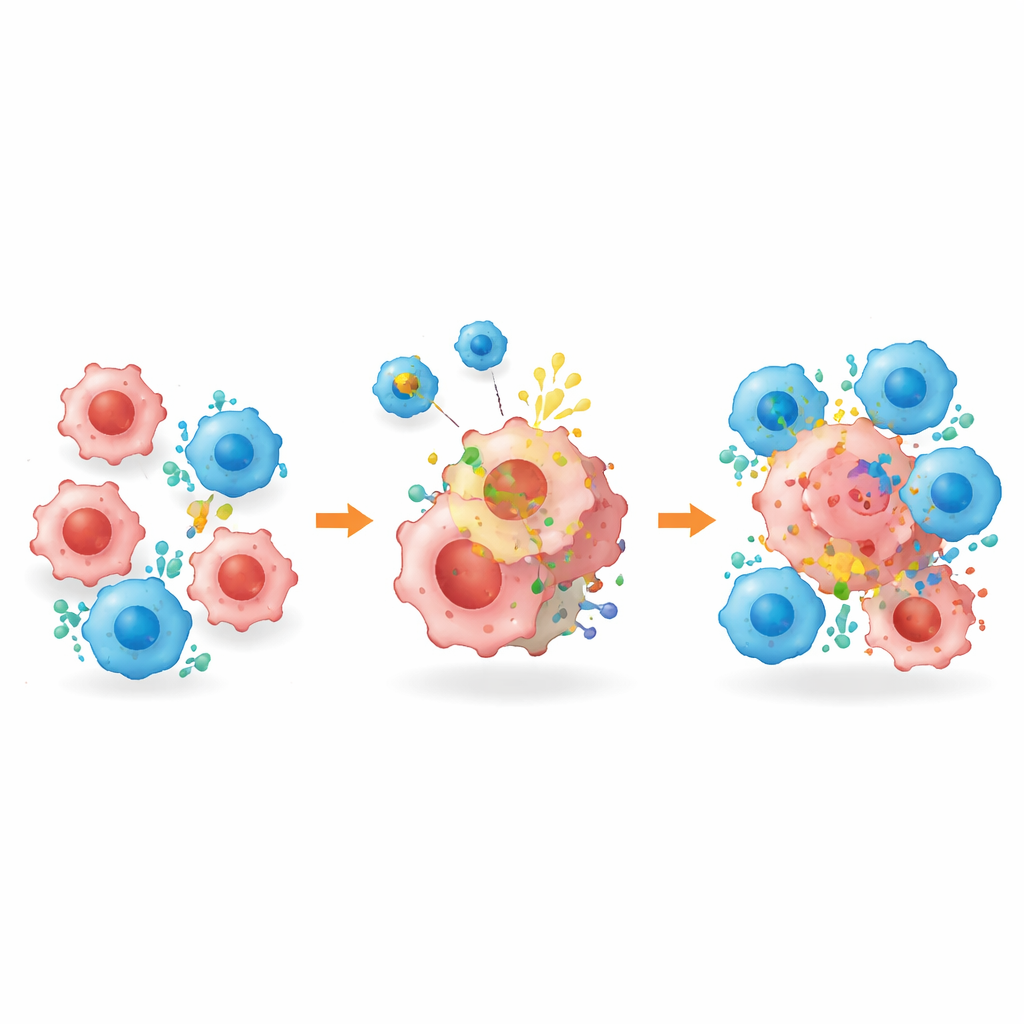
Etichettare le cellule tumorali nascoste per l’eliminazione
Oltre a rimodellare l’ambiente tumorale, la piattaforma — chiamata BROAD-CAR — ha affrontato direttamente il problema dei bersagli mancanti. In tumori misti contenenti sia cellule HER2-positive sia HER2-negative, la terapia CAR-T diretta contro HER2 inizialmente riduceva i tumori ma lasciava dietro cellule che avevano perso il bersaglio, portando a una ricrescita. Quando combinata con BROAD-CAR, però, i tumori furono quasi completamente eliminati: le vescicole inducevano la comparsa di HER2 su cellule precedentemente negative, permettendo alle CAR-T di riconoscerle e ucciderle. La stessa strategia ha funzionato in tumori epatici che inizialmente non esprimevano HER2. È importante che analisi dettagliate abbiano mostrato che la decorazione con HER2 rimaneva confinata al tessuto tumorale, senza espressione rilevabile negli organi sani o nelle cellule immunitarie, e il trattamento non ha causato danni evidenti agli organi né perdita di peso nei topi.
Protezione duratura contro recidiva e diffusione
I benefici si sono estesi oltre il tumore iniziale. Nei modelli di tumore al seno, il trattamento combinato BROAD-CAR e CAR-T non solo ha ridotto i tumori primari ma ha anche ridotto nettamente le metastasi polmonari. I topi completamente guariti hanno resistito a una successiva reintroduzione di cellule tumorali, indipendentemente dall’espressione di HER2, suggerendo che la risposta iniziale intensa ha scatenato una memoria immunitaria più ampia e duratura contro il tumore. Ciò suggerisce che la piattaforma potrebbe non solo potenziare un singolo prodotto di cellule T ingegnerizzate, ma anche aiutare il sistema immunitario più ampio a imparare a riconoscere il cancro in modo più completo.
Cosa potrebbe significare per la cura del cancro in futuro
Nel complesso, lo studio dimostra che le vescicole batteriche possono essere trasformate in helper sicuri e adattabili che rendono la terapia CAR-T molto più efficace contro i tumori solidi ostinati. Sia sollevando i freni immunitari sia dipingendo bersagli temporanei e chiari sulle cellule tumorali, il sistema BROAD-CAR ha permesso alle cellule T ingegnerizzate di eliminare tumori diversi e persino privi di bersaglio nei topi, evitando i tessuti sani. Se risultati simili si confermassero nell’uomo, questo approccio potrebbe estendere la terapia CAR-T a molti più pazienti con tumori solidi e rendere meno probabili le recidive dovute alla perdita di antigeni, offrendo un nuovo potente modo per aiutare il sistema immunitario a completare ciò che inizia.
Citazione: Li, X., Li, X., Shi, J. et al. Engineered outer membrane vesicles enhance solid tumour CAR-T cell therapy. Nat. Biomed. Eng 10, 660–675 (2026). https://doi.org/10.1038/s41551-025-01575-6
Parole chiave: terapia con cellule CAR-T, tumori solidi, microambiente tumorale, vesicole di membrana esterna batteriche, immunoterapia del cancro