Clear Sky Science · es
Vesículas de membrana externa diseñadas mejoran la terapia CAR-T contra tumores sólidos
Reiniciar a los combatientes del cuerpo contra el cáncer
Muchas de las remisiones más llamativas de cáncer en los últimos años han surgido de la terapia CAR-T, en la que las propias células inmunitarias del paciente se reprograman para buscar el cáncer. Sin embargo, en tumores sólidos como los de mama e hígado, este enfoque a menudo se estanca: el vecindario protector del tumor y las cambiantes “etiquetas de identidad” moleculares permiten que las células malignas se oculten o contraataquen. Este estudio presenta un sistema auxiliar ingenioso basado en pequeñísimas burbujas procedentes de bacterias que puede tanto abrir las defensas del tumor como pintar dianas claras en las células tumorales, de modo que las células CAR-T puedan encontrarlas y destruirlas con más eficacia.
Por qué las células T supercargadas tienen dificultades en tumores sólidos
Las células CAR-T reconocen las células cancerosas adhiriéndose a marcadores específicos en su superficie. Los cánceres de sangre suelen mostrar esos marcadores de forma consistente, pero los tumores sólidos son desiguales: algunas células portan el objetivo, otras no, y las células que sobreviven pueden simplemente dejar de mostrarlo. Al mismo tiempo, los tumores sólidos están rodeados por un entorno hostil repleto de células y señales que inhiben a las células T. Un freno clave es el apretón molecular entre PD-L1 en las células tumorales y PD-1 en las células T, que indica al sistema inmune que se detenga. A medida que las CAR-T comienzan a atacar, liberan moléculas inflamatorias que paradójicamente pueden aumentar aún más los niveles de PD-L1, debilitando su propio impacto.
Convertir burbujas bacterianas en mensajeros de precisión
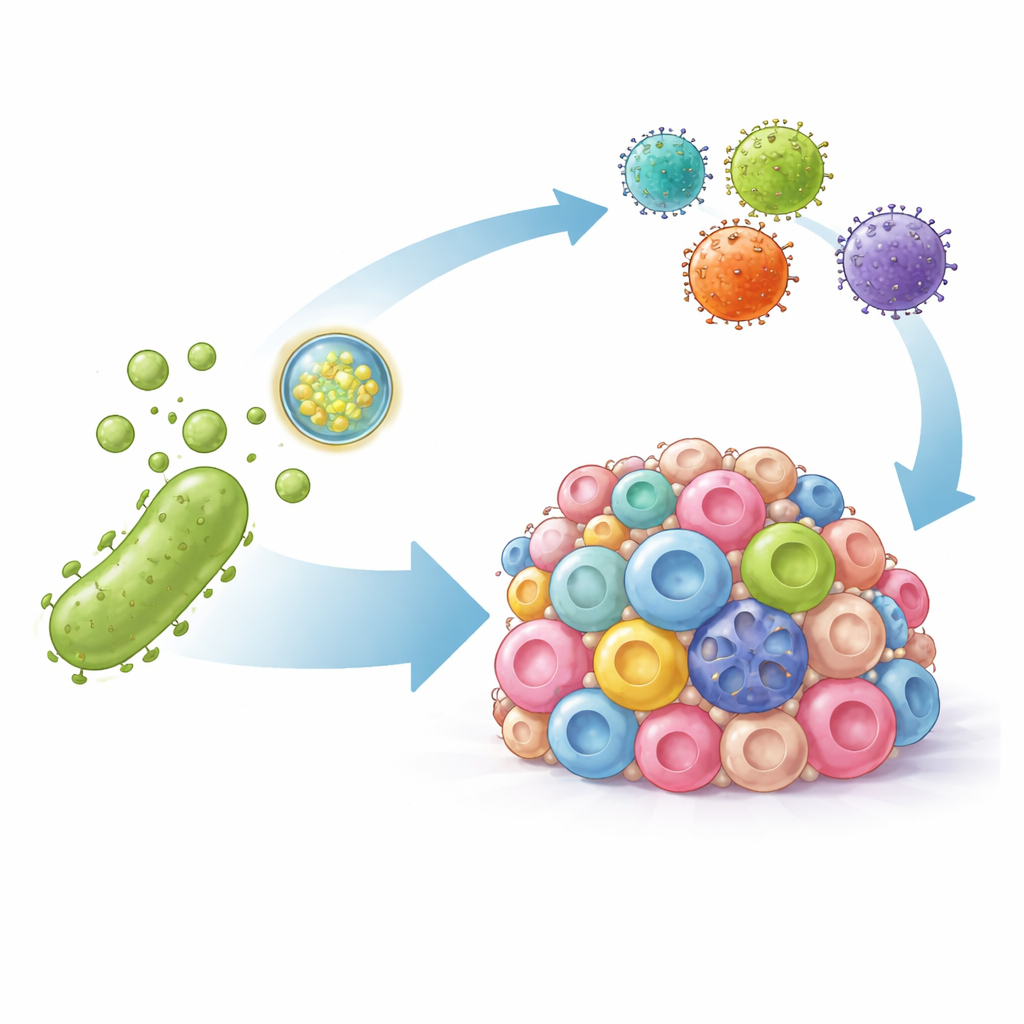
Los investigadores recurrieron a las vesículas de membrana externa bacterianas —burbujas nanoescalas naturales desprendidas por bacterias que pueden activar respuestas inmunitarias—. Modificaron estas vesículas de dos maneras. Primero, decoraron su superficie con un fragmento de anticuerpo que se adhiere con firmeza a PD-L1, de modo que las vesículas se dirigen hacia las células tumorales y bloquean físicamente esta señal inmunosupresora. Segundo, empaquetaron en las vesículas instrucciones en ADN que codifican una versión artificial del marcador HER2, un objetivo bien conocido para las células CAR-T. Una vez entregado a las células tumorales, este ADN hace que las células muestren temporalmente HER2 en su superficie, etiquetando incluso a las células cancerosas previamente invisibles para el ataque.
Reescribir el vecindario tumoral
En modelos murinos de cáncer de mama, las vesículas modificadas se acumularon de forma eficiente en los tumores y remodelaron el paisaje inmunitario local. Los tumores tratados con estas vesículas mostraron menos tipos celulares supresores, como células T reguladoras, ciertos macrófagos y células supresoras derivadas de la médula ósea, y más defensores agresivos como linfocitos T citotóxicos y células NK. Estas células T produjeron más perforina y granzima —moléculas que perforan las células cancerosas— y más mensajeros inflamatorios como interferón gamma y factor de necrosis tumoral. Al bloquear PD-L1 mientras también activaban la inmunidad innata, las vesículas convirtieron un vecindario tumoral frío y protector en uno que acoge y sostiene un asalto inmunitario.
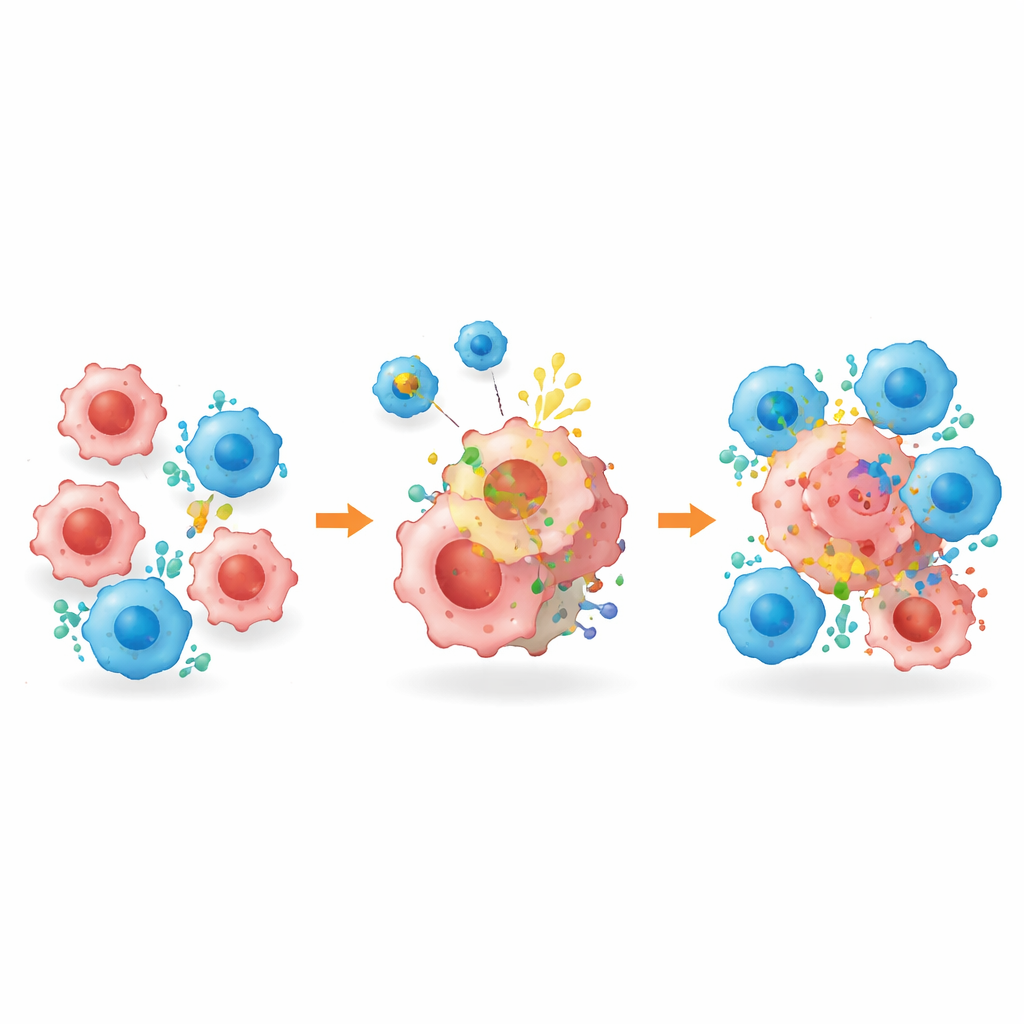
Etiquetar células tumorales ocultas para su eliminación
Más allá de remodelar el entorno tumoral, la plataforma —llamada BROAD-CAR— abordó directamente el problema de los objetivos ausentes. En tumores mixtos que contenían células HER2-positivas y HER2-negativas, la terapia CAR-T dirigida a HER2 convencional redujo inicialmente los tumores pero dejó células que habían perdido el objetivo, lo que condujo a la reaparición. Sin embargo, al combinarse con BROAD-CAR, los tumores quedaron casi eliminados: las vesículas provocaron la aparición de HER2 en células anteriormente negativas, lo que permitió a las CAR-T reconocerlas y eliminarlas. La misma estrategia funcionó en tumores hepáticos que no tenían HER2 desde el inicio. Es importante destacar que análisis detallados mostraron que la decoración con HER2 permaneció confinada al tejido tumoral, sin expresión detectable en órganos sanos o células inmunitarias, y el tratamiento no causó daños orgánicos evidentes ni pérdida de peso en los ratones.
Protección duradera contra recurrencia y diseminación
Los beneficios se extendieron más allá del tumor inicial. En modelos de cáncer de mama, el tratamiento combinado BROAD-CAR y CAR-T no solo redujo los tumores primarios, sino que también disminuyó drásticamente las metástasis pulmonares. Los ratones que se curaron completamente resistieron un reexposición posterior con células cancerosas, tanto si esas células expresaban HER2 como si no, lo que sugiere que la intensa batalla inicial desencadenó una memoria inmunitaria más amplia y duradera contra el tumor. Esto apunta a que la plataforma podría no solo potenciar un producto de células T diseñado, sino también ayudar al sistema inmune en general a aprender a reconocer el cáncer de forma más completa.
Qué podría significar esto para la atención futura del cáncer
En conjunto, el estudio muestra que las vesículas bacterianas pueden convertirse en ayudantes seguros y adaptables que mejoran considerablemente la eficacia de la terapia CAR-T contra tumores sólidos resistentes. Al levantar frenos inmunitarios y al mismo tiempo pintar objetivos temporales y claros en las células tumorales, el sistema BROAD-CAR permitió que las células T diseñadas eliminaran cánceres diversos e incluso carentes de diana en ratones, sin afectar a tejidos sanos. Si resultados similares se obtienen en humanos, este enfoque podría ampliar el uso de CAR-T a muchos más pacientes con tumores sólidos y reducir la probabilidad de recaídas por pérdida de antígeno, ofreciendo una nueva vía potente para ayudar al sistema inmunitario a culminar lo que inicia.
Cita: Li, X., Li, X., Shi, J. et al. Engineered outer membrane vesicles enhance solid tumour CAR-T cell therapy. Nat. Biomed. Eng 10, 660–675 (2026). https://doi.org/10.1038/s41551-025-01575-6
Palabras clave: terapia con células CAR-T, tumores sólidos, microambiente tumoral, vesículas de membrana externa bacteriana, inmunoterapia del cáncer